Fabricante de medicamentos: Merck Sharp & Dohme LLC (Updated: 2024-07-05)
ASPECTOS DESTACADOS DE LA INFORMACIÓN DE PRESCRIPCIÓN
ZEPATIER® (elbasvir y grazoprevir) comprimidos, para administración oral
Aprobación inicial en EE. UU.: 2016
ADVERTENCIA: RIESGO DE REACTIVACIÓN DEL VIRUS DE LA HEPATITIS B EN PACIENTES COINFECTADOS CON VHC Y VHB
Consulte la información completa de prescripción para obtener la advertencia completa en recuadro.
Se ha notificado la reactivación del virus de la hepatitis B (VHB), en algunos casos, lo que ha provocado hepatitis fulminante, insuficiencia hepática y muerte. (5.1)
CAMBIOS MAYORES RECIENTES
INDICACIONES Y USO
ZEPATIER es un producto de combinación de dosis fija que contiene elbasvir, un inhibidor de la NS5A del virus de la hepatitis C (VHC), y grazoprevir, un inhibidor de la proteasa NS3/4A del VHC, y está indicado para el tratamiento de la infección crónica por VHC de genotipo 1 o 4 en pacientes adultos y pediátricos de 12 años de edad o mayores o que pesen al menos 30 kg. ZEPATIER está indicado para su uso con ribavirina en ciertas poblaciones de pacientes. (1)
DOSIFICACIÓN Y ADMINISTRACIÓN
- Pruebas antes de iniciar la terapia:
- Dosificación recomendada en pacientes adultos y pediátricos de 12 años de edad o mayores o que pesen al menos 30 kg: Un comprimido administrado por vía oral una vez al día con o sin alimentos. (2.2)
| Población de pacientes | Tratamiento | Duración |
|---|---|---|
| Genotipo 1a: Tratamiento naive o con experiencia en PegIFN/RBV* sin polimorfismos de NS5A basales† |
ZEPATIER | 12 semanas |
| Genotipo 1a: Tratamiento naive o con experiencia en PegIFN/RBV* con polimorfismos de NS5A basales† |
ZEPATIER + ribavirina | 16 semanas |
| Genotipo 1b: Tratamiento naive o con experiencia en PegIFN/RBV* |
ZEPATIER | 12 semanas |
| Genotipo 1a o 1b: Con experiencia en PegIFN/RBV/PI‡ | ZEPATIER + ribavirina | 12 semanas |
| Genotipo 4: Tratamiento naive |
ZEPATIER | 12 semanas |
| Genotipo 4: Con experiencia en PegIFN/RBV* |
ZEPATIER + ribavirina | 16 semanas |
- Coinfección por VHC/VIH-1: Siga las recomendaciones de dosificación en la tabla anterior. (2.2)
- Insuficiencia renal, incluida la hemodiálisis: No se recomienda ningún ajuste de la dosis de ZEPATIER. Consulte la información de prescripción de ribavirina para la dosificación de ribavirina y las modificaciones de la dosis. (2.3)
FORMAS Y FUERZAS DE DOSIFICACIÓN
- Tabletas: 50 mg de elbasvir y 100 mg de grazoprevir (3)
CONTRAINDICACIONES
- Pacientes con insuficiencia hepática moderada o grave (Child-Pugh B o C). (4)
- Inhibidores de OATP1B1/3 que se sabe o se espera que aumenten significativamente las concentraciones plasmáticas de grazoprevir, inductores fuertes del CYP3A y efavirenz. (4)
- Si ZEPATIER se administra con ribavirina, también se aplican las contraindicaciones a la ribavirina. (4)
ADVERTENCIAS Y PRECAUCIONES
- Riesgo de reactivación del virus de la hepatitis B: Examine a todos los pacientes para detectar evidencia de infección por VHB actual o previa antes de iniciar el tratamiento contra el VHC. Controle a los pacientes coinfectados con VHC/VHB para detectar reactivación del VHB y brotes de hepatitis durante el tratamiento contra el VHC y el seguimiento posterior al tratamiento. Inicie la gestión adecuada del paciente para la infección por VHB según esté clínicamente indicado. (5.1)
- Elevaciones de ALT: Realice pruebas de laboratorio hepáticas antes de la terapia, en la semana 8 del tratamiento y según esté clínicamente indicado. Para los pacientes que reciben 16 semanas de terapia, realice pruebas de laboratorio hepáticas adicionales en la semana 12 del tratamiento. Para las elevaciones de ALT en ZEPATIER, siga las recomendaciones en la información completa de prescripción. (5.2)
- Riesgo de descompensación/insuficiencia hepática en pacientes con evidencia de enfermedad hepática avanzada: Se han notificado descompensación/insuficiencia hepática, incluidos resultados fatales, principalmente en pacientes con cirrosis e insuficiencia hepática moderada o grave de base (Child-Pugh B o C) tratados con regímenes que contienen inhibidores de la proteasa NS3/4A del VHC. Controle la evidencia clínica y de laboratorio de descompensación hepática. Suspenda ZEPATIER en pacientes que desarrollen evidencia de descompensación/insuficiencia hepática. (5.3)
- Riesgo asociado con el tratamiento combinado con ribavirina: Si ZEPATIER se administra con ribavirina, también se aplican las advertencias y precauciones para la ribavirina. (5.4)
REACCIONES ADVERSAS
En los sujetos que recibieron ZEPATIER durante 12 semanas, las reacciones adversas más comúnmente notificadas de todas las intensidades (mayores o iguales al 5% en los ensayos controlados con placebo) fueron fatiga, dolor de cabeza y náuseas. En los sujetos que recibieron ZEPATIER con ribavirina durante 16 semanas, las reacciones adversas más comúnmente notificadas de intensidad moderada o grave (mayores o iguales al 5%) fueron anemia y dolor de cabeza. (6.1)
Para notificar REACCIONES ADVERSAS SOSPECHOSAS, comuníquese con Merck Sharp & Dohme LLC al 1-877-888-4231 o con la FDA al 1-800-FDA-1088 o www.fda.gov/medwatch .
INTERACCIONES MEDICAMENTOSAS
- No se recomienda la coadministración de ZEPATIER con inductores moderados del CYP3A, ya que pueden disminuir la concentración plasmática de ZEPATIER. (7)
- No se recomienda la coadministración de ZEPATIER con ciertos inhibidores fuertes del CYP3A, ya que pueden aumentar la concentración plasmática de ZEPATIER. (7)
- La eliminación de la infección por VHC con antivirales de acción directa puede provocar cambios en la función hepática, lo que puede afectar el uso seguro y eficaz de los medicamentos concomitantes. Puede ser necesario un control frecuente de los parámetros de laboratorio relevantes (INR o glucosa en sangre) y ajustes de la dosis de ciertos medicamentos concomitantes. (7.2)
- Consulte la información completa de prescripción antes y durante el tratamiento para posibles interacciones medicamentosas. (4, 5.5, 7, 12.3)
Ver 17 para INFORMACIÓN DE ASESORAMIENTO AL PACIENTE y etiquetado del paciente aprobado por la FDA.
Revisado: 5/2022
Tabla de Contenido
INFORMACIÓN COMPLETA DE PRESCRIPCIÓN: CONTENIDO*
ADVERTENCIA: RIESGO DE REACTIVACIÓN DEL VIRUS DE LA HEPATITIS B EN PACIENTES COINFECTADOS CON VHC Y VHB
1 INDICACIONES Y USO
2 DOSIFICACIÓN Y ADMINISTRACIÓN
2.1 Pruebas previas al inicio de la terapia
2.2 Dosis recomendada en pacientes adultos y pediátricos de 12 años de edad o mayores o que pesen al menos 30 kg
2.3 Insuficiencia renal
2.4 Insuficiencia hepática
3 FORMAS Y FUERZAS DE DOSIFICACIÓN
4 CONTRAINDICACIONES
5 ADVERTENCIAS Y PRECAUCIONES
5.1 Riesgo de reactivación del virus de la hepatitis B en pacientes coinfectados con VHC y VHB
5.2 Aumento del riesgo de elevaciones de ALT
5.3 Riesgo de descompensación/insuficiencia hepática en pacientes con evidencia de enfermedad hepática avanzada
5.4 Riesgos asociados con el tratamiento de combinación con ribavirina
5.5 Riesgo de reacciones adversas o reducción del efecto terapéutico debido a interacciones medicamentosas
6 REACCIONES ADVERSAS
6.1 Experiencia en ensayos clínicos
6.2 Experiencia postcomercialización
7 INTERACCIONES MEDICAMENTOSAS
7.1 Potencial de interacciones medicamentosas
7.2 Interacciones medicamentosas establecidas y otras potencialmente significativas
7.3 Medicamentos sin interacciones clínicamente significativas con ZEPATIER
8 USO EN POBLACIONES ESPECÍFICAS
8.1 Embarazo
8.2 Lactancia
8.3 Mujeres y hombres en edad fértil
8.4 Uso pediátrico
8.5 Uso geriátrico
8.6 Género
8.7 Raza
8.8 Insuficiencia renal
8.9 Insuficiencia hepática
10 SOBREDOSIS
11 DESCRIPCIÓN
12 FARMACOLOGÍA CLÍNICA
12.1 Mecanismo de acción
12.2 Farmacodinamia
12.3 Farmacocinética
12.4 Microbiología
13 TOXICOLOGÍA NO CLÍNICA
13.1 Carcinogénesis, mutagénesis, deterioro de la fertilidad
14 ESTUDIOS CLÍNICOS
14.1 Descripción general de los ensayos clínicos
14.2 Ensayos clínicos en sujetos sin tratamiento previo con genotipo 1 VHC (C-EDGE TN y C-EDGE COINFECTION)
14.3 Ensayos clínicos en sujetos con experiencia en tratamiento con genotipo 1 VHC
14.4 Ensayo clínico en sujetos con genotipo 1 VHC e insuficiencia renal grave, incluidos sujetos en hemodiálisis (C-SURFER)
14.5 Ensayos clínicos con genotipo 4 VHC
14.6 Ensayo clínico en sujetos pediátricos con infección crónica por hepatitis C de genotipo 1 o 4
16 CÓMO SE SUMINISTRA/ALMACENAMIENTO Y MANEJO
17 INFORMACIÓN PARA EL PACIENTE
- *
- Las secciones o subsecciones omitidas de la información completa de prescripción no están enumeradas.
ADVERTENCIA EN EL RECUADRO
ADVERTENCIA: RIESGO DE REACTIVACIÓN DEL VIRUS DE LA HEPATITIS B EN PACIENTES COINFECTADOS CON VHC Y VHB
Analice a todos los pacientes para detectar evidencia de infección actual o previa por el virus de la hepatitis B (VHB) antes de iniciar el tratamiento con ZEPATIER. Se ha informado reactivación del VHB en pacientes coinfectados con VHC/VHB que estaban recibiendo o habían completado el tratamiento con antivirales de acción directa contra el VHC y no estaban recibiendo terapia antiviral contra el VHB. Algunos casos han provocado hepatitis fulminante, insuficiencia hepática y muerte. Monitoree a los pacientes coinfectados con VHC/VHB para detectar brotes de hepatitis o reactivación del VHB durante el tratamiento del VHC y el seguimiento posterior al tratamiento. Inicie la gestión adecuada del paciente para la infección por VHB según lo indicado clínicamente [ver Advertencias y precauciones (5.1)].
1 INDICACIONES Y USO
ZEPATIER® está indicado para el tratamiento de la infección por el virus de la hepatitis C crónica (VHC) de genotipo 1 o 4 en pacientes adultos y pediátricos de 12 años de edad o mayores o que pesen al menos 30 kg.
ZEPATIER está indicado para su uso con ribavirina en ciertas poblaciones de pacientes [ver Dosificación y administración (2.2)].
2 DOSIS Y ADMINISTRACIÓN
2.1 Pruebas previas al inicio de la terapia
Pruebas para infección por VHB
Realice pruebas a todos los pacientes para detectar evidencia de infección por VHB actual o previa midiendo el antígeno de superficie de la hepatitis B (HBsAg) y el anticuerpo contra el núcleo de la hepatitis B (anti-HBc) antes de iniciar el tratamiento con HCV con ZEPATIER [ver Advertencias y precauciones (5.1)].
Pruebas de resistencia a NS5A en pacientes infectados con genotipo 1a de VHC
Se recomienda realizar pruebas a los pacientes con infección por genotipo 1a de VHC para detectar la presencia de virus con polimorfismos asociados a resistencia a NS5A antes de iniciar el tratamiento con ZEPATIER para determinar el régimen de dosificación y la duración [ver Dosificación y administración (2.2), Tabla 1]. En los sujetos que recibieron ZEPATIER durante 12 semanas, las tasas de respuesta virológica sostenida (SVR12) fueron más bajas en los pacientes infectados con genotipo 1a con uno o más polimorfismos asociados a resistencia a NS5A en las posiciones de aminoácidos 28, 30, 31 o 93 [ver Microbiología (12.4), Tabla 12].
Pruebas de laboratorio hepáticas
Obtenga pruebas de laboratorio hepáticas antes y durante el tratamiento con ZEPATIER [ver Advertencias y precauciones (5.2, 5.3)].
2.2 Dosificación recomendada en pacientes adultos y pediátricos de 12 años de edad o mayores o que pesen al menos 30 kg
ZEPATIER es un producto de combinación de dosis fija de dos fármacos que contiene 50 mg de elbasvir y 100 mg de grazoprevir en un solo comprimido. La dosis recomendada de ZEPATIER es un comprimido administrado por vía oral una vez al día con o sin alimentos [ver Farmacología clínica (12.3)]. ZEPATIER se utiliza en combinación con ribavirina en ciertas poblaciones de pacientes (ver Tabla 1). Cuando se administra con ZEPATIER, la dosis recomendada de ribavirina en pacientes sin insuficiencia renal es basada en el peso administrada en dos dosis divididas con alimentos. Para obtener más información sobre la dosificación de ribavirina y las modificaciones de la dosis, consulte la información de prescripción de ribavirina.
Régimen de tratamiento y duración de la terapia
Las tasas de recaída se ven afectadas por los factores del huésped y virales de referencia y difieren entre los regímenes de tratamiento y las duraciones para ciertos subgrupos [ver Estudios clínicos (14)].
Tabla 1 a continuación proporciona el régimen de tratamiento recomendado con ZEPATIER y la duración basada en la población de pacientes y el genotipo en pacientes con infección mono-VHC y coinfectados con VHC/VIH-1 con o sin cirrosis y con o sin insuficiencia renal, incluidos los pacientes que reciben hemodiálisis.
| Población de pacientes | Tratamiento | Duración |
|---|---|---|
|
||
| Genotipo 1a: Tratamiento-naïve o con experiencia en PegIFN/RBV* sin polimorfismos de NS5A de referencia† | ZEPATIER | 12 semanas |
| Genotipo 1a: Tratamiento naive o con experiencia en PegIFN/RBV* con polimorfismos NS5A basales† | ZEPATIER + RBV‡ | 16 semanas |
| Genotipo 1b: Tratamiento naive o con experiencia en PegIFN/RBV* | ZEPATIER | 12 semanas |
| Genotipo 1a§ o 1b: Con experiencia en PegIFN/RBV/PI¶ | ZEPATIER + RBV‡ | 12 semanas |
| Genotipo 4: Tratamiento naive | ZEPATIER | 12 semanas |
| Genotipo 4: Con experiencia en PegIFN/RBV* | ZEPATIER + RBV‡ | 16 semanas |
2.3 Insuficiencia renal
No se recomienda ajustar la dosis de ZEPATIER en pacientes con cualquier grado de insuficiencia renal, incluidos los pacientes en hemodiálisis. Administrar ZEPATIER con o sin ribavirina de acuerdo con las recomendaciones de Tabla 1 [ver Uso en poblaciones específicas (8.8) y Estudios clínicos (14.4)]. Consulte la información de prescripción de la tableta de ribavirina para obtener la dosis correcta de ribavirina para pacientes con CrCl menor o igual a 50 mL por minuto.
2.4 Insuficiencia hepática
No se recomienda ajustar la dosis de ZEPATIER en pacientes con insuficiencia hepática leve (Child-Pugh A). ZEPATIER está contraindicado en pacientes con insuficiencia hepática moderada o grave (Child-Pugh B o C) o aquellos con antecedentes de descompensación hepática previa [ver Contraindicaciones (4), Advertencias y precauciones (5.3), Uso en poblaciones específicas (8.9), y Farmacología clínica (12.3)].
3 FORMAS DE DOSIFICACIÓN Y CONCENTRACIONES
ZEPATIER está disponible en forma de comprimidos recubiertos con película de color beige, ovalados, grabados con “770” en una cara y lisos en la otra. Cada comprimido contiene 50 mg de elbasvir y 100 mg de grazoprevir.
4 CONTRAINDICACIONES
- ZEPATIER está contraindicado en pacientes con insuficiencia hepática moderada o grave (Child-Pugh B o C) debido a la concentración plasmática de grazoprevir significativamente aumentada que se espera y al mayor riesgo de elevaciones de la alanina aminotransferasa (ALT) [ver Advertencias y precauciones (5.2), Uso en poblaciones específicas (8.9), y Farmacología clínica (12.3)].
- ZEPATIER está contraindicado en pacientes con insuficiencia hepática moderada o grave (Child-Pugh B o C) o en aquellos con antecedentes de descompensación hepática debido al riesgo de descompensación hepática [ver Advertencias y precauciones (5.3), Uso en poblaciones específicas (8.9)].
- ZEPATIER está contraindicado con inhibidores de los polipéptidos transportadores de aniones orgánicos 1B1/3 (OATP1B1/3) que se sabe o se espera que aumenten significativamente las concentraciones plasmáticas de grazoprevir, inductores fuertes del citocromo P450 3A (CYP3A) y efavirenz [ver Advertencias y precauciones (5.5), Interacciones medicamentosas (7), y Farmacología clínica (12.3)].
- Si ZEPATIER se administra con ribavirina, las contraindicaciones para ribavirina también se aplican a este régimen de combinación. Consulte la información de prescripción de ribavirina para obtener una lista de contraindicaciones para ribavirina.
Tabla 2 enumera los medicamentos que están contraindicados con ZEPATIER.
| Clase de medicamento | Medicamento(s) dentro de la clase que están contraindicados | Comentario clínico* |
|---|---|---|
|
||
| Anticonvulsivos | Fenitoína Carbamazepina |
Puede provocar la pérdida de la respuesta virológica a ZEPATIER debido a disminuciones significativas en las concentraciones plasmáticas de elbasvir y grazoprevir causadas por la inducción fuerte de CYP3A. |
| Antimiobacterianos | Rifampicina | Puede provocar la pérdida de la respuesta virológica a ZEPATIER debido a disminuciones significativas en las concentraciones plasmáticas de elbasvir y grazoprevir causadas por la inducción fuerte de CYP3A. |
| Productos herbales | Hierba de San Juan (Hypericum perforatum) | Puede provocar la pérdida de la respuesta virológica a ZEPATIER debido a disminuciones significativas en las concentraciones plasmáticas de elbasvir y grazoprevir causadas por la inducción fuerte de CYP3A. |
| Medicamentos para el VIH | Efavirenz† | Puede provocar la pérdida de la respuesta virológica a ZEPATIER debido a disminuciones significativas en las concentraciones plasmáticas de elbasvir y grazoprevir causadas por la inducción de CYP3A. |
| Medicamentos para el VIH | Atazanavir Darunavir Lopinavir Saquinavir Tipranavir |
Puede aumentar el riesgo de elevaciones de ALT debido a un aumento significativo en las concentraciones plasmáticas de grazoprevir causadas por la inhibición de OATP1B1/3. |
| Inmunosupresores | Ciclosporina | Puede aumentar el riesgo de elevaciones de ALT debido a un aumento significativo en las concentraciones plasmáticas de grazoprevir causadas por la inhibición de OATP1B1/3. |
5 ADVERTENCIAS Y PRECAUCIONES
5.1 Riesgo de reactivación del virus de la hepatitis B en pacientes coinfectados con VHC y VHB
Se ha notificado la reactivación del virus de la hepatitis B (VHB) en pacientes coinfectados con VHC/VHB que estaban en tratamiento o habían completado el tratamiento con antivirales de acción directa contra el VHC y que no estaban recibiendo tratamiento antiviral contra el VHB. Algunos casos han resultado en hepatitis fulminante, insuficiencia hepática y muerte. Se han notificado casos en pacientes que son HBsAg positivos y también en pacientes con evidencia serológica de infección por VHB resuelta (es decir, HBsAg negativo y anti-HBc positivo). También se ha notificado la reactivación del VHB en pacientes que reciben ciertos agentes inmunosupresores o quimioterapéuticos; el riesgo de reactivación del VHB asociado con el tratamiento con antivirales de acción directa contra el VHC puede aumentar en estos pacientes.
La reactivación del VHB se caracteriza como un aumento repentino de la replicación del VHB que se manifiesta como un aumento rápido del nivel de ADN del VHB en el suero. En pacientes con infección por VHB resuelta puede ocurrir la reaparición del HBsAg. La reactivación de la replicación del VHB puede ir acompañada de hepatitis, es decir, aumentos en los niveles de aminotransferasas y, en casos graves, aumentos en los niveles de bilirrubina, insuficiencia hepática y muerte.
Pruebe a todos los pacientes en busca de evidencia de infección actual o previa por VHB midiendo el HBsAg y el anti-HBc antes de iniciar el tratamiento del VHC con ZEPATIER. En pacientes con evidencia serológica de infección por VHB, controle las señales clínicas y de laboratorio de brote de hepatitis o reactivación del VHB durante el tratamiento del VHC con ZEPATIER y durante el seguimiento posterior al tratamiento. Inicie el manejo apropiado del paciente para la infección por VHB según se indique clínicamente.
5.2 Mayor riesgo de elevaciones de ALT
Durante los ensayos clínicos con ZEPATIER con o sin ribavirina, el 1% de los sujetos experimentó elevaciones de ALT desde niveles normales a más de 5 veces el límite superior de lo normal (ULN), generalmente en o después de la semana 8 de tratamiento. Las elevaciones de ALT fueron típicamente asintomáticas y la mayoría se resolvieron con la continuación o finalización de la terapia. Las tasas más altas de elevaciones de ALT tardías se produjeron en las siguientes subpoblaciones: sexo femenino (2% [10/608]), raza asiática (2% [4/164]) y edad de 65 años o más (2% [3/177]) [véase Reacciones adversas (6.1)].
Se debe realizar pruebas de laboratorio hepáticas antes del tratamiento, en la semana 8 de tratamiento y según se indique clínicamente. Para pacientes que reciben 16 semanas de tratamiento, se deben realizar pruebas de laboratorio hepáticas adicionales en la semana 12 de tratamiento.
- Los pacientes deben ser instruidos para consultar a su profesional de la salud sin demora si tienen inicio de fatiga, debilidad, falta de apetito, náuseas y vómitos, ictericia o heces descoloridas.
- Considere la interrupción de ZEPATIER si los niveles de ALT permanecen persistentemente mayores que 10 veces el ULN.
- Interrumpa ZEPATIER si la elevación de ALT va acompañada de señales o síntomas de inflamación hepática o aumento de la bilirrubina conjugada, fosfatasa alcalina o Ratio Internacional Normalizado (INR).
5.3 Riesgo de descompensación/fallo hepático en pacientes con evidencia de enfermedad hepática avanzada
Se han notificado casos postcomercialización de descompensación/fallo hepático, incluidos aquellos con resultados fatales, en pacientes tratados con regímenes que contienen inhibidores de la proteasa NS3/4A del VHC, incluyendo ZEPATIER.
Los casos notificados ocurrieron en pacientes tratados con regímenes que contienen inhibidores de la proteasa NS3/4A del VHC con cirrosis basal con y sin deterioro hepático moderado o grave (Child-Pugh B o C), así como en algunos pacientes sin cirrosis. Debido a que estos eventos se notifican voluntariamente desde una población de tamaño incierto, no siempre es posible estimar de manera fiable su frecuencia o establecer una relación causal con la exposición al fármaco.
Se deben realizar pruebas de laboratorio hepáticas en todos los pacientes [véase Advertencias y Precauciones (5.2)]. En pacientes con cirrosis compensada (Child-Pugh A) o evidencia de enfermedad hepática avanzada, como hipertensión portal, puede ser necesario realizar pruebas de laboratorio hepáticas más frecuentes; y se debe vigilar a los pacientes en busca de señales y síntomas de descompensación hepática, como la presencia de ictericia, ascitis, encefalopatía hepática y hemorragia varicosa. Interrumpa ZEPATIER en pacientes que desarrollen evidencia de descompensación/fallo hepático.
ZEPATIER está contraindicado en pacientes con deterioro hepático moderado a grave (Child-Pugh B o C) o aquellos con cualquier historia de descompensación hepática previa [véase Contraindicaciones (4), Reacciones adversas (6.1), Uso en poblaciones específicas (8.9) y Farmacología clínica (12.3)].
5.4 Riesgos asociados con el tratamiento combinado con ribavirina
Si ZEPATIER se administra con ribavirina, las advertencias y precauciones para la ribavirina, incluyendo la advertencia de evitar el embarazo, también se aplican a este régimen combinado. Consulte la información de prescripción de la ribavirina para una lista completa de advertencias y precauciones para la ribavirina [véase Dosis y administración (2.2)].
5.5 Riesgo de reacciones adversas o efecto terapéutico reducido debido a interacciones farmacológicas
El uso concomitante de ZEPATIER y ciertos fármacos puede resultar en interacciones farmacológicas conocidas o potencialmente significativas, algunas de las cuales pueden conducir a:
- Posibles reacciones adversas clínicamente significativas debido a una mayor exposición a fármacos concomitantes o componentes de ZEPATIER.
- Disminución significativa de las concentraciones plasmáticas de elbasvir y grazoprevir, lo que puede llevar a un efecto terapéutico reducido de ZEPATIER y posible desarrollo de resistencia.
Consulte Tablas 2 y 6 para conocer las medidas para prevenir o gestionar estas interacciones farmacológicas conocidas o potencialmente significativas, incluidas las recomendaciones de dosificación [véase Contraindicaciones (4) y Interacciones farmacológicas (7.2)].
6 REACCIONES ADVERSAS
La siguiente reacción adversa se describe a continuación y en otras partes del etiquetado:
- Aumento del riesgo de elevaciones de ALT [ver Advertencias y precauciones (5.2)].
6.1 Experiencia en ensayos clínicos
Debido a que los ensayos clínicos se llevan a cabo en condiciones muy variables, las tasas de reacciones adversas observadas en los ensayos clínicos de un fármaco no se pueden comparar directamente con las tasas en los ensayos clínicos de otro fármaco y pueden no reflejar las tasas observadas en la práctica.
Si ZEPATIER se administra con ribavirina, consulte la información de prescripción de ribavirina para obtener una descripción de las reacciones adversas asociadas a ribavirina.
Ensayos clínicos en sujetos adultos
La seguridad de ZEPATIER en sujetos adultos se evaluó en base a 2 ensayos controlados con placebo y 7 ensayos clínicos de fase 2 y 3 no controlados en aproximadamente 1700 sujetos con infección por el virus de la hepatitis C crónica con enfermedad hepática compensada (con o sin cirrosis) [ver Estudios clínicos (14)].
Reacciones adversas con ZEPATIER en sujetos sin tratamiento previo
C-EDGE TN fue un ensayo de fase 3 aleatorizado, doble ciego, controlado con placebo en 421 sujetos sin tratamiento previo (TN) con infección por VHC que recibieron ZEPATIER o placebo una tableta una vez al día durante 12 semanas. Las reacciones adversas (de todas las intensidades) que ocurrieron en C-EDGE TN en al menos el 5% de los sujetos tratados con ZEPATIER durante 12 semanas se presentan en Tabla 3. En los sujetos tratados con ZEPATIER que informaron una reacción adversa, el 73% tuvo reacciones adversas de gravedad leve. El tipo y la gravedad de las reacciones adversas en los sujetos con cirrosis compensada fueron comparables a los observados en los sujetos sin cirrosis. Ningún sujeto tratado con ZEPATIER o placebo tuvo reacciones adversas graves. La proporción de sujetos tratados con ZEPATIER o placebo que suspendieron permanentemente el tratamiento debido a reacciones adversas fue del 1% en cada grupo.
| C-EDGE TN | ||
|---|---|---|
| ZEPATIER N=316 % 12 semanas |
Placebo N=105 % 12 semanas |
|
| Fatiga | 11% | 10% |
| Dolor de cabeza | 10% | 9% |
Reacciones adversas con ZEPATIER con o sin ribavirina en sujetos con experiencia en tratamiento
C-EDGE TE fue un ensayo clínico de fase 3, aleatorizado, abierto en sujetos con experiencia en tratamiento (TE). Las reacciones adversas de intensidad moderada o grave notificadas en C-EDGE TE en al menos el 2% de los sujetos tratados con ZEPATIER una tableta una vez al día durante 12 semanas o ZEPATIER una tableta una vez al día con ribavirina durante 16 semanas se presentan en Tabla 4. Ningún sujeto tratado con ZEPATIER sin ribavirina durante 12 semanas informó reacciones adversas graves o interrumpió el tratamiento debido a reacciones adversas. La proporción de sujetos tratados con ZEPATIER con ribavirina durante 16 semanas con reacciones adversas graves fue del 1%. La proporción de sujetos tratados con ZEPATIER con ribavirina durante 16 semanas que interrumpieron permanentemente el tratamiento debido a reacciones adversas fue del 3%. El tipo y la gravedad de las reacciones adversas en los sujetos con cirrosis fueron comparables a los observados en los sujetos sin cirrosis.
| C-EDGE TE | ||
|---|---|---|
| ZEPATIER N=105 % 12 semanas |
ZEPATIER + Ribavirina N=106 % 16 semanas |
|
| Anemia | 0% | 8% |
| Dolor de cabeza | 0% | 6% |
| Fatiga | 5% | 4% |
| Disnea | 0% | 4% |
| Erupción o prurito | 0% | 4% |
| Irritabilidad | 1% | 3% |
| Dolor abdominal | 2% | 2% |
| Depresión | 1% | 2% |
| Artralgia | 0% | 2% |
| Diarrea | 2% | 0% |
El tipo y la gravedad de las reacciones adversas con ZEPATIER con o sin ribavirina en 10 sujetos con experiencia en tratamiento con coinfección por VHC/VIH fueron comparables a los informados en sujetos sin coinfección por VIH. Se observó un aumento mediano en los recuentos de células T CD4+ de 32 células/mm3 al final de las 12 semanas de tratamiento con ZEPATIER solo. En los sujetos tratados con ZEPATIER con ribavirina durante 16 semanas, los recuentos de células T CD4+ disminuyeron una mediana de 135 células por mm3 al final del tratamiento. Ningún sujeto cambió su régimen de terapia antirretroviral debido a la pérdida de la supresión del ARN del VIH-1 en plasma. Ningún sujeto experimentó una infección oportunista relacionada con el SIDA.
C-SALVAGE fue un ensayo de fase 2 abierto en 79 sujetos con experiencia en PegIFN/RBV/PI. Las reacciones adversas de intensidad moderada o grave informadas en C-SALVAGE en al menos el 2% de los sujetos tratados con ZEPATIER una vez al día con ribavirina durante 12 semanas fueron fatiga (3%) e insomnio (3%). Ningún sujeto informó reacciones adversas graves o interrumpió el tratamiento debido a reacciones adversas.
Reacciones adversas con ZEPATIER en sujetos con insuficiencia renal grave, incluidos los sujetos en hemodiálisis
La seguridad de elbasvir y grazoprevir en comparación con placebo en sujetos con insuficiencia renal grave (enfermedad renal crónica en estadio 4 o estadio 5, incluidos los sujetos en hemodiálisis) e infección por el virus de la hepatitis C crónica con enfermedad hepática compensada (con o sin cirrosis) se evaluó en 235 sujetos (C-SURFER) [ver Estudios clínicos (14.4)]. Las reacciones adversas (de todas las intensidades) que ocurrieron en al menos el 5% de los sujetos tratados con ZEPATIER durante 12 semanas se presentan en Tabla 5. En los sujetos tratados con ZEPATIER que informaron una reacción adversa, el 76% tuvo reacciones adversas de gravedad leve. La proporción de sujetos tratados con ZEPATIER o placebo con reacciones adversas graves fue inferior al 1% en cada brazo de tratamiento, y menos del 1% y el 3% de los sujetos, respectivamente, interrumpieron permanentemente el tratamiento debido a reacciones adversas en cada brazo de tratamiento.
| ZEPATIER N=122 % 12 semanas |
Placebo N=113 % 12 semanas |
|
|---|---|---|
| Náuseas | 11% | 8% |
| Dolor de cabeza | 11% | 5% |
| Fatiga | 5% | 8% |
Anormalidades de laboratorio en sujetos que recibieron ZEPATIER con o sin ribavirina
Elevaciones de ALT en suero
Durante los ensayos clínicos con ZEPATIER con o sin ribavirina, independientemente de la duración del tratamiento, el 1% (12/1599) de los sujetos experimentaron elevaciones de ALT desde niveles normales a más de 5 veces el LSN, generalmente en o después de la semana 8 de tratamiento (tiempo medio de inicio 10 semanas, rango 6-12 semanas). Estas elevaciones tardías de ALT fueron típicamente asintomáticas. La mayoría de las elevaciones tardías de ALT se resolvieron con la terapia en curso con ZEPATIER o después de la finalización de la terapia [ver Advertencias y precauciones (5.2)]. La frecuencia de las elevaciones tardías de ALT fue mayor en los sujetos con concentraciones plasmáticas de grazoprevir más altas [ver Interacciones medicamentosas (7.1) y Farmacología clínica (12.3)]. La incidencia de elevaciones tardías de ALT no se vio afectada por la duración del tratamiento. La cirrosis no fue un factor de riesgo para las elevaciones tardías de ALT.
Elevaciones de bilirrubina en suero
Durante los ensayos clínicos con ZEPATIER con o sin ribavirina, independientemente de la duración del tratamiento, se observaron elevaciones de bilirrubina a más de 2,5 veces el LSN en el 6% de los sujetos que recibieron ZEPATIER con ribavirina en comparación con menos del 1% en los que recibieron ZEPATIER solo. Estos aumentos de bilirrubina fueron predominantemente indirectos y generalmente se observaron en asociación con la coadministración de ribavirina. Las elevaciones de bilirrubina no estuvieron típicamente asociadas con elevaciones de ALT en suero.
Hemoglobina disminuida
Durante los ensayos clínicos con ZEPATIER con o sin ribavirina, el cambio medio desde el inicio en los niveles de hemoglobina en los sujetos tratados con ZEPATIER durante 12 semanas fue de –0,3 g por dL y con ZEPATIER con ribavirina durante 16 semanas fue de aproximadamente –2,2 g por dL. La hemoglobina disminuyó durante las primeras 8 semanas de tratamiento, se mantuvo baja durante el resto del tratamiento y se normalizó a los niveles iniciales durante el seguimiento. Menos del 1% de los sujetos tratados con ZEPATIER con ribavirina tuvieron niveles de hemoglobina que disminuyeron a menos de 8,5 g por dL durante el tratamiento. Ningún sujeto tratado con ZEPATIER solo tuvo un nivel de hemoglobina inferior a 8,5 g por dL.
Ensayo clínico en sujetos pediátricos
Reacciones adversas en sujetos pediátricos de 12 años de edad o mayores
La seguridad de ZEPATIER se evaluó en sujetos pediátricos de 12 años de edad o mayores en base a datos de 22 sujetos, sin cirrosis, que fueron tratados con ZEPATIER durante 12 semanas en un ensayo clínico de fase 2b, abierto (MK-5172-079). Las reacciones adversas observadas fueron consistentes con las observadas en los ensayos clínicos de ZEPATIER en adultos [ver Estudios clínicos (14.6)]. Las reacciones adversas a los medicamentos observadas en más del 5% de los sujetos que recibieron ZEPATIER fueron dolor de cabeza (14%) y náuseas (9%).
6.2 Experiencia postcomercialización
Las siguientes reacciones adversas se han identificado durante el uso posterior a la aprobación de ZEPATIER. Debido a que estas reacciones se informan voluntariamente de una población de tamaño incierto, no siempre es posible estimar de manera confiable su frecuencia o establecer una relación causal con la exposición al fármaco.
Trastornos hepatobiliares
Descompensación hepática, insuficiencia hepática [ver Advertencias y precauciones (5.3)]
7 INTERACCIONES MEDICAMENTOSAS
7.1 Posibilidad de interacciones medicamentosas
Grazoprevir es un sustrato de los transportadores OATP1B1/3. La administración conjunta de ZEPATIER con inhibidores de OATP1B1/3 que se sabe o se espera que aumenten significativamente las concentraciones plasmáticas de grazoprevir está contraindicada [ver Contraindicaciones (4), Farmacología clínica (12.3), y Tabla 2].
Elbasvir y grazoprevir son sustratos de CYP3A y P-gp, pero el papel de la P-gp intestinal en la absorción de elbasvir y grazoprevir parece ser mínimo. La administración conjunta de inductores moderados o fuertes de CYP3A con ZEPATIER puede disminuir las concentraciones plasmáticas de elbasvir y grazoprevir, lo que lleva a una reducción del efecto terapéutico de ZEPATIER. La administración conjunta de ZEPATIER con inductores fuertes de CYP3A o efavirenz está contraindicada [ver Contraindicaciones (4), Farmacología clínica (12.3), y Tabla 2]. La administración conjunta de ZEPATIER con inductores moderados de CYP3A no se recomienda [ver Advertencias y precauciones (5.5), Farmacología clínica (12.3), y Tabla 6]. La administración conjunta de ZEPATIER con inhibidores fuertes de CYP3A puede aumentar las concentraciones de elbasvir y grazoprevir. La administración conjunta de ZEPATIER con ciertos inhibidores fuertes de CYP3A no se recomienda [ver Advertencias y precauciones (5.5), Farmacología clínica (12.3), y Tabla 6].
7.2 Interacciones medicamentosas establecidas y otras potencialmente significativas
Si se realizan ajustes de dosis de los medicamentos concomitantes debido al tratamiento con ZEPATIER, las dosis deben reajustarse después de que se complete la administración de ZEPATIER.
La eliminación de la infección por VHC con antivirales de acción directa puede provocar cambios en la función hepática, lo que puede afectar el uso seguro y eficaz de los medicamentos concomitantes. Por ejemplo, se ha informado de un control alterado de la glucosa en sangre que da como resultado hipoglucemia sintomática grave en pacientes diabéticos en informes de casos posteriores a la comercialización y estudios epidemiológicos publicados. El manejo de la hipoglucemia en estos casos requirió la interrupción o la modificación de la dosis de los medicamentos concomitantes utilizados para el tratamiento de la diabetes.
Se recomienda el control frecuente de los parámetros de laboratorio relevantes (por ejemplo, Índice Internacional Normalizado [INR] en pacientes que toman warfarina, niveles de glucosa en sangre en pacientes diabéticos) o las concentraciones de fármacos de los medicamentos concomitantes, como los sustratos de CYP450 con un índice terapéutico estrecho (por ejemplo, ciertos inmunosupresores) para garantizar un uso seguro y eficaz. Pueden ser necesarios ajustes de dosis de los medicamentos concomitantes.
Tabla 6 proporciona una lista de interacciones medicamentosas establecidas o potencialmente clínicamente significativas. Las interacciones medicamentosas descritas se basan en estudios realizados con ZEPATIER, los componentes de ZEPATIER (elbasvir [EBR] y grazoprevir [GZR]) como agentes individuales, o son interacciones medicamentosas predichas que pueden ocurrir con ZEPATIER [ver Contraindicaciones (4), Advertencias y precauciones (5.5), y Farmacología clínica (12.3)].
| Clase de fármaco concomitante: Nombre del fármaco | Efecto sobre la concentración† | Comentario clínico |
|---|---|---|
|
||
| Antibióticos: Nafcilina |
↓ EBR ↓ GZR |
La administración conjunta de ZEPATIER con nafcilina puede provocar una reducción del efecto terapéutico de ZEPATIER. No se recomienda la administración conjunta. |
| Antifúngicos: Ketoconazol oral‡ |
↑ EBR ↑ GZR |
No se recomienda la administración conjunta de ketoconazol oral. |
| Antagonistas de la endotelina: Bosentan |
↓ EBR ↓ GZR |
La administración conjunta de ZEPATIER con bosentan puede provocar una reducción del efecto terapéutico de ZEPATIER. No se recomienda la administración conjunta. |
| Inmunosupresores: Tacrolimus‡ |
↑ tacrolimus | Se recomienda el control frecuente de las concentraciones de tacrolimus en sangre total, los cambios en la función renal y los eventos adversos asociados al tacrolimus al inicio de la administración conjunta. |
| Medicamentos para el VIH: | ||
| Etravirina | ↓ EBR ↓ GZR |
La coadministración de ZEPATIER con etravirina puede conducir a una reducción del efecto terapéutico de ZEPATIER. No se recomienda la coadministración. |
| Elvitegravir/ cobicistat/ emtricitabina/ tenofovir (disoproxil fumarato‡ o alafenamida) | ↑ EBR ↑ GZR |
No se recomienda la coadministración de regímenes que contienen cobicistat. |
| Inhibidores de la HMG-CoA reductasa§: | ||
| Atorvastatina‡ | ↑ atorvastatina | La dosis de atorvastatina no debe exceder una dosis diaria de 20 mg cuando se administra conjuntamente con ZEPATIER.§ |
| Rosuvastatina‡ | ↑ rosuvastatina | La dosis de rosuvastatina no debe exceder una dosis diaria de 10 mg cuando se administra conjuntamente con ZEPATIER.§ |
| Fluvastatina Lovastatina Simvastatina |
↑ fluvastatina ↑ lovastatina ↑ simvastatina |
Los eventos adversos relacionados con las estatinas, como la miopatía, deben controlarse estrechamente. Se debe utilizar la dosis más baja necesaria cuando se administra conjuntamente con ZEPATIER.§ |
| Agentes que promueven la vigilia: Modafinilo |
↓ EBR ↓ GZR |
La coadministración de ZEPATIER con modafinilo puede conducir a una reducción del efecto terapéutico de ZEPATIER. No se recomienda la coadministración. |
7.3 Medicamentos sin interacciones clínicamente significativas con ZEPATIER
La interacción entre los componentes de ZEPATIER (elbasvir o grazoprevir) o ZEPATIER y los siguientes medicamentos se evaluó en estudios clínicos, y no se necesitan ajustes de dosis cuando ZEPATIER se usa con los siguientes medicamentos individualmente: agentes reductores del ácido (inhibidores de la bomba de protones, bloqueadores H2, antiácidos), buprenorfina/naloxona, digoxina, dolutegravir, metadona, micofenolato mofetil, píldoras anticonceptivas orales, fijadores de fosfato, pitavastatina, pravastatina, prednisona, raltegravir, ribavirina, rilpivirina, tenofovir disoproxil fumarato y sofosbuvir [ver Farmacología clínica (12.3)].
No se espera una interacción fármaco-fármaco clínicamente relevante cuando ZEPATIER se administra conjuntamente con abacavir, emtricitabina, entecavir y lamivudina.
8 USO EN POBLACIONES ESPECÍFICAS
8.1 Embarazo
Resumen de riesgos
No se dispone de datos adecuados en humanos para establecer si ZEPATIER supone o no un riesgo para los resultados del embarazo. En estudios de reproducción animal, no se observaron indicios de resultados adversos en el desarrollo con los componentes de ZEPATIER (elbasvir o grazoprevir) a exposiciones superiores a las de los humanos a la dosis humana recomendada (DHR) (ver Datos). Durante la organogénesis en ratas y conejos, las exposiciones sistémicas (AUC) fueron aproximadamente 10 y 18 veces (para elbasvir) y 117 y 41 veces (para grazoprevir), respectivamente, la exposición en humanos a la DHR. En estudios de desarrollo pre/postnatal en ratas, las exposiciones sistémicas maternas (AUC) a elbasvir y grazoprevir fueron aproximadamente 10 y 78 veces, respectivamente, la exposición en humanos a la DHR.
Se desconoce el riesgo de base de defectos congénitos importantes y abortos espontáneos para la población indicada. En la población general de EE. UU., el riesgo de base estimado de defectos congénitos importantes y abortos espontáneos en embarazos clínicamente reconocidos es del 2-4 % y del 15-20 %, respectivamente.
Si se administra ZEPATIER con ribavirina, la pauta combinada está contraindicada en mujeres embarazadas y en hombres cuyas parejas femeninas estén embarazadas. Consulte la información de prescripción de ribavirina para obtener más información sobre el uso durante el embarazo.
Datos
Datos en animales
Elbasvir: Se administró elbasvir por vía oral a dosis de hasta 1000 mg/kg/día a ratas y conejas preñadas en los días de gestación 6 a 20 y 7 a 20, respectivamente, y también a ratas en el día de gestación 6 al día 20 de lactancia/posparto. No se observaron efectos sobre el desarrollo embriofetal (ratas y conejos) ni pre/postnatal (ratas) hasta la dosis más alta probada. Las exposiciones sistémicas (AUC) a elbasvir fueron aproximadamente 10 (ratas) y 18 (conejos) veces la exposición en humanos a la DHR. En ambas especies, se ha demostrado que elbasvir atraviesa la placenta, con concentraciones plasmáticas fetales de hasta el 0,8 % (conejos) y el 2,2 % (ratas) de las concentraciones maternas observadas en el día 20 de gestación.
Grazoprevir: Se administró grazoprevir a ratas preñadas (dosis orales de hasta 400 mg/kg/día) y conejas (dosis intravenosas de hasta 100 mg/kg/día) en los días de gestación 6 a 20 y 7 a 20, respectivamente, y también a ratas (dosis orales de hasta 400 mg/kg/día) en el día de gestación 6 al día 20 de lactancia/posparto. No se observaron efectos sobre el desarrollo embriofetal (ratas y conejos) ni pre/postnatal (ratas) hasta la dosis más alta probada. Las exposiciones sistémicas (AUC) a grazoprevir fueron ≥78 (ratas) y 41 (conejos) veces la exposición en humanos a la DHR. En ambas especies, se ha demostrado que grazoprevir atraviesa la placenta, con concentraciones plasmáticas fetales de hasta el 7 % (conejos) y el 89 % (ratas) de las concentraciones maternas observadas en el día 20 de gestación.
8.2 Lactancia
Resumen de riesgos
Se desconoce si ZEPATIER está presente en la leche materna humana, afecta a la producción de leche materna o tiene efectos en el lactante. Cuando se administraron a ratas lactantes, los componentes de ZEPATIER (elbasvir y grazoprevir) estuvieron presentes en la leche, sin que se observaran efectos sobre el crecimiento y el desarrollo de las crías lactantes (ver Datos).
Deben tenerse en cuenta los beneficios del desarrollo y la salud de la lactancia materna, junto con la necesidad clínica de la madre de ZEPATIER y cualquier posible efecto adverso sobre el niño amamantado por ZEPATIER o por la condición materna subyacente.
Si se administra ZEPATIER con ribavirina, la información para la ribavirina con respecto a las madres lactantes también se aplica a esta pauta combinada. Consulte la información de prescripción de ribavirina para obtener información sobre el uso durante la lactancia.
Datos
Elbasvir: No se observaron efectos del elbasvir sobre el crecimiento y el desarrollo posnatal en las crías lactantes hasta la dosis más alta probada. La exposición sistémica materna (AUC) a elbasvir fue aproximadamente 10 veces la exposición en humanos a la DHR. El elbasvir se excretó en la leche de ratas lactantes tras la administración oral (1000 mg/kg/día) desde el día 6 de gestación hasta el día 14 de lactancia, con concentraciones en leche aproximadamente 4 veces superiores a las concentraciones plasmáticas maternas observadas 2 horas después de la dosis en el día 14 de lactancia.
Grazoprevir: No se observaron efectos del grazoprevir sobre el crecimiento y el desarrollo posnatal en las crías lactantes hasta la dosis más alta probada. La exposición sistémica materna (AUC) a grazoprevir fue aproximadamente 78 veces la exposición en humanos a la DHR. El grazoprevir se excretó en la leche de ratas lactantes tras la administración oral (hasta 400 mg/kg/día) desde el día 6 de gestación hasta el día 14 de lactancia, con concentraciones en leche del 54 y el 87 % de las concentraciones plasmáticas maternas observadas 2 y 8 horas después de la dosis, respectivamente, en el día 14 de lactancia.
8.3 Mujeres y hombres con potencial reproductivo
Si se administra ZEPATIER con ribavirina, la información para la ribavirina con respecto a las pruebas de embarazo, la anticoncepción y la infertilidad también se aplica a esta pauta combinada. Consulte la información de prescripción de ribavirina para obtener información adicional.
8.4 Uso pediátrico
La seguridad, eficacia y farmacocinética de ZEPATIER se evaluaron en un ensayo clínico abierto (MK-5172-079), que incluyó a 22 sujetos (n=21, genotipo 1; n=1, genotipo 4) de 12 años de edad y mayores que recibieron ZEPATIER durante 12 semanas. La seguridad, farmacocinética y eficacia observadas en este ensayo fueron comparables a las observadas en adultos [ver Dosificación y administración (2.2), Reacciones adversas (6.1), Farmacología clínica (12.3) y Estudios clínicos (14.6)].
No se ha establecido la seguridad y eficacia de ZEPATIER en pacientes pediátricos menores de 12 años de edad que pesan menos de 30 kg.
8.5 Uso geriátrico
Los ensayos clínicos de ZEPATIER con o sin ribavirina incluyeron a 187 sujetos de 65 años de edad y mayores. Se observaron concentraciones plasmáticas más altas de elbasvir y grazoprevir en sujetos de 65 años de edad y mayores. Se observó una mayor tasa de elevaciones tardías de ALT en sujetos de 65 años de edad y mayores en ensayos clínicos [ver Advertencias y precauciones (5.2)]. Sin embargo, no se recomienda ajustar la dosis de ZEPATIER en pacientes geriátricos [ver Farmacología clínica (12.3)].
8.6 Sexo
Se observaron concentraciones plasmáticas más altas de elbasvir y grazoprevir en mujeres en comparación con los hombres. Las mujeres experimentaron una mayor tasa de elevaciones tardías de ALT en ensayos clínicos [ver Advertencias y precauciones (5.2)]. Sin embargo, no se recomienda ajustar la dosis de ZEPATIER en función del sexo [ver Farmacología clínica (12.3)].
8.7 Raza
Se observaron concentraciones plasmáticas más altas de elbasvir y grazoprevir en asiáticos en comparación con los caucásicos. Los asiáticos experimentaron una mayor tasa de elevaciones tardías de ALT en ensayos clínicos [ver Advertencias y precauciones (5.2)]. Sin embargo, no se recomienda ajustar la dosis de ZEPATIER en función de la raza/etnia [ver Farmacología clínica (12.3)].
8.8 Insuficiencia renal
No se recomienda ajustar la dosis de ZEPATIER en pacientes con cualquier grado de insuficiencia renal, incluidos los pacientes que reciben hemodiálisis [ver Farmacología clínica (12.3)]. Administre ZEPATIER con o sin ribavirina de acuerdo con las recomendaciones de la Tabla 1 [ver Dosificación y administración (2.2, 2.3)]. Consulte la información de prescripción de las tabletas de ribavirina para conocer el ajuste de la dosis renal de ribavirina en pacientes con CrCl inferior o igual a 50 ml por minuto.
8.9 Insuficiencia hepática
No se recomienda ajustar la dosis de ZEPATIER en pacientes con insuficiencia hepática leve (Child-Pugh A). ZEPATIER está contraindicado en pacientes con insuficiencia hepática moderada (Child-Pugh B) debido a la falta de experiencia clínica sobre seguridad y eficacia en pacientes con infección por VHC Child-Pugh B, y en pacientes con insuficiencia hepática grave (Child-Pugh C) debido a un aumento de 12 veces en la exposición a grazoprevir en sujetos Child-Pugh C no infectados por VHC. Además, se han notificado casos poscomercialización de descompensación/insuficiencia hepática en pacientes con enfermedad hepática avanzada [ver Dosificación y administración (2.4), Contraindicaciones (4), Advertencias y precauciones (5.3) y Farmacología clínica (12.3)].
No se ha establecido la seguridad y eficacia de ZEPATIER en pacientes en espera de trasplante de hígado o en receptores de trasplante de hígado.
10 SOBREDOSIS
La experiencia humana de sobredosis con ZEPATIER es limitada. No hay antídoto específico disponible para la sobredosis con ZEPATIER. En caso de sobredosis, se recomienda que el paciente sea monitoreado por cualquier signo o síntoma de reacciones adversas y se instituya el tratamiento sintomático apropiado.
La hemodiálisis no elimina elbasvir o grazoprevir ya que elbasvir y grazoprevir están altamente unidos a la proteína plasmática [ver Farmacología clínica (12.3)].
11 DESCRIPCIÓN
ZEPATIER es una tableta de combinación de dosis fija que contiene elbasvir y grazoprevir para administración oral.
Elbasvir es un inhibidor de NS5A de HCV, y grazoprevir es un inhibidor de la proteasa NS3/4A de HCV.
Cada tableta contiene 50 mg de elbasvir y 100 mg de grazoprevir. Las tabletas incluyen los siguientes ingredientes inactivos: dióxido de silicio coloidal, copovidona, croscarmelosa sódica, hipromelosa, lactosa monohidrato, estearato de magnesio, manitol, celulosa microcristalina, cloruro de sodio, lauril sulfato de sodio y succinato de polietilenglicol de vitamina E. Las tabletas están recubiertas con un material de recubrimiento que contiene los siguientes ingredientes inactivos: cera de carnauba, óxido ferroso férrico, hipromelosa, óxido de hierro rojo, óxido de hierro amarillo, lactosa monohidrato, dióxido de titanio y triacetina.
Elbasvir:
El nombre IUPAC para elbasvir es Dimetil N,N’-([(6S)-6-fenilindolo[1,2-c][1,3]benzoxazina-3,10-diyl]bis{1H-imidazol-5,2-diyl-(2S)-pirrolidina-2,1-diyl[(2S)-3-metil-1-oxobutano-1,2-diyl]})dicarbamato.
Tiene una fórmula molecular de C49H55N9O7 y un peso molecular de 882.02. Tiene la siguiente fórmula estructural:
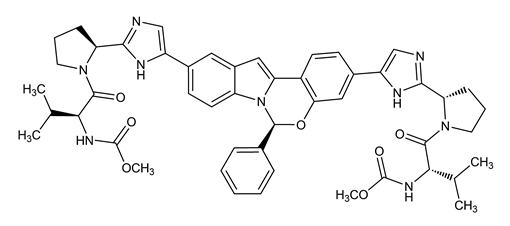
Elbasvir es prácticamente insoluble en agua (menos de 0,1 mg por mL) y muy poco soluble en etanol (0,2 mg por mL), pero es muy soluble en acetato de etilo y acetona.
Grazoprevir:
El nombre IUPAC para grazoprevir es (1aR,5S,8S,10R,22aR)-N-[(1R,2S)-1-[(Ciclopropilsulfonamido)carbonil]-2-etenilciclopropil]-14-metoxi-5-(2-metilpropan-2-il)-3,6-dioxo-1,1a,3,4,5,6,9,10,18,19,20,21,22,22a-tetradecahidro-8H-7,10-metanociclopropa[18,19][1,10,3,6]dioxadiazaciclononadecino[11,12-b]quinoxalina-8-carboxamida.
Tiene una fórmula molecular de C38H50N6O9S y un peso molecular de 766.90. Tiene la siguiente fórmula estructural:
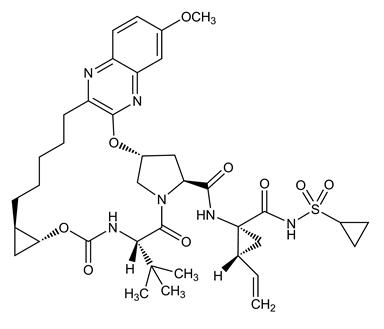
Grazoprevir es prácticamente insoluble en agua (menos de 0,1 mg por mL) pero es libremente soluble en etanol y algunos solventes orgánicos (por ejemplo, acetona, tetrahidrofurano y N,N-dimetilformamida).
12 FARMACOLOGÍA CLÍNICA
12.1 Mecanismo de acción
ZEPATIER es una combinación de dosis fija de elbasvir y grazoprevir, que son agentes antivirales de acción directa contra el virus de la hepatitis C [ver Microbiología (12.4)].
12.2 Farmacodinamia
Electrofisiología cardíaca
Se han realizado estudios exhaustivos de QT para elbasvir y grazoprevir.
El efecto de elbasvir 700 mg en el intervalo QTc se evaluó en un ensayo exhaustivo de QT de 3 períodos de cruce aleatorizado, de dosis única, controlado con placebo y activo (moxifloxacino 400 mg) en 42 sujetos sanos. A una concentración de 3 a 4 veces la concentración terapéutica, elbasvir no prolonga el QTc en ningún grado clínicamente relevante.
El efecto de grazoprevir 1600 mg (16 veces la dosis aprobada) en el intervalo QTc se evaluó en un ensayo exhaustivo de QT de 3 períodos de cruce aleatorizado, de dosis única, controlado con placebo y activo (moxifloxacino 400 mg) en 41 sujetos sanos. A una concentración 40 veces la concentración terapéutica, grazoprevir no prolonga el QTc en ningún grado clínicamente relevante.
12.3 Farmacocinética
Las propiedades farmacocinéticas de elbasvir y grazoprevir se han evaluado en sujetos adultos no infectados por el VHC y en sujetos adultos infectados por el VHC. La farmacocinética de elbasvir fue similar en sujetos sanos y en sujetos infectados por el VHC y fue aproximadamente proporcional a la dosis en el rango de 5-100 mg una vez al día. Las exposiciones orales de grazoprevir son aproximadamente 2 veces mayores en sujetos infectados por el VHC en comparación con los sujetos sanos. La farmacocinética de grazoprevir aumentó de manera mayor que proporcional a la dosis en el rango de 10-800 mg una vez al día en sujetos infectados por el VHC. La coadministración de ribavirina con ZEPATIER no tuvo un impacto clínicamente relevante en el AUC plasmático y la Cmax de elbasvir y grazoprevir en comparación con la administración de ZEPATIER solo. Los valores medios geométricos de los parámetros farmacocinéticos en estado estacionario para elbasvir y grazoprevir en sujetos infectados por el VHC no cirróticos se proporcionan en Tabla 7. Después de la administración una vez al día de ZEPATIER a sujetos infectados por el VHC, elbasvir y grazoprevir alcanzaron el estado estacionario en aproximadamente 6 días.
| Media geométrica (intervalo de confianza del 90%) | |||
|---|---|---|---|
| AUC0-24 (ng•hr/mL) | Cmax (ng/mL) | C24 (ng/mL) | |
| Elbasvir | 1920 (1880, 1960) | 121 (118, 123) | 48.4 (47.3, 49.6) |
| Grazoprevir | 1420 (1400, 1530) | 165 (161, 176) | 18.0 (17.8, 19.9) |
Absorción
Tras la administración de ZEPATIER a sujetos infectados por VHC, las concentraciones máximas de elbasvir se producen a una Tmax mediana de 3 horas (rango de 3 a 6 horas); las concentraciones máximas de grazoprevir se producen a una Tmax mediana de 2 horas (rango de 30 minutos a 3 horas). La biodisponibilidad absoluta de elbasvir se estima en un 32%, y la de grazoprevir se estima en un 27%.
Efecto de los alimentos
En relación con las condiciones de ayuno, la administración de una dosis única de ZEPATIER con una comida rica en grasas (900 kcal, 500 kcal de grasa) a sujetos sanos dio como resultado disminuciones en el AUC0-inf y la Cmax de elbasvir de aproximadamente un 11% y un 15%, respectivamente, y aumentos en el AUC0-inf y la Cmax de grazoprevir de aproximadamente 1,5 veces y 2,8 veces, respectivamente. Estas diferencias en la exposición a elbasvir y grazoprevir no son clínicamente relevantes; por lo tanto, ZEPATIER puede tomarse con independencia de las comidas [ver Posología y forma de administración (2.2)].
Distribución
Elbasvir y grazoprevir se unen ampliamente (más del 99,9% y el 98,8%, respectivamente) a las proteínas plasmáticas humanas. Tanto elbasvir como grazoprevir se unen a la albúmina sérica humana y a la α1-glicoproteína ácida. Los valores estimados del volumen de distribución aparente de elbasvir y grazoprevir son de aproximadamente 680 L y 1250 L, respectivamente, según el modelado farmacocinético poblacional.
En estudios preclínicos de distribución, elbasvir se distribuye a la mayoría de los tejidos, incluido el hígado; mientras que grazoprevir se distribuye principalmente al hígado, probablemente facilitado por el transporte activo a través del transportador de captación hepática OATP1B1/3.
Eliminación
La media geométrica de la semivida terminal aparente para elbasvir (50 mg) y grazoprevir (100 mg) es de aproximadamente 24 y 31 horas, respectivamente, en sujetos infectados por VHC.
Poblaciones específicas
Población pediátrica
La farmacocinética de elbasvir y grazoprevir se evaluó en 22 sujetos pediátricos de 12 años de edad o mayores, con genotipo 1 o 4 del VHC, que recibieron una dosis diaria de ZEPATIER (50 mg de elbasvir/100 mg de grazoprevir). Las propiedades farmacocinéticas de elbasvir y grazoprevir en sujetos pediátricos de 12 años de edad o mayores se proporcionan en la Tabla 8. Las exposiciones en sujetos pediátricos fueron comparables a las observadas en adultos.
| Parámetros de FC* | Media geométrica (intervalo de confianza del 90%) | ||
|---|---|---|---|
| AUC0-24 (ng•hr/mL) | Cmax (ng/mL) | C24 (ng/mL) | |
|
|||
| Elbasvir | 2120 (1800, 2510) | 167 (140, 199) | 50.3 (41.7, 60.6) |
| Grazoprevir | 1110 (871, 1410) | 188 (140, 253) | 11.7 (9.43, 14.5) |
Población geriátrica
En análisis farmacocinéticos poblacionales, se estima que las AUC de elbasvir y grazoprevir son, respectivamente, un 16% y un 45% más altas en sujetos de al menos 65 años de edad en comparación con sujetos menores de 65 años de edad.
Género
En análisis farmacocinéticos poblacionales, se estima que las AUC de elbasvir y grazoprevir son, respectivamente, un 50% y un 30% más altas en mujeres en comparación con hombres.
Peso/IMC
En análisis farmacocinéticos poblacionales, no hubo efecto del peso en la farmacocinética de elbasvir. Se estima que la AUC de grazoprevir es un 15% más alta en un sujeto de 53 kg en comparación con un sujeto de 77 kg. Este cambio no es clínicamente relevante para grazoprevir.
Raza/Etnia
En análisis farmacocinéticos poblacionales, se estima que las AUC de elbasvir y grazoprevir son, respectivamente, un 15% y un 50% más altas en asiáticos en comparación con caucásicos. Las estimaciones farmacocinéticas poblacionales de la exposición de elbasvir y grazoprevir fueron comparables entre caucásicos y negros/afroamericanos.
Insuficiencia renal
En análisis farmacocinéticos poblacionales, la AUC de elbasvir fue un 25% más alta en sujetos dependientes de hemodiálisis y un 46% más alta en sujetos no dependientes de hemodiálisis con insuficiencia renal grave en comparación con la AUC de elbasvir en sujetos sin insuficiencia renal grave. En el análisis farmacocinético poblacional en sujetos infectados con VHC, la AUC de grazoprevir fue un 10% más alta en sujetos dependientes de hemodiálisis y un 40% más alta en sujetos no dependientes de hemodiálisis con insuficiencia renal grave en comparación con la AUC de grazoprevir en sujetos sin insuficiencia renal grave. Elbasvir y grazoprevir no se eliminan por hemodiálisis. Es poco probable que elbasvir y grazoprevir se eliminen por diálisis peritoneal, ya que ambos están altamente unidos a proteínas.
En general, los cambios en la exposición de elbasvir y grazoprevir en sujetos infectados con VHC con insuficiencia renal, con o sin hemodiálisis, no son clínicamente relevantes [véase Uso en poblaciones específicas (8.8)].
Insuficiencia hepática
La farmacocinética de elbasvir y grazoprevir se evaluó en sujetos no infectados con VHC con insuficiencia hepática leve (categoría Child-Pugh A [CP-A], puntuación de 5-6), insuficiencia hepática moderada (categoría Child-Pugh B [CP-B], puntuación de 7-9) e insuficiencia hepática grave (categoría Child-Pugh C [CP-C], puntuación de 10-15). Además, la farmacocinética de elbasvir y grazoprevir también se evaluó en sujetos infectados con VHC, incluidos sujetos con cirrosis compensada de CP-A.
En relación con sujetos no infectados con VHC con función hepática normal, no se observaron diferencias clínicamente relevantes en los valores de AUC de elbasvir en sujetos no infectados con VHC con insuficiencia hepática leve, moderada o grave. En análisis farmacocinéticos poblacionales, la AUC en estado estacionario de elbasvir fue similar en sujetos infectados con VHC con cirrosis compensada en comparación con sujetos infectados con VHC sin cirrosis.
En relación con sujetos no infectados con VHC con función hepática normal, los valores de AUC de grazoprevir fueron 1,7 veces, 5 veces y 12 veces más altos, respectivamente, en sujetos no infectados con VHC con insuficiencia hepática leve, moderada y grave. En análisis farmacocinéticos poblacionales, los valores de AUC en estado estacionario de grazoprevir fueron 1,65 veces más altos en sujetos infectados con VHC con cirrosis compensada en comparación con sujetos infectados con VHC sin cirrosis.
Estudios de interacción farmacológica
Se realizaron estudios de interacción farmacológica en adultos sanos con elbasvir, grazoprevir o la administración conjunta de elbasvir y grazoprevir y fármacos que probablemente se administrarán conjuntamente o fármacos comúnmente utilizados como sondas para interacciones farmacocinéticas. Tabla 9 resume los efectos de los fármacos administrados conjuntamente en las exposiciones de los componentes individuales de ZEPATIER (elbasvir y grazoprevir). Tabla 10 resume los efectos de los componentes individuales de ZEPATIER en las exposiciones de los fármacos administrados conjuntamente. Para información sobre las recomendaciones clínicas, [véase Contraindicaciones (4), Advertencias y Precauciones (5) y Interacciones farmacológicas (7)].
Elbasvir y grazoprevir son sustratos de CYP3A y P-gp, pero el papel de P-gp intestinal en la absorción de elbasvir y grazoprevir parece ser mínimo. La administración conjunta de inductores moderados y fuertes de CYP3A con ZEPATIER puede disminuir las concentraciones plasmáticas de elbasvir y grazoprevir, lo que puede conducir a un efecto terapéutico reducido de ZEPATIER. La administración conjunta de inhibidores fuertes de CYP3A4 con ZEPATIER puede aumentar las concentraciones plasmáticas de elbasvir y grazoprevir.
Grazoprevir es un sustrato de OATP1B1/3. La administración conjunta de ZEPATIER con fármacos que inhiben los transportadores OATP1B1/3 puede resultar en un aumento clínicamente relevante en las concentraciones plasmáticas de grazoprevir.
Elbasvir no es un inhibidor de CYP3A in vitro y grazoprevir es un inhibidor débil de CYP3A en humanos. La administración conjunta con grazoprevir resultó en un aumento del 34% en la exposición plasmática de midazolam y un 43% en la exposición plasmática de tacrolimus (véase Tablas 6 y 10). Elbasvir inhibió P-gp in vitro, pero no se observaron aumentos clínicamente relevantes en las concentraciones de digoxina (un sustrato de P-gp; véase Tabla 10) mediante la administración conjunta de elbasvir. Grazoprevir no es un inhibidor de P-gp in vitro. Elbasvir y grazoprevir son inhibidores del transportador de fármacos proteína de resistencia al cáncer de mama (BCRP) a nivel intestinal en humanos y pueden aumentar las concentraciones plasmáticas de los sustratos de BCRP administrados conjuntamente.
No se esperan interacciones medicamentosas clínicamente significativas con ZEPATIER como inhibidor de otras enzimas CYP (CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19 y CYP2D6), UGT1A1, esterasas (CES1, CES2 y CatA), transportadores de aniones orgánicos (OAT) 1 y OAT3, y transportador de cationes orgánicos (OCT) 2, y la administración de dosis múltiples de elbasvir o grazoprevir es poco probable que induzca el metabolismo de los fármacos metabolizados por CYP1A2, CYP2B6 o CYP3A según los datos in vitro.
| Fármaco coadministrado | Régimen del fármaco coadministrado | Régimen de EBR o/y GZR | N | Razón media geométrica [IC del 90%] de la FC de EBR y GZR con/sin fármaco coadministrado (Sin efecto=1,00) | |||
|---|---|---|---|---|---|---|---|
| AUC* | Cmax | C24 | |||||
| Abreviaturas: EBR, elbasvir; GZR, grazoprevir; IV, intravenoso; PO, oral; EBR + GZR, administración de EBR y GZR como pastillas separadas; EBR/GZR, administración de EBR y GZR como una sola tableta de combinación de dosis fija. | |||||||
| Antifúngico | |||||||
| Ketoconazol | 400 mg una vez al día | EBR 50 mg dosis única | 7 | EBR | 1.80 (1.41, 2.29) | 1.29 (1.00, 1.66) | 1.89 (1.37, 2.60) |
| 400 mg una vez al día | GZR 100 mg dosis única | 8 | GZR | 3.02 (2.42, 3.76) | 1.13 (0.77, 1.67) | 2.01 (1.49, 2.71) | |
| Antimiobácterico | |||||||
| Rifampicina | 600 mg dosis única IV | EBR 50 mg dosis única | 14 | EBR | 1.22 (1.06, 1.40) | 1.41 (1.18, 1.68) | 1.31 (1.12, 1.53) |
| 600 mg dosis única PO | EBR 50 mg dosis única | 14 | EBR | 1.17 (0.98, 1.39) | 1.29 (1.06, 1.58) | 1.21 (1.03, 1.43) | |
| 600 mg PO una vez al día | GZR 200 mg una vez al día | 12 | GZR | 0.93 (0.75, 1.17) | 1.16 (0.82, 1.65) | 0.10 (0.07, 0.13) | |
| 600 mg IV dosis única | GZR 200 mg dosis única | 12 | GZR | 10.21 (8.68, 12.00) | 10.94 (8.92, 13.43) | 1.77 (1.40, 2.24) | |
| 600 mg PO dosis única | GZR 200 mg una vez al día | 12 | GZR | 8.35 (7.38, 9.45)† | 6.52 (5.16, 8.24) | 1.62 (1.32, 1.98) | |
| Antiviral para el VHC | |||||||
| EBR | 20 mg una vez al día | GZR 200 mg una vez al día | 10 | GZR | 0.90 (0.63, 1.28) | 0.87 (0.50, 1.52) | 0.94 (0.77, 1.15) |
| GZR | 200 mg una vez al día | EBR 20 mg una vez al día | 10 | EBR | 1.01 (0.83, 1.24) | 0.93 (0.76, 1.13) | 1.02 (0.83, 1.24) |
| Inhibidor de la Proteasa del VIH | |||||||
| Atazanavir/ ritonavir | 300 mg/100 mg una vez al día | EBR 50 mg una vez al día | 10 | EBR | 4.76 (4.07, 5.56) | 4.15 (3.46, 4.97) | 6.45 (5.51, 7.54) |
| 300 mg/100 mg una vez al día | GZR 200 mg una vez al día | 12 | GZR | 10.58 (7.78, 14.39) | 6.24 (4.42, 8.81) | 11.64 (7.96, 17.02) | |
| Darunavir/ ritonavir | 600 mg/100 mg dos veces al día | EBR 50 mg una vez al día | 10 | EBR | 1.66 (1.35, 2.05) | 1.67 (1.36, 2.05) | 1.82 (1.39, 2.39) |
| 600 mg/100 mg dos veces al día | GZR 200 mg una vez al día | 13 | GZR | 7.50 (5.92, 9.51) | 5.27 (4.04, 6.86) | 8.05 (6.33, 10.24) | |
| Lopinavir/ ritonavir | 400 mg/100 mg dos veces al día | EBR 50 mg una vez al día | 10 | EBR | 3.71 (3.05, 4.53) | 2.87 (2.29, 3.58) | 4.58 (3.72, 5.64) |
| 400 mg/100 mg dos veces al día | GZR 200 mg una vez al día | 13 | GZR | 12.86 (10.25, 16.13) | 7.31 (5.65, 9.45) | 21.70 (12.99, 36.25) | |
| Ritonavir‡ | 100 mg dos veces al día | GZR 200 mg dosis única | 10 | GZR | 2.03 (1.60, 2.56) | 1.15 (0.60, 2.18) | 1.88 (1.65, 2.14) |
| Inhibidor de la Transferencia de la Hebra de la Integrasa del VIH | |||||||
| Dolutegravir | 50 mg dosis única | EBR 50 mg + GZR 200 mg una vez al día | 12 | EBR | 0.98 (0.93, 1.04) | 0.97 (0.89, 1.05) | 0.98 (0.93, 1.03) |
| 50 mg dosis única | EBR 50 mg + GZR 200 mg una vez al día | 12 | GZR | 0.81 (0.67, 0.97) | 0.64 (0.44, 0.93) | 0.86 (0.79, 0.93) | |
| Raltegravir | 400 mg dosis única | EBR 50 mg dosis única | 10 | EBR | 0.81 (0.57, 1.17) | 0.89 (0.61, 1.29) | 0.80 (0.55, 1.16) |
| 400 mg dos veces al día | GZR 200 mg una vez al día | 11 | GZR | 0.89 (0.72, 1.09) | 0.85 (0.62, 1.16) | 0.90 (0.82, 0.99) | |
| Inhibidor No Nucleósido de la Transcriptasa Inversa del VIH | |||||||
| Efavirenz | 600 mg una vez al día | EBR 50 mg una vez al día | 10 | EBR | 0.46 (0.36, 0.59) | 0.55 (0.41, 0.73) | 0.41 (0.28, 0.59) |
| 600 mg una vez al día | GZR 200 mg una vez al día | 12 | GZR | 0.17 (0.13, 0.24) | 0.13 (0.09, 0.19) | 0.31 (0.25, 0.38) | |
| Rilpivirine | 25 mg una vez al día | EBR 50 mg + GZR 200 mg una vez al día | 19 | EBR | 1.07 (1.00, 1.15) | 1.07 (0.99, 1.16) | 1.04 (0.98, 1.11) |
| 25 mg una vez al día | EBR 50 mg + GZR 200 mg una vez al día | 19 | GZR | 0.98 (0.89, 1.07) | 0.97 (0.83, 1.14) | 1.00 (0.93, 1.07) | |
| Inhibidor de la transcriptasa inversa de nucleótidos del VIH | |||||||
| Tenofovir disoproxil fumarato | 300 mg una vez al día | EBR 50 mg una vez al día | 10 | EBR | 0.93 (0.82, 1.05) | 0.88 (0.77, 1.00) | 0.92 (0.81, 1.05) |
| 300 mg una vez al día | GZR 200 mg una vez al día | 12 | GZR | 0.86 (0.65, 1.12) | 0.78 (0.51, 1.18) | 0.89 (0.78, 1.01) | |
| Régimen de combinación de dosis fija del VIH | |||||||
| Elvitegravir/ cobicistat/ emtricitabina/ tenofovir disoproxil fumarato | 150 mg/ 150 mg/ 200 mg/ 300 mg una vez al día | EBR 50 mg/ GZR 100 mg una vez al día | 21 | EBR | 2.18 (2.02, 2.35) | 1.91 (1.77, 2.05) | 2.38 (2.19, 2.60) |
| EBR 50 mg/ GZR 100 mg una vez al día | 21 | GZR | 5.36 (4.48, 6.43) | 4.59 (3.70, 5.69) | 2.78 (2.48, 3.11) | ||
| Inmunosupresor | |||||||
| Ciclosporina | 400 mg dosis única | EBR 50 mg + GZR 200 mg una vez al día | 14 | EBR | 1.98 (1.84, 2.13) | 1.95 (1.84, 2.07) | 2.21 (1.98, 2.47) |
| 400 mg dosis única | EBR 50 mg + GZR 200 mg una vez al día | 14 | GZR | 15.21 (12.83, 18.04) | 17.00 (12.94, 22.34) | 3.39 (2.82, 4.09) | |
| Micofenolato de mofetilo | 1000 mg dosis única | EBR 50 mg + GZR 200 mg una vez al día | 14 | EBR | 1.07 (1.00, 1.14) | 1.07 (0.98, 1.16) | 1.05 (0.97, 1.14) |
| 1000 mg dosis única | EBR 50 mg + GZR 200 mg una vez al día | 14 | GZR | 0.74 (0.60, 0.92) | 0.58 (0.42, 0.82) | 0.97 (0.89, 1.06) | |
| Prednisona | 40 mg dosis única | EBR 50 mg + GZR 200 mg una vez al día | 14 | EBR | 1.17 (1.11, 1.24) | 1.25 (1.16, 1.35) | 1.04 (0.97, 1.12) |
| 40 mg dosis única | EBR 50 mg + GZR 200 mg una vez al día | 14 | GZR | 1.09 (0.95, 1.25) | 1.34 (1.10, 1.62) | 0.93 (0.87, 1.00) | |
| Tacrolimus | 2 mg dosis única | EBR 50 mg + GZR 200 mg una vez al día | 16 | EBR | 0.97 (0.90, 1.06) | 0.99 (0.88, 1.10) | 0.92 (0.83, 1.02) |
| 2 mg dosis única | EBR 50 mg + GZR 200 mg una vez al día | 16 | GZR | 1.12 (0.97, 1.30) | 1.07 (0.83, 1.37) | 0.94 (0.87, 1.02) | |
| Terapia de sustitución de opioides | |||||||
| Buprenorfina/naloxona | 8 mg/2 mg dosis única | EBR 50 mg dosis única | 15 | EBR | 1.22 (0.98, 1.52) | 1.13 (0.87, 1.46) | 1.22 (0.99, 1.51) |
| 8-24 mg/ 2-6 mg una vez al día | GZR 200 mg una vez al día | 12§ | GZR | 0.86 (0.63, 1.18) | 0.80 (0.54, 1.20) | 0.97 (0.77, 1.22) | |
| Metadona | 20-120 mg una vez al día | EBR 50 mg una vez al día | 10§ | EBR | 1.20 (0.94, 1.53) | 1.23 (0.94, 1.62) | 1.32 (1.03, 1.68) |
| 20-150 mg una vez al día | GZR 200 mg una vez al día | 12§ | GZR | 1.03 (0.76, 1.41) | 0.89 (0.60, 1.32) | 0.98 (0.79, 1.23) | |
| Agente reductor de ácido | |||||||
| Famotidina | 20 mg dosis única | EBR 50 mg/ GZR 100 mg dosis única | 16 | EBR | 1.05 (0.92, 1.18) | 1.11 (0.98, 1.26) | 1.03 (0.91, 1.17) |
| 20 mg dosis única | EBR 50 mg/ GZR 100 mg dosis única | 16 | GZR | 1.10 (0.95, 1.28) | 0.89 (0.71, 1.11) | 1.12 (0.97, 1.30) | |
| Pantoprazol | 40 mg una vez al día | EBR 50 mg/ GZR 100 mg dosis única | 16 | EBR | 1.05 (0.93, 1.18) | 1.02 (0.92, 1.14) | 1.03 (0.92, 1.17) |
| 40 mg una vez al día | EBR 50 mg/ GZR 100 mg dosis única | 16 | GZR | 1.12 (0.96, 1.30) | 1.10 (0.89, 1.37) | 1.17 (1.02, 1.34) | |
| Enlazador de fosfato | |||||||
| Acetato de calcio | 2668 mg dosis única | EBR 50 mg + GZR 100 mg dosis única | 12 | EBR | 0.92 (0.75, 1.14) | 0.86 (0.71, 1.04) | 0.87 (0.70, 1.09) |
| 2668 mg dosis única | EBR 50 mg + GZR 100 mg dosis única | 12 | GZR | 0.79 (0.68, 0.91) | 0.57 (0.40, 0.83) | 0.77 (0.61, 0.99) | |
| Carbonato de sevelamer | 2400 mg dosis única | EBR 50 mg + GZR 100 mg dosis única | 12 | EBR | 1.13 (0.94, 1.37) | 1.07 (0.88, 1.29) | 1.22 (1.02, 1.45) |
| 2400 mg dosis única | EBR 50 mg + GZR 100 mg dosis única | 12 | GZR | 0.82 (0.68, 0.99) | 0.53 (0.37, 0.76) | 0.84 (0.71, 0.99) | |
| Estatina | |||||||
| Atorvastatina | 20 mg dosis única | GZR 200 mg una vez al día | 9 | GZR | 1.26 (0.97, 1.64) | 1.26 (0.83, 1.90) | 1.11 (1.00, 1.23) |
| Pitavastatina | 1 mg dosis única | GZR 200 mg una vez al día | 9 | GZR | 0.81 (0.70, 0.95) | 0.72 (0.57, 0.92) | 0.91 (0.82, 1.01) |
| Pravastatina | 40 mg dosis única | EBR 50 mg + GZR 200 mg una vez al día | 12 | EBR | 0.98 (0.93, 1.02) | 0.97 (0.89, 1.05) | 0.97 (0.92, 1.02) |
| 40 mg dosis única | EBR 50 mg + GZR 200 mg una vez al día | 12 | GZR | 1.24 (1.00, 1.53) | 1.42 (1.00, 2.03) | 1.07 (0.99, 1.16) | |
| Rosuvastatin | 10 mg dosis única | EBR 50 mg + GZR 200 mg dosis única | 11 | EBR | 1.09 (0.98, 1.21) | 1.11 (0.99, 1.26) | 0.96 (0.86, 1.08) |
| 10 mg dosis única | GZR 200 mg una vez al día | 11 | GZR | 1.16 (0.94, 1.44) | 1.13 (0.77, 1.65) | 0.93 (0.84, 1.03) | |
| 10 mg dosis única | EBR 50 mg + GZR 200 mg una vez al día | 11 | GZR | 1.01 (0.79, 1.28) | 0.97 (0.63, 1.50) | 0.95 (0.87, 1.04) | |
| Fármaco coadministrado | Régimen del fármaco coadministrado | Administración de EBR o/y GZR | Régimen de EBR o/y GZR | N | Razón media geométrica [IC del 90%] de la farmacocinética del fármaco coadministrado con/sin EBR o/y GZR (Sin efecto=1,00) | ||
|---|---|---|---|---|---|---|---|
| AUC* | Cmax | Ctrough† | |||||
| Abreviaturas: EBR, elbasvir; GZR, grazoprevir; EBR + GZR, administración de EBR y GZR como comprimidos separados; EBR/GZR, administración de EBR y GZR como un comprimido de combinación de dosis fija única | |||||||
| Sustrato de P-gp | |||||||
| Digoxina | Digoxina 0,25 mg dosis única | EBR | 50 mg una vez al día | 18 | 1,11 (1,02, 1,22) | 1,47 (1,25, 1,73) | — |
| Sustrato de CYP3A | |||||||
| Midazolam | Midazolam 2 mg dosis única | GZR | 200 mg una vez al día | 11 | 1,34 (1,29, 1,39) | 1,15 (1,01, 1,31) | — |
| Sustrato de CYP2C8 | |||||||
| Montelukast | Montelukast 10 mg dosis única | GZR | 200 mg una vez al día | 23 | 1,11 (1,01, 1,20) | 0,92 (0,81, 1,06) | 1,39 (1,25, 1,56) |
| Antiviral para la HCV | |||||||
| GS-331007 | Sofosbuvir 400 mg dosis única | EBR + GZR | 50 mg + 200 mg una vez al día | 16 | 1,13 (1,05, 1,21) | 0,87 (0,78, 0,96) | 1,53 (1,43, 1,63) |
| Sofosbuvir | Sofosbuvir 400 mg dosis única | EBR + GZR | 50 mg + 200 mg una vez al día | 16 | 2,43 (2,12, 2,79)‡ | 2,27 (1,72, 2,99) | — |
| Inhibidor de la proteasa del VIH | |||||||
| Atazanavir/ ritonavir | Atazanavir 300 mg/ ritonavir 100 mg una vez al día | EBR | 50 mg una vez al día | 8 | 1,07 (0,98, 1,17) | 1,02 (0,96, 1,08) | 1,15 (1,02, 1,29) |
| Atazanavir 300 mg/ ritonavir 100 mg una vez al día | GZR | 200 mg una vez al día | 11 | 1,43 (1,30, 1,57) | 1,12 (1,01, 1,24) | 1,23 (1,13, 1,34) | |
| Darunavir/ ritonavir | Darunavir 600 mg/ ritonavir 100 mg dos veces al día | EBR | 50 mg una vez al día | 8 | 0,95 (0,86, 1,06) | 0,95 (0,85, 1,05) | 0,94 (0,85, 1,05) |
| Darunavir 600 mg/ ritonavir 100 mg dos veces al día | GZR | 200 mg una vez al día | 13 | 1.11 (0.99, 1.24) | 1.10 (0.96, 1.25) | 1.00 (0.85, 1.18) | |
| Lopinavir/ ritonavir | Lopinavir 400 mg/ ritonavir 100 mg dos veces al día | EBR | 50 mg una vez al día | 9 | 1.02 (0.93, 1.13) | 1.02 (0.92, 1.13) | 1.07 (0.97, 1.18) |
| Lopinavir 400 mg/ ritonavir 100 mg dos veces al día | GZR | 200 mg una vez al día | 13 | 1.03 (0.96, 1.16) | 0.97 (0.88, 1.08) | 0.97 (0.81, 1.15) | |
| Inhibidor de la transferencia de la cadena de la integrasa del VIH | |||||||
| Dolutegravir | Dolutegravir 50 mg dosis única | EBR + GZR | 50 mg + 200 mg una vez al día | 12 | 1.16 (1.00, 1.34) | 1.22 (1.05, 1.40) | 1.14 (0.95, 1.36) |
| Raltegravir | Raltegravir 400 mg dosis única | EBR | 50 mg dosis única | 10 | 1.02 (0.81, 1.27) | 1.09 (0.83, 1.44) | 0.99 (0.80, 1.22)§ |
| Raltegravir 400 mg dos veces al día | GZR | 200 mg una vez al día | 11 | 1.43 (0.89, 2.30) | 1.46 (0.78, 2.73) | 1.47 (1.09, 2.00) | |
| Inhibidor no nucleósido de la transcriptasa inversa del VIH | |||||||
| Efavirenz | Efavirenz 600 mg una vez al día | EBR | 50 mg una vez al día | 7 | 0.82 (0.78, 0.86) | 0.74 (0.67, 0.82) | 0.91 (0.87, 0.96) |
| Efavirenz 600 mg una vez al día | GZR | 200 mg una vez al día | 11 | 1.00 (0.96, 1.05) | 1.03 (0.99, 1.08) | 0.93 (0.88, 0.98) | |
| Rilpivirine | Rilpivirine 25 mg una vez al día | EBR + GZR | 50 mg + 200 mg una vez al día | 19 | 1.13 (1.07, 1.20) | 1.07 (0.97, 1.17) | 1.16 (1.09, 1.23) |
| Inhibidor de la transcriptasa inversa nucleótido del VIH | |||||||
| Tenofovir disoproxil fumarate | Tenofovir disoproxil fumarate 300 mg una vez al día | EBR | 50 mg una vez al día | 10 | 1.34 (1.23, 1.47) | 1.47 (1.32, 1.63) | 1.29 (1.18, 1.41) |
| Tenofovir disoproxil fumarate 300 mg una vez al día | GZR | 200 mg una vez al día | 12 | 1.18 (1.09, 1.28) | 1.14 (1.04, 1.25) | 1.24 (1.10, 1.39) | |
| Tenofovir disoproxil fumarate 300 mg una vez al día | EBR/GZR | 50 mg + 100 mg una vez al día | 13 | 1.27 (1.20, 1.35) | 1.14 (0.95, 1.36) | 1.23 (1.09, 1.40) | |
| Régimen de combinación de dosis fija del VIH | |||||||
| Elvitegravir/ cobicistat/ emtricitabine/ tenofovir disoproxil fumarate | Elvitegravir 150 mg una vez al día | EBR/GZR | 50 mg / 100 mg una vez al día | 22 | 1.10 (1.00, 1.21) | 1.02 (0.93, 1.11) | 1.31 (1.11, 1.55) |
| Cobicistat 150 mg una vez al día | EBR/GZR | 50 mg / 100 mg una vez al día | 22 | 1.49 (1.42, 1.57) | 1.39 (1.29, 1.50) | — | |
| Emtricitabina 200 mg una vez al día | EBR/GZR | 50 mg / 100 mg una vez al día | 22 | 1.07 (1.03, 1.10) | 0.96 (0.90, 1.02) | 1.19 (1.13, 1.25) | |
| Tenofovir disoproxil fumarato 300 mg una vez al día | EBR/GZR | 50 mg / 100 mg una vez al día | 22 | 1.18 (1.13, 1.24) | 1.25 (1.14, 1.37) | 1.20 (1.15, 1.26) | |
| Inmunosupresor | |||||||
| Ciclosporina | Ciclosporina 400 mg dosis única | EBR + GZR | 50 mg + 200 mg una vez al día | 14 | 0.96 (0.90, 1.02) | 0.90 (0.85, 0.97) | 1.00 (0.92, 1.08)§ |
| Ácido micofenólico | Micofenolato de mofetilo 1000 mg dosis única | EBR + GZR | 50 mg + 200 mg una vez al día | 14 | 0.95 (0.87, 1.03) | 0.85 (0.67, 1.07) | — |
| Prednisolona | Prednisona 40 mg dosis única | EBR + GZR | 50 mg + 200 mg una vez al día | 14 | 1.08 (1.01, 1.16) | 1.04 (0.99, 1.09) | — |
| Prednisona | Prednisona 40 mg dosis única | EBR + GZR | 50 mg + 200 mg una vez al día | 14 | 1.08 (1.00, 1.17) | 1.05 (1.00, 1.10) | — |
| Tacrolimus | Tacrolimus 2 mg dosis única |
EBR + GZR | 50 mg + 200 mg una vez al día | 16 | 1.43 (1.24, 1.64) | 0.60 (0.52, 0.69) | 1.70 (1.49, 1.94)§ |
| Anticonceptivo oral | |||||||
| Etinilestradiol (EE) | 0.03 mg EE/ 0.15 mg LNG dosis única | EBR | 50 mg una vez al día | 20 | 1.01 (0.97, 1.05) | 1.10 (1.05, 1.16) | — |
| GZR | 200 mg una vez al día | 20 | 1.10 (1.05, 1.14) | 1.05 (0.98, 1.12) | — | ||
| Levonorgestrel (LNG) | EBR | 50 mg una vez al día | 20 | 1.14 (1.04, 1.24) | 1.02 (0.95, 1.08) | — | |
| GZR | 200 mg una vez al día | 20 | 1.23 (1.15, 1.32) | 0.93 (0.84, 1.03) | — | ||
| Terapia de sustitución de opioides | |||||||
| Buprenorfina | Buprenorfina 8 mg/Naloxona 2 mg dosis única | EBR | 50 mg una vez al día | 15 | 0.98 (0.89, 1.08) | 0.94 (0.82, 1.08) | 0.98 (0.88, 1.09) |
| Buprenorfina 8-24 mg/ Naloxona 2-6 mg una vez al día | GZR | 200 mg una vez al día | 12 | 0.98 (0.81, 1.19) | 0.90 (0.76, 1.07) | — | |
| R-Metadona | Metadona 20-120 mg una vez al día | EBR | 50 mg una vez al día | 10 | 1.03 (0.92, 1.15) | 1.07 (0.95, 1.20) | 1.10 (0.96, 1.26) |
| Metadona 20-150 mg una vez al día | GZR | 200 mg una vez al día | 12 | 1.09 (1.02, 1.17) | 1.03 (0.96, 1.11) | — | |
| S-Methadone | Methadone 20-120 mg una vez al día | EBR | 50 mg una vez al día | 10 | 1.09 (0.94, 1.26) | 1.09 (0.95, 1.25) | 1.20 (0.98, 1.47) |
| Methadone 20-150 mg una vez al día | GZR | 200 mg una vez al día | 12 | 1.23 (1.12, 1.35) | 1.15 (1.07, 1.25) | — | |
| Statin | |||||||
| Atorvastatin | Atorvastatin 10 mg dosis única | EBR + GZR | 50 mg + 200 mg una vez al día | 16 | 1.94 (1.63, 2.33) | 4.34 (3.10, 6.07) | 0.21 (0.17, 0.26) |
| Pitavastatin | Pitavastatin 1 mg dosis única | GZR | 200 mg una vez al día | 9 | 1.11 (0.91, 1.34) | 1.27 (1.07, 1.52) | — |
| Pravastatin | Pravastatin 40 mg dosis única | EBR + GZR | 50 mg + 200 mg una vez al día | 12 | 1.33 (1.09, 1.64)¶ | 1.28 (1.05, 1.55) | — |
| Rosuvastatin | Rosuvastatin 10 mg dosis única | EBR + GZR | 50 mg + 200 mg una vez al día | 12 | 2.26 (1.89, 2.69)# | 5.49 (4.29, 7.04) | 0.98 (0.84, 1.13) |
12.4 Microbiología
Mecanismo de acción
ZEPATIER combina dos agentes antivirales de acción directa con mecanismos de acción distintos y perfiles de resistencia no superpuestos para atacar el VHC en múltiples pasos del ciclo de vida viral.
Elbasvir es un inhibidor de la NS5A del VHC, que es esencial para la replicación del ARN viral y el ensamblaje de viriones. El mecanismo de acción de elbasvir se ha caracterizado en base a la actividad antiviral en cultivos celulares y estudios de mapeo de resistencia a fármacos.
Grazoprevir es un inhibidor de la proteasa NS3/4A del VHC, que es necesaria para la escisión proteolítica de la poliproteína codificada por el VHC (en formas maduras de las proteínas NS3, NS4A, NS4B, NS5A y NS5B) y es esencial para la replicación viral. En un ensayo bioquímico, grazoprevir inhibió la actividad proteolítica de las enzimas recombinantes de la proteasa NS3/4A del VHC de los genotipos 1a, 1b y 4a con valores de IC50 de 7 pM, 4 pM y 62 pM, respectivamente.
Actividad antiviral
En ensayos de replicones del VHC, los valores de EC50 de elbasvir contra replicones de longitud completa de los genotipos 1a, 1b y 4 fueron 4 pM, 3 pM y 0,3 pM, respectivamente. Los valores medianos de EC50 de elbasvir contra replicones quiméricos que codifican secuencias de NS5A de aislados clínicos fueron 5 pM para el genotipo 1a (rango 3-9 pM; N=5), 9 pM para el genotipo 1b (rango 5-10 pM; N=4), 0,2 pM para el genotipo 4a (rango 0,2-0,2 pM; N=2), 3600 pM para el genotipo 4b (rango 17 pM-34000 pM; N=3), 0,45 pM para el genotipo 4d (rango 0,4-0,5 pM; N=2), 1,9 pM para el genotipo 4f (N=1), 36,3 pM para el genotipo 4g (rango 0,6-72 pM; N=2), 0,6 pM para el genotipo 4m (rango 0,4-0,7 pM; N=2), 2,2 pM para el genotipo 4o (N=1) y 0,5 pM para el genotipo 4q (N=1).
En ensayos de replicones del VHC, los valores de EC50 de grazoprevir contra replicones de longitud completa de los genotipos 1a, 1b y 4 fueron 0,4 nM, 0,5 nM y 0,3 nM, respectivamente. Los valores medianos de EC50 de grazoprevir contra replicones quiméricos que codifican secuencias de NS3/4A de aislados clínicos fueron 0,8 nM para el genotipo 1a (rango 0,4-5,1 nM; N=10), 0,3 nM para el genotipo 1b (rango 0,2-5,9 nM; N=9), 0,3 nM para el genotipo 4a (N=1), 0,16 nM para el genotipo 4b (rango 0,11-0,2 nM; N=2) y 0,24 nM para el genotipo 4g (rango 0,15-0,33 nM; N=2).
Actividad antiviral combinada
La evaluación de elbasvir en combinación con grazoprevir o ribavirina no mostró ningún efecto antagónico en la reducción de los niveles de ARN del VHC en las células de replicones. La evaluación de grazoprevir en combinación con ribavirina no mostró ningún efecto antagónico en la reducción de los niveles de ARN del VHC en las células de replicones.
Resistencia
En cultivo celular
Se han seleccionado replicones del VHC con susceptibilidad reducida a elbasvir y grazoprevir en cultivo celular para los genotipos 1a, 1b y 4, lo que dio lugar a la aparición de sustituciones de aminoácidos asociadas a la resistencia en NS5A o NS3, respectivamente. La mayoría de las sustituciones de aminoácidos en NS5A o NS3 seleccionadas en cultivo celular o identificadas en ensayos clínicos de fase 2b y 3 se caracterizaron fenotípicamente en replicones de genotipo 1a, 1b o 4.
Para elbasvir, en replicones del VHC de genotipo 1a, las sustituciones únicas de NS5A M28A/G/T, Q30D/E/H/K/R, L31M/V, H58D e Y93C/H/N redujeron la actividad antiviral de elbasvir entre 1,5 y 2000 veces. En replicones de genotipo 1b, las sustituciones únicas de NS5A L28M, L31F e Y93H redujeron la actividad antiviral de elbasvir entre 2 y 17 veces. En replicones de genotipo 4, las sustituciones únicas de NS5A L30S, M31V e Y93H redujeron la actividad antiviral de elbasvir entre 3 y 23 veces. En general, en replicones del VHC de genotipo 1a, 1b o 4, las combinaciones de sustituciones asociadas a la resistencia a elbasvir redujeron aún más la actividad antiviral de elbasvir.
Para grazoprevir, en replicones del VHC de genotipo 1a, las sustituciones únicas de NS3 Y56H, R155K, A156G/T/V y D168A/E/G/N/S/V/Y redujeron la actividad antiviral de grazoprevir entre 2 y 81 veces; las sustituciones únicas V36L/M, Q80K/R o V107I no tuvieron ningún impacto en la actividad antiviral de grazoprevir en cultivo celular. En replicones de genotipo 1b, las sustituciones únicas de NS3 F43S, Y56F, V107I, A156S/T/V y D168A/G/V redujeron la actividad antiviral de grazoprevir entre 1,5 y 375 veces. En replicones de genotipo 4, las sustituciones únicas de NS3 D168A/V redujeron la actividad antiviral de grazoprevir entre 110 y 320 veces. En general, en replicones del VHC de genotipo 1a, 1b o 4, las combinaciones de sustituciones asociadas a la resistencia a grazoprevir redujeron aún más la actividad antiviral de grazoprevir.
En estudios clínicos
En un análisis agrupado de sujetos tratados con regímenes que contenían ZEPATIER o elbasvir + grazoprevir con o sin ribavirina en ensayos clínicos de fase 2 y 3, se realizaron análisis de resistencia de ambos objetivos farmacológicos para 50 sujetos que experimentaron fracaso virológico y tenían datos de secuencia disponibles (6 con fracaso virológico durante el tratamiento, 44 con recaída posterior al tratamiento). Las sustituciones emergentes durante el tratamiento observadas en las poblaciones virales de estos sujetos en función de los genotipos y subtipos del VHC se muestran en Tabla 11. Se detectaron sustituciones de NS5A emergentes durante el tratamiento en 30/37 (81%) sujetos infectados con genotipo 1a, 7/8 (88%) sujetos infectados con genotipo 1b y 5/5 (100%) sujetos infectados con genotipo 4. Las sustituciones de NS5A emergentes durante el tratamiento más comunes en el genotipo 1a fueron en la posición Q30 (n=22). Se detectaron sustituciones de NS3 emergentes durante el tratamiento en 29/37 (78%) sujetos infectados con genotipo 1a, 2/8 (25%) sujetos infectados con genotipo 1b y 2/5 (40%) sujetos infectados con genotipo 4. Las sustituciones de NS3 emergentes durante el tratamiento más comunes en el genotipo 1a fueron en la posición D168 (n=18). Se detectaron sustituciones emergentes durante el tratamiento en ambos objetivos farmacológicos del VHC en 23/37 (62%) sujetos infectados con genotipo 1a, 1/8 (13%) sujetos infectados con genotipo 1b y 2/5 (40%) sujetos infectados con genotipo 4.
| Objetivo | Genotipo 1a N = 37 |
Genotipo 1b N = 8 |
Genotipo 4 N = 5 |
|---|---|---|---|
| NS5A | M28A/G/T, Q30H/K/R/Y, L31F/M/V, H58D, Y93H/N/S | L28M, L31F/V, Y93H | L28S/T, M31I/V, P58D, Y93H |
| NS3 | V36L/M, Y56H, V107I, R155I/K, A156G/T/V, V158A, D168A/G/N/V/Y | Y56F, V107I, A156T | A156M/T/V, D168A/G, V170I |
Persistencia de las Sustituciones Asociadas a Resistencia
La persistencia de las sustituciones de aminoácidos emergentes durante el tratamiento con elbasvir y grazoprevir en NS5A y NS3, respectivamente, se evaluó en sujetos infectados con VHC genotipo 1 en ensayos de fase 2 y 3 cuyo virus tenía sustituciones asociadas a resistencia emergentes durante el tratamiento en el objetivo farmacológico, y con datos disponibles hasta al menos 24 semanas después del tratamiento utilizando análisis de secuencia de nucleótidos poblacionales.
Las poblaciones virales con sustituciones asociadas a resistencia NS5A emergentes durante el tratamiento fueron generalmente más persistentes que las que tenían sustituciones asociadas a resistencia NS3. Entre los sujetos infectados con genotipo 1a, las sustituciones asociadas a resistencia NS5A persistieron a niveles detectables en la semana 12 de seguimiento en el 95% (35/37) de los sujetos y en el 100% (9/9) de los sujetos con datos de la semana 24 de seguimiento. Entre los sujetos infectados con genotipo 1b, las sustituciones asociadas a resistencia NS5A persistieron a niveles detectables en el 100% (7/7) de los sujetos en la semana 12 de seguimiento y en el 100% (3/3) de los sujetos con datos de la semana 24 de seguimiento.
Entre los sujetos infectados con genotipo 1a, las sustituciones asociadas a resistencia NS3 persistieron a niveles detectables en la semana 24 de seguimiento en el 31% (4/13) de los sujetos. Entre los sujetos infectados con genotipo 1b, las sustituciones asociadas a resistencia NS3 persistieron a niveles detectables en la semana 24 de seguimiento en el 50% (1/2) de los sujetos.
Debido al número limitado de sujetos infectados con genotipo 4 con sustituciones asociadas a resistencia NS5A y NS3 emergentes durante el tratamiento, no se pudieron establecer tendencias en la persistencia de las sustituciones emergentes durante el tratamiento en este genotipo.
La falta de detección de un virus que contenga una sustitución asociada a resistencia no indica necesariamente que las poblaciones virales que portan esa sustitución hayan disminuido a un nivel de fondo que puede haber existido antes del tratamiento. Se desconoce el impacto clínico a largo plazo de la aparición o persistencia del virus que contiene sustituciones asociadas a resistencia a ZEPATIER.
Efecto de los Polimorfismos de Aminoácidos del VHC de Línea Base en la Respuesta al Tratamiento en Sujetos Infectados con Genotipo 1
Se realizaron análisis utilizando secuenciación de nucleótidos poblacionales para explorar la asociación entre los polimorfismos de aminoácidos NS5A o NS3 y la respuesta al tratamiento entre sujetos infectados con genotipo 1 naive al tratamiento y con experiencia en tratamiento. Se evaluaron los polimorfismos NS5A de línea base en posiciones asociadas a resistencia (centrándose en cualquier cambio de la referencia de subtipo en las posiciones de aminoácidos NS5A 28, 30, 31 o 93). Se evaluaron los polimorfismos NS3 de línea base en las posiciones 36, 54, 55, 56, 80, 107, 122, 132, 155, 156, 158, 168, 170 o 175. Los análisis de las tasas de SVR12 agruparon datos de sujetos naive a antivirales de acción directa y que recibieron ZEPATIER con o sin ribavirina en ensayos clínicos de fase 3, y censuraron a los sujetos que no alcanzaron SVR12 por razones no relacionadas con el fracaso virológico.
Genotipo 1a
En Estudios Clínicos
En sujetos infectados con genotipo 1a, la presencia de uno o más polimorfismos de aminoácidos del VHC NS5A en la posición M28, Q30, L31 o Y93 se asoció con una eficacia reducida de ZEPATIER durante 12 semanas (Tabla 12), independientemente de la historia previa de tratamiento o el estado de cirrosis. La prevalencia de polimorfismos en cualquiera de estas posiciones en sujetos infectados con genotipo 1a fue del 11% (62/561) en general, y del 12% (37/309) específicamente para los sujetos en los EE. UU. en los ensayos clínicos de fase 2 y fase 3 que evaluaron ZEPATIER durante 12 semanas o ZEPATIER más ribavirina durante 16 semanas. La prevalencia de polimorfismos en estas posiciones en sujetos infectados con genotipo 1a fue del 6% (35/561) en la posición M28, del 2% (11/561) en la posición Q30, del 3% (15/561) en la posición L31 y del 2% (10/561) en la posición Y93. Los polimorfismos en la posición H58 de NS5A fueron comunes (10%) y no se asociaron con una eficacia reducida de ZEPATIER, excepto para un solo sujeto con fracaso virológico cuyo virus tenía polimorfismos M28V y H58D de línea base.
Las tasas de SVR12 para los sujetos tratados con ZEPATIER durante 12 semanas fueron del 88% (29/33) para los sujetos con polimorfismos M28V/T/L (n=29, 3 y 1, respectivamente), del 40% (4/10) para los sujetos con polimorfismos Q30H/R/L (n=5, 3 y 2, respectivamente), del 38% (5/13) para los sujetos con un polimorfismo L31M y del 63% (5/8) para los sujetos con polimorfismos Y93C/H/N/S (n=3, 3, 1 y 1, respectivamente). Aunque los datos de los ensayos clínicos son limitados, entre los sujetos infectados con genotipo 1a con estos polimorfismos NS5A que recibieron ZEPATIER más ribavirina durante 16 semanas, seis de seis sujetos alcanzaron SVR12. Los polimorfismos NS5A específicos observados en los sujetos tratados con ZEPATIER más ribavirina durante 16 semanas incluyeron M28V (n=2), Q30H (n=1), L31M (n=2) o Y93C/H (n=1 cada uno).
| Estado de Polimorfismo NS5A | ZEPATIER 12 Semanas SVR12 % (n/N) |
ZEPATIER + RBV 16 Semanas SVR12 % (n/N) |
|---|---|---|
|
||
| Sin polimorfismo NS5A de línea base (M28, Q30, L31 o Y93) |
98% (441/450) | 100% (49/49) |
| Con polimorfismo NS5A de línea base (M28*, Q30*, L31* o Y93*) |
70% (39/56) | 100% (6/6) |
No hay datos suficientes de ensayos clínicos para determinar el impacto de los polimorfismos de aminoácidos HCV NS5A en sujetos con experiencia en tratamiento que fallaron en la terapia previa con PegIFN + RBV + inhibidor de la proteasa del VHC y recibieron ZEPATIER con ribavirina.
En sujetos infectados con genotipo 1a, el polimorfismo NS3 Q80K no afectó la respuesta al tratamiento. Los polimorfismos en otras posiciones asociadas a resistencia a NS3 fueron poco comunes y no se asociaron con una reducción de la eficacia del tratamiento.
En estudios observacionales poscomercialización
La eficacia (tasas de SVR12) en los estudios observacionales puede estar sujeta a ciertos sesgos y factores de confusión que no se pueden tener en cuenta en los análisis, en parte debido a la naturaleza de los diseños de estudio y las poblaciones estudiadas.
Protocolo 095
En el Protocolo 095, un subestudio de un estudio comparativo observacional prospectivo, se evaluó la eficacia del tratamiento con ZEPATIER más ribavirina durante 16 semanas en 29 pacientes infectados con VHC de genotipo 1a con 1 o más polimorfismos NS5A de referencia en las posiciones de aminoácidos M28, Q30, L31 y/o Y93. En general, la tasa de SVR12 para los pacientes con 1 o más polimorfismos NS5A de referencia en cualquiera de las 4 posiciones de aminoácidos fue del 93% (27/29). 23 pacientes tenían un polimorfismo NS5A en una sola posición de aminoácido en la línea de base. Las tasas de SVR12 para los pacientes con un solo polimorfismo en la posición de aminoácido M28, Q30, L31 o Y93 fueron del 100% (14/14), 100% (1/1), 33% (1/3) y 100% (5/5), respectivamente. Seis pacientes tenían polimorfismos NS5A en más de 1 posición de aminoácido (M28, Q30, L31 y/o Y93) en la línea de base. La tasa de SVR12 para estos pacientes fue del 100% (6/6).
Estudio de cohorte VA NS5A
En un estudio de cohorte retrospectivo de la Administración de Veteranos (VA) NS5A, se evaluó la eficacia del tratamiento con ZEPATIER más ribavirina durante 16 semanas en 93 pacientes infectados con VHC de genotipo 1a con 1 o más polimorfismos NS5A de referencia en las posiciones de aminoácidos M28, Q30, L31 y/o Y93. En general, la tasa de SVR12 para los pacientes con 1 o más polimorfismos NS5A de referencia en cualquiera de las 4 posiciones de aminoácidos fue del 81% (75/93). 65 pacientes tenían un polimorfismo NS5A en una sola posición de aminoácido en la línea de base. Las tasas de SVR12 para los pacientes con un solo polimorfismo en la posición de aminoácido M28, Q30, L31 o Y93 fueron del 94% (16/17), 100% (8/8), 84% (16/19) y 81% (17/21), respectivamente. 28 pacientes tenían polimorfismos NS5A en más de 1 posición de aminoácido (M28, Q30, L31 y/o Y93) en la línea de base. La tasa de SVR12 para estos pacientes fue del 64% (18/28).
Genotipo 1b
En estudios clínicos
En sujetos infectados con genotipo 1b tratados con ZEPATIER durante 12 semanas, las tasas de SVR12 (censuradas por fallo no virológico) fueron del 94% (48/51) y del 99% (247/248) para aquellos con y sin uno o más polimorfismos NS5A en la posición 28, 30, 31 o 93.
En sujetos infectados con genotipo 1b, los polimorfismos NS3 de referencia no afectaron la respuesta al tratamiento.
Efecto de los polimorfismos del VHC de referencia en la respuesta al tratamiento en sujetos infectados con genotipo 4
El análisis filogenético de las secuencias del VHC de sujetos infectados con genotipo 4 (n=71) en los análisis agrupados de sujetos (censurados por fallo no virológico) tratados con regímenes que contenían ZEPATIER o elbasvir + grazoprevir con o sin ribavirina en ensayos clínicos de fase 2 y 3 identificó 4 subtipos del VHC de genotipo 4 (4a, 4d, 4k, 4o). La mayoría de los sujetos estaban infectados con el subtipo 4a (42%) o 4d (51%); 1 a 2 sujetos estaban infectados con cada uno de los otros subtipos del genotipo 4. Entre los sujetos inscritos en los sitios de estudio de EE. UU., 11/13 (85%) estaban infectados con el subtipo 4a del VHC. Hubo dos sujetos infectados con el subtipo 4d del VHC que experimentaron un fallo virológico con el régimen que contenía grazoprevir y elbasvir.
En sujetos infectados con genotipo 4, las tasas de SVR12 para los sujetos con polimorfismos NS5A de referencia (cualquier cambio con respecto a la referencia en las posiciones de aminoácidos NS5A 28, 30, 31, 58 y 93 mediante secuenciación de nucleótidos de la población) fueron del 100% (28/28) y para los sujetos sin polimorfismos NS5A de referencia fueron del 95% (41/43).
En sujetos infectados con genotipo 4, las tasas de SVR12 para los sujetos con polimorfismos NS3 de referencia (cualquier cambio con respecto a la referencia en las posiciones de aminoácidos NS3 36, 54, 55, 56, 80, 107, 122, 132, 155, 156, 158, 168, 170 y 175 mediante secuenciación de nucleótidos de la población) fueron del 100% (18/18) y para los sujetos sin polimorfismos NS3 de referencia fueron del 96% (51/53).
Resistencia cruzada
La resistencia cruzada es posible entre los inhibidores de NS5A y los inhibidores de la proteasa NS3/4A por clase. Elbasvir y grazoprevir son totalmente activos contra las poblaciones virales con sustituciones que confieren resistencia a los inhibidores de NS5B.
En el ensayo C-SALVAGE, los sujetos con infección de genotipo 1 que habían fracasado en el tratamiento previo con boceprevir (n=28), simeprevir (n=8) o telaprevir (n=43) en combinación con PegIFN + RBV recibieron EBR 50 mg una vez al día + GZR 100 mg una vez al día + RBV durante 12 semanas. Hay datos limitados para determinar el impacto de las sustituciones asociadas a resistencia a NS3 del VHC detectadas en la línea de base en sujetos con experiencia en tratamiento que fallaron en la terapia previa con PegIFN + RBV + inhibidor de la proteasa del VHC y recibieron ZEPATIER con ribavirina. Se logró la SVR en el 88% (21/24) de los sujetos infectados con genotipo 1a y genotipo 1b con sustituciones asociadas a resistencia a NS3 detectadas en la línea de base. Las sustituciones específicas de NS3 observadas en la línea de base incluyeron una o más de las siguientes: V36L/M (n=8), T54S (n=4), S122G/T (n=9), R155K/T (n=9), A156S/T (n=1) y D168E/N (n=3). La SVR fue del 100% (55/55) en los sujetos sin sustituciones de resistencia a NS3 de referencia. Los 3 sujetos con fallo virológico tenían las siguientes sustituciones/polimorfismos NS3 o NS5A en la línea de base: NS3 R155T/D168N, NS3 R155K más NS5A H58D y NS3 T54S más NS5A L31M.
No se ha establecido la eficacia de ZEPATIER en pacientes que previamente han fracasado en el tratamiento con otros regímenes que incluían un inhibidor de NS5A.
13 TOXICOLOGÍA NO CLÍNICA
13.1 Carcinogenesis, Mutagenesis, Impairment of Fertility
Carcinogénesis y mutagénesis
Elbasvir y grazoprevir no mostraron genotoxicidad en una batería de ensayos in vitro o in vivo, incluyendo mutagénesis microbiana, aberración cromosómica en células de ovario de hámster chino y en ensayos de micronúcleos in vivo en ratas.
No se han realizado estudios de carcinogenicidad con elbasvir o grazoprevir.
Si ZEPATIER se administra en un régimen que contiene ribavirina, la información para ribavirina sobre carcinogénesis y mutagénesis también se aplica a este régimen combinado. Consulte la información de prescripción de ribavirina para obtener información sobre carcinogénesis y mutagénesis.
Deterioro de la fertilidad
No se observaron efectos sobre el apareamiento, la fertilidad femenina o masculina, o el desarrollo embrionario temprano en ratas hasta la dosis más alta probada. Las exposiciones sistémicas (AUC) a elbasvir y grazoprevir fueron aproximadamente 8 y 114 veces, respectivamente, la exposición en humanos a la dosis humana recomendada.
Si ZEPATIER se administra con ribavirina, la información para ribavirina sobre el deterioro de la fertilidad también se aplica a este régimen combinado. Consulte la información de prescripción de ribavirina para obtener información sobre el deterioro de la fertilidad.
14 ESTUDIOS CLÍNICOS
14.1 Descripción general de los ensayos clínicos
La eficacia de ZEPATIER se evaluó en 2 ensayos controlados con placebo y 4 ensayos clínicos de fase 2 y 3 no controlados en 1401 sujetos con genotipo (GT) 1, 4 o 6 y en 1 ensayo clínico en 22 sujetos pediátricos con infección por el virus de la hepatitis C crónica GT 1 o 4 con enfermedad hepática compensada (con o sin cirrosis). En la Tabla 13 se proporciona una descripción general de los 6 ensayos (n=1373) que contribuyen a la evaluación de la eficacia en el genotipo 1 o 4. C-EDGE TN, C-EDGE COINFECTION, C-SCAPE y C-EDGE TE también incluyeron sujetos con infección por VHC de genotipo 6 (n=28). Debido a que ZEPATIER no está indicado para la infección por el genotipo 6, los resultados en pacientes con infección por el genotipo 6 no se incluyen en los Estudios clínicos (14).
| Ensayo | Población | Grupos de estudio y duración (Número de sujetos tratados) |
|---|---|---|
| GT = Genotipo | ||
| TN = Tratamiento-Naïve | ||
| TE = Tratamiento-Experimentado (fracaso del tratamiento previo con interferón [IFN] o peginterferón alfa [PegIFN] con o sin ribavirina [RBV] o intolerancia a la terapia previa). | ||
| C-EDGE TN (doble ciego) |
GT 1, 4 TN con o sin cirrosis |
|
| C-EDGE COINFECTION (abierto) |
GT 1, 4 TN con o sin cirrosis Coinfección por VHC/VIH-1 |
|
| C-SURFER (doble ciego) |
GT 1 TN o TE con o sin cirrosis Insuficiencia renal grave, incluida la hemodiálisis |
|
| C-SCAPE (abierto) |
GT 4 TN sin cirrosis |
|
| C-EDGE TE (abierto) |
GT 1, 4 TE con o sin cirrosis con o sin coinfección por VHC/VIH-1 |
|
| C-SALVAGE (abierto) |
GT 1 TE con régimen de inhibidores de la proteasa del VHC† con o sin cirrosis |
|
| MK-5172-079 (abierto) |
GT 1, 4 Sujetos pediátricos TN o TE |
|
ZEPATIER se administró una vez al día por vía oral en estos ensayos. Para los sujetos que recibieron ribavirina (RBV), la dosis de RBV fue basada en el peso (menos de 66 kg = 800 mg al día, 66 a 80 kg = 1000 mg al día, 81 a 105 kg = 1200 mg al día, más de 105 kg = 1400 mg al día) administrada por vía oral en dos dosis divididas con alimentos.
La respuesta virológica sostenida (SVR) fue el punto final primario en todos los ensayos y se definió como ARN del VHC inferior al límite inferior de cuantificación (LLOQ) a las 12 semanas después de la interrupción del tratamiento (SVR12). Los valores de ARN del VHC sérico se midieron durante estos ensayos clínicos utilizando la prueba COBAS AmpliPrep/COBAS Taqman HCV (versión 2.0) con un LLOQ de 15 IU de ARN del VHC por mL, excepto en C-SCAPE, donde el ensayo tenía un LLOQ de 25 IU de ARN del VHC por mL.
14.2 Ensayos clínicos en sujetos no tratados previamente con genotipo 1 del VHC (C-EDGE TN y C-EDGE COINFECTION)
La eficacia de ZEPATIER en sujetos no tratados previamente con infección crónica por el virus de la hepatitis C de genotipo 1 con o sin cirrosis se demostró en los ensayos C-EDGE TN y C-EDGE COINFECTION.
C-EDGE TN fue un ensayo aleatorizado, doble ciego, controlado con placebo en sujetos no tratados previamente con infección de genotipo 1 o 4 con o sin cirrosis. Los sujetos se aleatorizaron en una proporción de 3:1 a: ZEPATIER durante 12 semanas (grupo de tratamiento inmediato) o placebo durante 12 semanas seguido de tratamiento abierto con ZEPATIER durante 12 semanas (grupo de tratamiento diferido). Entre los sujetos con infección de genotipo 1 aleatorizados al grupo de tratamiento inmediato, la edad media fue de 55 años (rango: 20 a 78); el 56% de los sujetos eran hombres; el 61% eran blancos; el 20% eran negros o afroamericanos; el 8% eran hispanos o latinos; el índice de masa corporal promedio era de 26 kg/m2; el 72% tenían niveles de ARN del VHC en el punto basal superiores a 800.000 IU por mL; el 24% tenían cirrosis; el 67% tenían alelos IL28B no C/C (CT o TT); y el 55% tenían infección crónica por VHC de genotipo 1a y el 45% tenían genotipo 1b.
C-EDGE COINFECTION fue un ensayo abierto, de un solo brazo en sujetos no tratados previamente con coinfección VHC/VIH-1 con infección de genotipo 1 o 4 con o sin cirrosis. Los sujetos recibieron ZEPATIER durante 12 semanas. Entre los sujetos con infección de genotipo 1, la edad media era de 50 años (rango: 21 a 71); el 85% de los sujetos eran hombres; el 75% eran blancos; el 19% eran negros o afroamericanos; el 6% eran hispanos o latinos; el índice de masa corporal promedio era de 25 kg/m2; el 59% tenían niveles de ARN del VHC en el punto basal superiores a 800.000 IU por mL; el 16% tenían cirrosis; el 65% tenían alelos IL28B no C/C (CT o TT); y el 76% tenían genotipo 1a, el 23% tenían genotipo 1b y el 1% tenían genotipo 1-Otro infección crónica por VHC.
Tabla 14 presenta los resultados del tratamiento de ZEPATIER en sujetos no tratados previamente con infección de genotipo 1 de C-EDGE TN (grupo de tratamiento inmediato) y C-EDGE COINFECTION. Para los resultados del tratamiento de ZEPATIER en infección de genotipo 4, [ver Estudios clínicos (14.5)].
| Ensayo | C-EDGE TN (Grupo de tratamiento inmediato) |
C-EDGE COINFECTION (Coinfección VHC/VIH-1 ) |
|---|---|---|
| Regimen | ZEPATIER 12 Semanas N=288 |
ZEPATIER 12 Semanas N=189 |
|
||
| SVR en Genotipo 1 | 95% (273/288) | 95% (179/189) |
| Resultado para sujetos sin SVR | ||
| Fallo virológico durante el tratamiento* | <1% (1/288) | 0% (0/189) |
| Recaída | 3% (10/288) | 3% (6/189) |
| Otro† | 1% (4/288) | 2% (4/189) |
| SVR por subtipos de Genotipo 1 | ||
| GT 1a‡ | 92% (144/157) | 94% (136/144) |
| GT 1b§ | 98% (129/131) | 96% (43/45) |
| SVR por estado de cirrosis | ||
| No cirrótico | 94% (207/220) | 94% (148/158) |
| Cirrótico | 97% (66/68) | 100% (31/31) |
14.3 Ensayos clínicos en sujetos con experiencia en tratamiento y genotipo 1 de VHC
Sujetos con experiencia en tratamiento que fracasaron en terapia previa con PegIFN y RBV (C-EDGE TE)
C-EDGE TE fue un ensayo comparativo aleatorizado, de etiqueta abierta, en sujetos con infección de genotipo 1 o 4, con o sin cirrosis, con o sin coinfección VHC/VIH-1, que habían fracasado en la terapia previa con PegIFN + RBV. Los sujetos fueron aleatorizados en una proporción 1:1:1:1 a uno de los siguientes grupos de tratamiento: ZEPATIER durante 12 semanas, ZEPATIER + RBV durante 12 semanas, ZEPATIER durante 16 semanas o ZEPATIER + RBV durante 16 semanas. Entre los sujetos con infección de genotipo 1, la edad mediana fue de 57 años (rango: 19 a 77); el 64% de los sujetos eran hombres; el 67% eran blancos; el 18% eran negros o afroamericanos; el 9% eran hispanos o latinos; el índice de masa corporal medio era de 28 kg/m2; el 78% tenían niveles basales de ARN del VHC mayores de 800 000 UI/mL; el 34% tenían cirrosis; el 79% tenían alelos de IL28B no C/C (CT o TT); y el 60% tenían genotipo 1a, el 39% tenían genotipo 1b y el 1% tenían genotipo 1-Otras infecciones crónicas por VHC.
Los resultados del tratamiento en sujetos de genotipo 1 tratados con ZEPATIER durante 12 semanas o ZEPATIER con RBV durante 16 semanas se presentan en Tabla 15. Los resultados del tratamiento con ZEPATIER con RBV durante 12 semanas o sin RBV durante 16 semanas no se muestran porque estos regímenes no se recomiendan en pacientes de genotipo 1 con experiencia en PegIFN/RBV. Para los resultados del tratamiento de ZEPATIER en la infección de genotipo 4, [ver Estudios clínicos (14.5)].
| Regimen | ZEPATIER 12 semanas N=96 |
ZEPATIER + RBV 16 semanas N=96 |
|---|---|---|
|
||
| SVR en genotipo 1 | 94% (90/96) | 97% (93/96) |
| Resultado para sujetos sin SVR | ||
| Fracaso virológico durante el tratamiento* | 0% (0/96) | 0% (0/96) |
| Recaída | 5% (5/96) | 0% (0/96) |
| Otro† | 1% (1/96) | 3% (3/96) |
| SVR por subtipos de genotipo 1 | ||
| GT 1a‡ | 90% (55/61) | 95% (55/58) |
| GT 1b§ | 100% (35/35) | 100% (38/38) |
| SVR por estado de cirrosis | ||
| No cirrótico | 94% (61/65) | 95% (61/64) |
| Cirrótico | 94% (29/31) | 100% (32/32) |
| SVR por respuesta al tratamiento previo contra el VHC | ||
| Fracaso virológico durante el tratamiento¶ | 90% (57/63) | 95% (58/61) |
| Recaída | 100% (33/33) | 100% (35/35) |
Sujetos con experiencia en tratamiento que fallaron en la terapia previa con PegIFN + RBV + inhibidor de la proteasa del VHC (C-SALVAGE)
C-SALVAGE fue un ensayo abierto de un solo brazo en sujetos con infección del genotipo 1, con o sin cirrosis, que habían fallado en el tratamiento previo con boceprevir, simeprevir o telaprevir en combinación con PegIFN + RBV. Los sujetos recibieron EBR 50 mg una vez al día + GZR 100 mg una vez al día + RBV durante 12 semanas. Los sujetos tenían una mediana de edad de 55 años (rango: 23 a 75); el 58% de los sujetos eran hombres; el 97% eran blancos; el 3% eran negros o afroamericanos; el 15% eran hispanos o latinos; el índice de masa corporal promedio era de 28 kg/m2; el 63% tenían niveles basales de ARN del VHC superiores a 800 000 UI/mL; el 43% tenían cirrosis; y el 97% tenían alelos IL28B no C/C (CT o TT); el 46% tenían sustituciones asociadas a la resistencia NS3 en la línea basal.
Se alcanzó una RVS global en el 96% (76/79) de los sujetos que recibieron EBR + GZR + RBV durante 12 semanas. El 4% (3/79) de los sujetos no alcanzaron la RVS debido a la recaída. Los resultados del tratamiento fueron consistentes en sujetos con genotipo 1a y genotipo 1b, en sujetos con diferentes respuestas al tratamiento previo del VHC y en sujetos con o sin cirrosis. Los resultados del tratamiento fueron generalmente consistentes en sujetos con o sin sustituciones asociadas a la resistencia NS3 en la línea basal, aunque hay datos limitados disponibles para sujetos con sustituciones asociadas a la resistencia NS3 específicas [ver Microbiología (12.4)].
14.4 Ensayo clínico en sujetos con VHC del genotipo 1 y deterioro renal grave, incluidos sujetos en hemodiálisis (C-SURFER)
C-SURFER fue un ensayo aleatorizado, doble ciego, controlado con placebo en sujetos con infección del genotipo 1, con o sin cirrosis, con enfermedad renal crónica (ERC) en estadio 4 (TFGe 15-29 mL/min/1.73 m2) o ERC en estadio 5 (TFGe <15 mL/min/1.73 m2), incluidos sujetos en hemodiálisis, que eran naïve al tratamiento o que habían fallado en el tratamiento previo con IFN o PegIFN ± RBV. Los sujetos fueron aleatorizados en una proporción 1:1 a uno de los siguientes grupos de tratamiento: EBR 50 mg una vez al día + GZR 100 mg una vez al día durante 12 semanas (grupo de tratamiento inmediato) o placebo durante 12 semanas seguido de tratamiento abierto con EBR + GZR durante 12 semanas (grupo de tratamiento diferido). Además, 11 sujetos recibieron tratamiento abierto con EBR + GZR durante 12 semanas (grupo de farmacocinética intensiva [PK]). Los sujetos aleatorizados al grupo de tratamiento inmediato y al grupo de PK intensiva tenían una mediana de edad de 58 años (rango: 31 a 76); el 75% de los sujetos eran hombres; el 50% eran blancos; el 45% eran negros o afroamericanos; el 11% eran hispanos o latinos; el 57% tenían niveles basales de ARN del VHC superiores a 800 000 UI/mL; el 6% tenían cirrosis; y el 72% tenían alelos IL28B no C/C (CT o TT).
Los resultados del tratamiento en sujetos tratados con ZEPATIER durante 12 semanas en el grupo combinado de tratamiento inmediato y el grupo de PK intensiva se presentan en Tabla 16.
| Regimen | EBR + GZR 12 semanas (Grupo de tratamiento inmediato) N=122* |
|---|---|
|
|
| RVS global | 94% (115/122)† |
| Resultado para sujetos sin RVS | |
| Fallo virológico durante el tratamiento | 0% (0/122) |
| Recaída | <1% (1/122) |
| Otros‡ | 5% (6/122) |
| RVS por genotipo | |
| GT 1a | 97% (61/63) |
| GT 1b§ | 92% (54/59) |
| RVS por estado de cirrosis | |
| No | 95% (109/115) |
| Sí | 86% (6/7) |
| RVS por estado de tratamiento previo del VHC | |
| Naïve al tratamiento | 95% (96/101) |
| Con experiencia en tratamiento | 90% (19/21) |
| RVS por estado de hemodiálisis | |
| No | 97% (29/30) |
| Sí | 93% (86/92) |
| RVS por estadio de enfermedad renal crónica | |
| Etapa 4 | 100% (22/22) |
| Etapa 5 | 93% (93/100) |
14.5 Ensayos clínicos con VHC de genotipo 4
La eficacia de ZEPATIER en sujetos con infección crónica por VHC de genotipo 4 se demostró en C-EDGE TN, C-EDGE COINFECCIÓN, C-EDGE TE y C-SCAPE. C-SCAPE fue un ensayo aleatorizado, de etiqueta abierta que incluyó sujetos no tratados previamente con infección de genotipo 4 sin cirrosis. Los sujetos fueron aleatorizados en una proporción 1:1 a EBR 50 mg una vez al día + GZR 100 mg una vez al día durante 12 semanas o EBR 50 mg una vez al día + GZR 100 mg una vez al día + RBV durante 12 semanas. En estos estudios combinados en sujetos con infección de genotipo 4, el 64% no habían recibido tratamiento previo; el 66% de los sujetos eran hombres; el 87% eran blancos; el 10% eran negros o afroamericanos; el 22% tenían cirrosis; y el 30% tenían coinfección VHC/VIH-1.
En los ensayos combinados de C-SCAPE, C-EDGE TN y C-EDGE COINFECCIÓN, un total de 66 sujetos no tratados previamente de genotipo 4 recibieron ZEPATIER o EBR + GZR durante 12 semanas. En estos ensayos combinados, la RVS12 entre los sujetos tratados con ZEPATIER o EBR + GZR durante 12 semanas fue del 97% (64/66).
En C-EDGE TE, un total de 37 sujetos con experiencia en tratamiento de genotipo 4 recibieron un régimen de ZEPATIER con o sin RBV durante 12 o 16 semanas. La RVS12 entre los sujetos aleatorizados tratados con ZEPATIER + RBV durante 16 semanas fue del 100% (8/8).
14.6 Ensayo clínico en sujetos pediátricos con infección crónica por hepatitis C de genotipo 1 o 4
La eficacia de ZEPATIER se evaluó en un estudio de etiqueta abierta (MK-5172-079, NCT03379506) que evaluó a sujetos pediátricos de 12 años a menos de 18 años que recibieron ZEPATIER durante 12 semanas. Los sujetos infectados con VHC GT1a con una o más RAS de NS5A en la línea de base fueron excluidos de la participación en el estudio. En el estudio MK-5172-079, 22 sujetos no tratados previamente o con experiencia en tratamiento de 12 años a menos de 18 años con genotipo 1 (n = 21) o 4 CHC (n = 1), sin cirrosis, fueron tratados con ZEPATIER durante 12 semanas. La edad media fue de 13,5 años (rango: 12 a 17); el 50% eran mujeres; el 95% eran blancos; el rango de peso fue de 28,1 kg a 96,5 kg; el 95,5% tenían genotipo 1 y el 4,5% tenían genotipo 4; el 64% no habían recibido tratamiento previo, el 36% tenían experiencia en tratamiento; el 46% tenían niveles de ARN de VHC en la línea de base superiores a 800.000 UI/mL. La tasa global de RVS12 fue del 100% (22/22).
16 FORMA DE SUMINISTRO/ALMACENAMIENTO Y MANIPULACIÓN
Cada tableta de ZEPATIER contiene 50 mg de elbasvir y 100 mg de grazoprevir, es de color beige, de forma ovalada, recubierta con película, con la marca “770” en un lado y lisa en el otro. Las tabletas se envasan en una caja (NDC 0006-3074-02) que contiene dos (2) paquetes de dosis a prueba de niños de 14 unidades para un total de 28 tabletas.
Almacene ZEPATIER en el blíster original hasta su uso para protegerlo de la humedad.
Almacene ZEPATIER a 20°C a 25°C (68°F a 77°F); se permiten excursiones entre 15°C a 30°C (entre 59°F a 86°F) [ver Temperatura ambiente controlada de USP].
17 INFORMACIÓN PARA EL PACIENTE
Aconseje al paciente que lea el etiquetado del paciente aprobado por la FDA (Información para el paciente).
Para los pacientes que reciben ZEPATIER con ribavirina, aconseje a los pacientes que lean el etiquetado del paciente aprobado por la FDA (Guía de medicamentos) para ribavirina [ver Advertencias y precauciones (5.4)].
Riesgo de reactivación del virus de la hepatitis B en pacientes coinfectados con VHC y VHB
Informe a los pacientes que la reactivación del VHB puede ocurrir en pacientes coinfectados con VHB durante o después del tratamiento de la infección por VHC. Aconseje a los pacientes que le digan a su proveedor de atención médica si tienen antecedentes de infección por el virus de la hepatitis B [ver Advertencias y precauciones (5.1)].
Riesgo de descompensación/insuficiencia hepática en pacientes con evidencia de enfermedad hepática avanzada
Aconseje a los pacientes que busquen evaluación médica inmediatamente por síntomas de empeoramiento de los problemas hepáticos, como náuseas, cansancio, color amarillento de la piel o la parte blanca de los ojos, sangrado o moretones más fácilmente de lo normal, confusión, pérdida de apetito, diarrea, orina oscura o marrón, heces oscuras o con sangre, hinchazón del área del estómago (abdomen) o dolor en la parte superior derecha del área del estómago, somnolencia o vómito de sangre [ver Advertencias y precauciones (5.3)].
Riesgo de elevaciones de ALT
Informe a los pacientes que deben observar las señales de advertencia temprana de inflamación hepática, como fatiga, debilidad, falta de apetito, náuseas y vómitos, así como señales posteriores como ictericia y heces descoloridas, y que consulten a su profesional de la salud sin demora si se presentan estos síntomas [ver Advertencias y precauciones (5.2) y Reacciones adversas (6.1)].
Embarazo
Aconseje a los pacientes que toman ZEPATIER con ribavirina que eviten el embarazo durante el tratamiento y dentro de los 6 meses de dejar de tomar ribavirina y que notifiquen a su proveedor de atención médica inmediatamente en caso de embarazo [ver Uso en poblaciones específicas (8.1)].
Interacciones medicamentosas
Informe a los pacientes que ZEPATIER puede interactuar con algunos medicamentos; por lo tanto, aconseje a los pacientes que informen a su proveedor de atención médica sobre el uso de cualquier medicamento recetado, de venta libre o productos herbales [ver Contraindicaciones (4), Advertencias y precauciones (5.5), y Interacciones medicamentosas (7)].
Almacenamiento
Aconseje a los pacientes que almacenen ZEPATIER en el envase original hasta su uso para protegerlo de la humedad [ver Presentación/Almacenamiento y manipulación (16)].
Administración
Aconseje a los pacientes que tomen ZEPATIER todos los días a la hora programada, con o sin alimentos. Informe a los pacientes que es importante no perderse ni omitir dosis y que tomen ZEPATIER durante el tiempo que el proveedor de atención médica lo recomiende.
SECCIÓN NO CLASIFICADA SPL
Fabricado para: Merck Sharp & Dohme LLC
Rahway, NJ 07065, USA
Información sobre patentes: www.msd.com/research/patent
Copyright © 2016-2022 Merck & Co., Inc., Rahway, NJ, USA, and its affiliates.
Todos los derechos reservados.
uspi-mk5172a-t-2205r008
INSERTO PARA EL PACIENTE
| Información para el paciente ZEPATIER® (se pronuncia “zep-ah-tir”) (elbasvir y grazoprevir) tabletas |
Lo que usted necesita saber sobre ZEPATIER
|
ZEPATIER puede causar efectos secundarios graves, entre ellos,
Reactivación del virus de la hepatitis B: antes de comenzar el tratamiento con ZEPATIER, su proveedor de atención médica le hará análisis de sangre para detectar la infección por el virus de la hepatitis B. Si alguna vez ha tenido una infección por el virus de la hepatitis B, este podría volver a activarse durante o después del tratamiento de la infección por el virus de la hepatitis C con ZEPATIER. La reactivación del virus de la hepatitis B puede causar problemas hepáticos graves, como insuficiencia hepática y la muerte. Su proveedor de atención médica lo controlará si usted corre riesgo de reactivación del virus de la hepatitis B durante el tratamiento y después de dejar de tomar ZEPATIER.
Para obtener más información sobre los efectos secundarios, consulte la sección “¿Cuáles son los posibles efectos secundarios de ZEPATIER?“
| ¿Qué es ZEPATIER®? |
ZEPATIER es un medicamento recetado que se usa con o sin ribavirina para tratar la infección crónica (de larga duración) por el virus de la hepatitis C (VHC) de genotipos 1 o 4 en adultos y niños de 12 años de edad o mayores que pesan al menos 66 libras (30 kilogramos).
ZEPATIER no debe usarse en niños menores de 12 años que pesen menos de 66 libras (30 kilogramos).
Se desconoce si ZEPATIER es seguro y eficaz en personas que están en espera de un trasplante de hígado o que se han sometido a un trasplante de hígado.
No tome ZEPATIER si tiene ciertos problemas hepáticos.
| ¿Qué debo decirle a mi proveedor de atención médica antes de tomar ZEPATIER? |
Antes de tomar ZEPATIER, informe a su proveedor de atención médica sobre todas sus afecciones médicas, incluso si:
- alguna vez ha tenido una infección por el virus de la hepatitis B
- tiene problemas hepáticos distintos de la hepatitis C
- alguna vez ha tomado algún medicamento para la hepatitis C
- tiene VIH
- se ha sometido o está en espera de un trasplante de hígado
- está embarazada o tratando de quedar embarazada. ZEPATIER no se ha estudiado en mujeres embarazadas. Se desconoce si ZEPATIER causará daño a su bebé durante el embarazo.
- Los hombres y las mujeres que toman ZEPATIER y ribavirina también deben leer la Guía del Medicamento de la ribavirina para obtener información importante sobre el embarazo, la anticoncepción y la infertilidad.
- está amamantando o planea amamantar. Se desconoce si ZEPATIER pasa a la leche materna y si esto causa daño a su bebé.
- Hable con su proveedor de atención médica sobre la mejor manera de alimentar a su bebé durante el tratamiento con ZEPATIER.
| ¿Está tomando otros medicamentos? |
Informe a su proveedor de atención médica sobre todos los medicamentos que toma, incluidos los medicamentos recetados y de venta libre, las vitaminas y los suplementos a base de hierbas. ZEPATIER puede afectar la forma en que actúan otros medicamentos, y otros medicamentos pueden afectar la forma en que actúa ZEPATIER. Algunos medicamentos no pueden tomarse con ZEPATIER. Su proveedor de atención médica puede decirle si es seguro tomar ZEPATIER con otros medicamentos.
- Conozca los medicamentos que toma. Lleve una lista de sus medicamentos y muéstresela a su proveedor de atención médica y farmacéutico cuando le receten un nuevo medicamento.
- Puede pedirle a su proveedor de atención médica o farmacéutico una lista de los medicamentos que interactúan con este medicamento.
- No comience a tomar un nuevo medicamento sin antes informarle a su proveedor de atención médica.
| ¿Cómo debo tomar ZEPATIER? |
- Tome 1 comprimido de ZEPATIER a la misma hora todos los días.
- ZEPATIER viene en un envase blíster con comprimidos envasados individualmente. Mantenga los comprimidos en este envase hasta que esté listo para tomar su dosis.
- Tome ZEPATIER exactamente como se lo indique su proveedor de atención médica.
- Tome ZEPATIER con o sin alimentos.
- No deje de tomar ZEPATIER sin antes consultar con su proveedor de atención médica.
- Si toma más de la dosis recetada, llame a su proveedor de atención médica de inmediato.
| ¿Qué sucede si olvido tomar ZEPATIER? |
- No tome dos dosis de ZEPATIER al mismo tiempo para compensar la dosis olvidada.
- Si no está seguro de qué hacer, llame a su proveedor de atención médica o farmacéutico. Es importante que no olvide ni omita dosis de ZEPATIER durante el tratamiento.
ZEPATIER puede provocar efectos secundarios graves, entre ellos:
Reactivación del virus de la hepatitis B. Consulte “¿Cuál es la información más importante que debo saber sobre ZEPATIER?“
Signos de problemas hepáticos. ZEPATIER puede causar aumentos en sus análisis de sangre relacionados con el hígado. Esto podría ser un signo de problemas hepáticos graves. Su proveedor de atención médica le hará análisis de sangre para controlar su hígado antes y durante el tratamiento con ZEPATIER. Informe a su proveedor de atención médica de inmediato si presenta alguno de los siguientes síntomas o si estos empeoran durante el tratamiento con ZEPATIER:
|
|
Los efectos secundarios comunes de ZEPATIER cuando se usa sin ribavirina incluyen:
|
|
Los efectos secundarios comunes de ZEPATIER cuando se usa con ribavirina incluyen:
|
|
Si tiene algún efecto secundario que le moleste o que no desaparezca, informe a su proveedor de atención médica.
Puede haber otros efectos secundarios de ZEPATIER que no se enumeran.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088. Para obtener más información o asesoramiento médico, llame a su médico.
| ¿Dónde debo guardar ZEPATIER? |
- Mantenga ZEPATIER en su envase original (envase blíster) hasta que esté listo para tomarlo. No saque los comprimidos del envase blíster original para guardarlos en otro recipiente, como un pastillero. Esto es importante porque los comprimidos son sensibles a la humedad. El envase está diseñado para protegerlos.
- Mantenga ZEPATIER a temperatura ambiente.
- Mantenga ZEPATIER y todos los medicamentos fuera del alcance de los niños.
| Información general sobre ZEPATIER |
- Los medicamentos a veces se recetan para fines distintos de los que se enumeran en la información para el paciente. No use ZEPATIER para una afección para la que no fue recetado. No le dé ZEPATIER a otras personas, incluso si tienen la misma afección. Podría perjudicarlos.
- Si desea obtener más información, hable con su proveedor de atención médica o farmacéutico. Puede pedirles información sobre ZEPATIER que fue escrita para profesionales de la salud.
- Para obtener más información, llame a la compañía que fabrica ZEPATIER al 1-877-888-4231 o visite www.ZEPATIER.com.
| ¿Cuáles son los ingredientes de ZEPATIER? |
Los ingredientes activos son: elbasvir y grazoprevir.
Los ingredientes inactivos son: dióxido de silicio coloidal, copovidona, croscarmelosa sódica, hipromelosa, lactosa monohidrato, estearato de magnesio, manitol, celulosa microcristalina, cloruro de sodio, lauril sulfato de sodio y vitamina E polietilenglicol succinato.
Los comprimidos están recubiertos con película, la cual contiene los siguientes ingredientes inactivos: cera de carnauba, óxido ferroso férrico, hipromelosa, óxido de hierro rojo, óxido de hierro amarillo, lactosa monohidrato, dióxido de titanio y triacetina.
Esta Información para el paciente ha sido aprobada por la Administración de Alimentos y Medicamentos de los Estados Unidos.
SECCIÓN NO CLASIFICADA SPL
Fabricado para: Merck Sharp & Dohme LLC
Rahway, NJ 07065, USA
Para información de patentes: www.msd.com/research/patent
Las marcas comerciales que se muestran en este documento son propiedad de sus respectivas empresas.
Copyright © 2016-2022 Merck & Co., Inc., Rahway, NJ, USA, y sus afiliadas.
Todos los derechos reservados.
Revisado: 05/2022
usppi-mk5172a-t-2205r005
PANEL PRINCIPAL DE PRESENTACIÓN – Envase de dosis en blíster de comprimidos de 50 mg/100 mg
NDC 0006-3074-02
Zepatier®
(elbasvir and grazoprevir) tablets
50 mg/100 mg
Rx only
28 Tabletas
Esta caja contiene un total de 28 tabletas
envasadas en 2 envases de dosis.
Cada envase de dosis contiene 14 unidades de blíster
con una tableta por unidad de blíster.


