Fabricante de medicamentos: Gilead Sciences, Inc. (Updated: 2024-03-14)
INFORMACIÓN DESTACADA DE LA PRESCRIPCIÓN
Tabla de Contenidos
INFORMACIÓN DE PRESCRIPCIÓN COMPLETA: CONTENIDOS*
ADVERTENCIA: RIESGO DE REACTIVACIÓN DEL VIRUS DE LA HEPATITIS B EN PACIENTES COINFECTADOS CON VHC Y VHB
1 INDICACIONES Y USO
2 DOSIFICACIÓN Y ADMINISTRACIÓN
2.1 Pruebas antes del inicio del tratamiento
2.2 Dosis recomendada
2.3 Insuficiencia renal
2.4 Insuficiencia hepática moderada o grave
3 FORMAS FARMACÉUTICAS Y CONCENTRACIONES
4 CONTRAINDICACIONES
5 ADVERTENCIAS Y PRECAUCIONES
5.1 Riesgo de reactivación del virus de la hepatitis B en pacientes coinfectados con VHC y VHB
5.2 Riesgo de descompensación/insuficiencia hepática en pacientes con evidencia de enfermedad hepática avanzada
5.3 Bradicardia sintomática grave cuando se coadministra con amiodarona
5.4 Riesgo de reducción del efecto terapéutico debido al uso concomitante de VOSEVI con inductores de P-gp y/o inductores moderados a fuertes de CYP
6 REACCIONES ADVERSAS
6.1 Experiencia en ensayos clínicos
6.2 Experiencia posterior a la comercialización
7 INTERACCIONES FARMACOLÓGICAS
7.1 Potencial de otros medicamentos para afectar a VOSEVI
7.2 Potencial de VOSEVI para afectar a otros medicamentos
7.3 Interacciones farmacológicas establecidas y potencialmente significativas
7.4 Medicamentos sin interacciones clínicamente significativas con VOSEVI
8 USO EN POBLACIONES ESPECÍFICAS
8.1 Embarazo
8.2 Lactancia
8.4 Uso pediátrico
8.5 Uso geriátrico
8.6 Insuficiencia renal
8.7 Insuficiencia hepática
10 SOBREDOSIS
11 DESCRIPCIÓN
12 FARMACOLOGÍA CLÍNICA
12.1 Mecanismo de acción
12.2 Farmacodinámica
12.3 Farmacocinética
12.4 Microbiología
13 TOXICOLOGÍA NO CLÍNICA
13.1 Carcinogénesis, Mutagénesis, Alteración de la fertilidad
14 ESTUDIOS CLÍNICOS
14.1 Descripción de los ensayos clínicos
14.2 Ensayos clínicos en sujetos con experiencia con AAD para el VHC
16 PRESENTACIÓN/ALMACENAMIENTO Y MANEJO
17 INFORMACIÓN PARA EL ASESORAMIENTO DEL PACIENTE
- *
- No se enumeran las secciones o subsecciones omitidas de la información de prescripción completa.
ADVERTENCIA EN RECUADRO
ADVERTENCIA: RIESGO DE REACTIVACIÓN DEL VIRUS DE LA HEPATITIS B EN PACIENTES COINFECTADOS CON VHC Y VHB
Pruebe a todos los pacientes para detectar evidencia de infección actual o previa por el virus de la hepatitis B (VHB) antes de iniciar el tratamiento con VOSEVI. Se ha notificado reactivación del VHB en pacientes coinfectados con VHC/VHB que estaban recibiendo o habían completado el tratamiento con antivirales de acción directa (AAD) contra el VHC y no recibían terapia antiviral contra el VHB. Algunos casos han resultado en hepatitis fulminante, insuficiencia hepática y muerte. Monitoree a los pacientes coinfectados con VHC/VHB para detectar brote de hepatitis o reactivación del VHB durante el tratamiento del VHC y el seguimiento posterior al tratamiento. Inicie el manejo apropiado del paciente para la infección por VHB según esté clínicamente indicado [ver Advertencias y precauciones (5.1)].
1 INDICACIONES Y USO
VOSEVI está indicado para el tratamiento de pacientes adultos con infección crónica por el virus de la hepatitis C (VHC) sin cirrosis o con cirrosis compensada (Child-Pugh A) que tienen [ver Dosificación y Administración (2.2) y Estudios Clínicos (14)]:
- infección por genotipo 1, 2, 3, 4, 5 o 6 y han sido tratados previamente con un régimen de VHC que contiene un inhibidor de NS5A.
- infección por genotipo 1a o 3 y han sido tratados previamente con un régimen de VHC que contiene sofosbuvir sin un inhibidor de NS5A.
- No se demostró un beneficio adicional de VOSEVI sobre sofosbuvir/velpatasvir en adultos con infección por genotipo 1b, 2, 4, 5 o 6 previamente tratados con sofosbuvir sin un inhibidor de NS5A.
2 DOSIFICACIÓN Y ADMINISTRACIÓN
2.1 Análisis previos al inicio del tratamiento
Analizar en todos los pacientes la evidencia de infección por VHB actual o previa mediante la medición del antígeno de superficie de la hepatitis B (AgsHB) y el anticuerpo contra la proteína central de la hepatitis B (anti-HBc) antes de iniciar el tratamiento del VHC con VOSEVI [ver Advertencias y precauciones (5.1)].
2.2 Dosificación recomendada
La dosificación recomendada de VOSEVI es una tableta, tomada por vía oral, una vez al día con alimentos [ver Farmacología clínica (12.3)]. Una tableta de VOSEVI contiene 400 mg de sofosbuvir, 100 mg de velpatasvir y 100 mg de voxilaprevir. La Tabla 1 muestra el régimen de tratamiento recomendado y la duración según la población de pacientes.
| Genotipo | Pacientes tratados previamente con un régimen de VHC que contiene: | Duración de VOSEVI |
|---|---|---|
|
||
| 1, 2, 3, 4, 5 o 6 | Un inhibidor de la NS5A* | 12 semanas |
| 1a o 3 | Sofosbuvir sin un inhibidor de la NS5A† | 12 semanas |
2.3 Insuficiencia renal
No se recomienda ajuste de la dosificación de VOSEVI en pacientes con cualquier grado de insuficiencia renal, incluidos los pacientes en diálisis [ver Uso en poblaciones específicas (8.6) y Farmacología clínica (12.3)].
2.4 Insuficiencia hepática moderada o grave
No se recomienda VOSEVI en pacientes con insuficiencia hepática moderada o grave (Child-Pugh B o C) debido a las mayores exposiciones de voxilaprevir en estos pacientes [ver Advertencias y precauciones (5.2), Uso en poblaciones específicas (8.7) y Farmacología clínica (12.3)].
3 FORMAS POSOLÓGICAS Y CONCENTRACIONES
Cada tableta de VOSEVI contiene 400 mg de sofosbuvir, 100 mg de velpatasvir y 100 mg de voxilaprevir. Las tabletas son beige, con forma de cápsula, recubiertas con película y grabadas con “GSI” en un lado y “ ” en el otro lado.
” en el otro lado.
4 CONTRAINDICACIONES
VOSEVI está contraindicado con rifampicina [ver Interacciones farmacológicas (7.3), y Farmacología clínica (12.3)].
5 ADVERTENCIAS Y PRECAUCIONES
5.1 Riesgo de reactivación del virus de la hepatitis B en pacientes coinfectados con VHC y VHB
Se ha reportado la reactivación del virus de la hepatitis B (VHB) en pacientes coinfectados con VHC/VHB que estaban recibiendo o habían completado el tratamiento con antivirales de acción directa contra el VHC y que no estaban recibiendo terapia antiviral contra el VHB. Algunos casos han resultado en hepatitis fulminante, insuficiencia hepática y muerte. Se han reportado casos en pacientes que son HBsAg positivos y también en pacientes con evidencia serológica de infección resuelta por VHB (es decir, HBsAg negativo y anti-HBc positivo). También se ha reportado la reactivación del VHB en pacientes que reciben ciertos agentes inmunosupresores o quimioterapéuticos; el riesgo de reactivación del VHB asociado con el tratamiento con antivirales de acción directa contra el VHC puede aumentar en estos pacientes.
La reactivación del VHB se caracteriza como un aumento abrupto en la replicación del VHB que se manifiesta como un rápido aumento en el nivel sérico de ADN del VHB. En pacientes con infección resuelta por VHB, puede ocurrir la reaparición de HBsAg. La reactivación de la replicación del VHB puede ir acompañada de hepatitis, es decir, aumentos en los niveles de aminotransferasas y, en casos graves, aumentos en los niveles de bilirrubina, insuficiencia hepática y puede ocurrir la muerte.
Analice a todos los pacientes para detectar evidencia de infección actual o previa por VHB mediante la medición de HBsAg y anti-HBc antes de iniciar el tratamiento del VHC con VOSEVI. En pacientes con evidencia serológica de infección por VHB, monitoree las señales clínicas y de laboratorio de brote de hepatitis o reactivación del VHB durante el tratamiento del VHC con VOSEVI y durante el seguimiento posterior al tratamiento. Inicie el manejo adecuado del paciente para la infección por VHB según esté clínicamente indicado.
5.2 Riesgo de descompensación/insuficiencia hepática en pacientes con evidencia de enfermedad hepática avanzada
Se han reportado casos postcomercialización de descompensación/insuficiencia hepática, incluyendo aquellos con desenlaces fatales, en pacientes tratados con regímenes que contienen inhibidores de la proteasa NS3/4A del VHC, incluido el tratamiento con VOSEVI. Los casos reportados ocurrieron en pacientes con cirrosis basal con y sin insuficiencia hepática moderada o grave (Child-Pugh B o C). Debido a que estos eventos se reportan voluntariamente en una población de tamaño incierto, no siempre es posible estimar de manera confiable su frecuencia o establecer una relación causal con la exposición al medicamento.
En pacientes con cirrosis compensada (Child-Pugh A) o evidencia de enfermedad hepática avanzada, como hipertensión portal, realice pruebas de laboratorio hepáticas según esté clínicamente indicado; y monitoree las señales y síntomas de descompensación hepática, como la presencia de ictericia, ascitis, encefalopatía hepática y hemorragia varicosa. Suspenda VOSEVI en pacientes que desarrollen evidencia de descompensación/insuficiencia hepática.
VOSEVI no se recomienda en pacientes con insuficiencia hepática moderada a grave (Child-Pugh B o C) o aquellos con cualquier historial previo de descompensación hepática [ver Dosificación y administración (2.4), Reacciones adversas (6.2), Uso en poblaciones específicas (8.7) y Farmacología clínica (12.3)].
5.3 Bradicardia sintomática grave cuando se coadministra con amiodarona
Se han reportado casos postcomercialización de bradicardia sintomática y casos que requirieron intervención con marcapasos cuando se coadministra amiodarona con un régimen que contiene sofosbuvir. Se reportó un paro cardíaco fatal en un paciente que tomaba amiodarona y al que se le coadministró un régimen que contiene sofosbuvir (HARVONI® (ledipasvir/sofosbuvir)). La bradicardia generalmente ha ocurrido dentro de horas a días, pero se han observado casos hasta 2 semanas después de iniciar el tratamiento del VHC. Los pacientes que también toman bloqueadores beta, o aquellos con comorbilidades cardíacas subyacentes y/o enfermedad hepática avanzada pueden tener un mayor riesgo de bradicardia sintomática con la coadministración de amiodarona. La bradicardia generalmente se resolvió después de suspender el tratamiento del VHC. El mecanismo de este efecto es desconocido.
No se recomienda la coadministración de amiodarona con VOSEVI. Para los pacientes que toman amiodarona y no tienen otras opciones de tratamiento viables y a los que se les coadministrará VOSEVI:
- Aconseje a los pacientes sobre el riesgo de bradicardia sintomática.
- Se recomienda el monitoreo cardíaco en un entorno hospitalario durante las primeras 48 horas de coadministración, después de lo cual se debe realizar un monitoreo ambulatorio o automonitoreo de la frecuencia cardíaca diariamente durante al menos las 2 primeras semanas de tratamiento.
Los pacientes que están tomando VOSEVI y necesitan comenzar terapia con amiodarona debido a que no hay otras opciones de tratamiento viables, deben someterse a un monitoreo cardíaco similar al descrito anteriormente.
Debido a la larga vida media de la amiodarona, los pacientes que suspenden la amiodarona justo antes de comenzar VOSEVI también deben someterse a un monitoreo cardíaco similar al descrito anteriormente.
Los pacientes que desarrollen signos o síntomas de bradicardia deben buscar evaluación médica de inmediato. Los síntomas pueden incluir casi desmayarse o desmayarse, mareos o vértigo, malestar, debilidad, cansancio excesivo, dificultad para respirar, dolores en el pecho, confusión o problemas de memoria [ver Reacciones adversas (6.2) y Interacciones farmacológicas (7.3)].
5.4 Riesgo de efecto terapéutico reducido debido al uso concomitante de VOSEVI con inductores de P-gp y/o inductores moderados a potentes de CYP
Los medicamentos que son inductores de P-gp y/o inductores moderados a potentes de CYP2B6, CYP2C8 o CYP3A4 (p. ej., hierba de San Juan, carbamazepina) pueden disminuir significativamente las concentraciones plasmáticas de sofosbuvir, velpatasvir y/o voxilaprevir, lo que puede llevar a un efecto terapéutico potencialmente reducido de VOSEVI. No se recomienda el uso de estos agentes con VOSEVI [ver Interacciones farmacológicas (7.3)].
6 REACCIONES ADVERSAS
Las siguientes reacciones adversas graves se describen a continuación y en otras partes del etiquetado:
- Bradicardia sintomática grave cuando se coadministra con amiodarona [ver Advertencias y precauciones (5.3)].
6.1 Experiencia de ensayos clínicos
Debido a que los ensayos clínicos se realizan en condiciones muy variables, las tasas de reacción adversa observadas en los ensayos clínicos de un medicamento no se pueden comparar directamente con las tasas de los ensayos clínicos de otro medicamento y pueden no reflejar las tasas observadas en la práctica.
Reacciones adversas en sujetos infectados por VHC sin cirrosis o con cirrosis compensada
Los datos de reacciones adversas de VOSEVI se derivaron de dos ensayos clínicos de Fase 3 (POLARIS-1 y POLARIS-4) que evaluaron un total de 445 sujetos infectados con VHC genotipo 1, 2, 3, 4, 5 o 6, sin cirrosis o con cirrosis compensada (Child-Pugh A), que recibieron VOSEVI durante 12 semanas. VOSEVI se estudió en ensayos controlados con placebo y activo (sofosbuvir/velpatasvir) [ver Estudios clínicos (14.1 y 14.2)].
La proporción de sujetos que interrumpieron permanentemente el tratamiento debido a eventos adversos fue del 0,2% para los sujetos que recibieron VOSEVI durante 12 semanas.
Las reacciones adversas más comunes (eventos adversos evaluados como relacionados causalmente por el investigador y al menos 10%) fueron cefalea, fatiga, diarrea y náuseas en sujetos tratados con VOSEVI durante 12 semanas.
La Tabla 2 enumera las reacciones adversas (eventos adversos evaluados como relacionados causalmente por el investigador, todos los grados) observadas en al menos el 5% de los sujetos que recibieron 12 semanas de tratamiento con VOSEVI en los ensayos clínicos de Fase 3. La tabulación lateral por lado simplifica la presentación; no se deben hacer comparaciones directas entre ensayos debido a los diferentes diseños.
| POLARIS-1 | POLARIS-4 | |||
|---|---|---|---|---|
| VOSEVI 12 semanas (N=263) |
Placebo 12 semanas (N=152) |
VOSEVI 12 semanas (N=182) |
SOF/VEL 12 semanas (N=151) |
|
| Cefalea | 21% | 14% | 23% | 23% |
| Fatiga | 17% | 15% | 19% | 23% |
| Diarrea | 13% | 9% | 14% | 3% |
| Náuseas | 13% | 7% | 10% | 3% |
| Astenia | 6% | 4% | 4% | 6% |
| Insomnio | 6% | 3% | 3% | 1% |
En POLARIS-1, de los sujetos que recibieron VOSEVI que experimentaron reacciones adversas, el 99% fueron de leves a moderadas (Grado 1 o 2) en gravedad. En POLARIS-4, de los sujetos que recibieron VOSEVI que experimentaron reacciones adversas, todas las reacciones adversas reportadas fueron leves o moderadas (Grado 1 o 2) en gravedad.
Reacciones adversas menos comunes reportadas en ensayos clínicos
Las siguientes reacciones adversas ocurrieron en menos del 5% de los sujetos sin cirrosis o con cirrosis compensada tratados con VOSEVI durante 12 semanas y se incluyen debido a una posible relación causal.
Erupción cutánea: En los ensayos POLARIS-1 y POLARIS-4, la erupción cutánea ocurrió en menos del 1% y 2% de los sujetos tratados con VOSEVI, respectivamente. La erupción cutánea se reportó en el 1% de los sujetos tratados con placebo en POLARIS-1 y no fue reportada por ningún sujeto que tomó sofosbuvir/velpatasvir en POLARIS-4. No ocurrieron reacciones adversas graves de erupción cutánea y todas las erupciones fueron leves o moderadas en gravedad.
Depresión: En los ensayos POLARIS-1 y POLARIS-4, el estado de ánimo deprimido ocurrió en menos del 1% y 1% de los sujetos tratados con VOSEVI, respectivamente. El estado de ánimo deprimido no fue reportado por ningún sujeto que tomó placebo en POLARIS-1 y se reportó en el 1% de los sujetos tratados con sofosbuvir/velpatasvir en POLARIS-4. No ocurrieron reacciones adversas graves de estado de ánimo deprimido y todos los eventos fueron leves o moderados en gravedad.
Anormalidades de laboratorio
Elevaciones de lipasa: Se observaron elevaciones aisladas asintomáticas de lipasa mayores de 3×LSN en POLARIS-1 en el 2% de los sujetos tratados con VOSEVI y el 3% de los sujetos tratados con placebo, y en POLARIS-4 en el 2% de los sujetos tratados con VOSEVI y menos del 1% de los sujetos tratados con sofosbuvir/velpatasvir.
Creatina quinasa: En POLARIS-1 se informaron elevaciones aisladas asintomáticas de la creatina quinasa mayores o iguales a 10×LSN en el 1% de los sujetos tratados con VOSEVI y en el 1% de los sujetos tratados con placebo, y en POLARIS-4 en menos del 1% de los sujetos tratados con VOSEVI y ningún sujeto tratado con sofosbuvir/velpatasvir.
Bilirrubina total: Se observaron aumentos en la bilirrubina total menores o iguales a 1.5×LSN en sujetos tratados con VOSEVI debido a la inhibición de OATP1B1 y OATP1B3 por voxilaprevir: 4% y 6% de los sujetos sin cirrosis en POLARIS-1 y POLARIS-4, respectivamente; y 7% y 13% de los sujetos con cirrosis compensada en POLARIS-1 y POLARIS-4, respectivamente. Ningún sujeto experimentó ictericia y los niveles de bilirrubina total disminuyeron después de completar el tratamiento con VOSEVI.
6.2 Experiencia posterior a la comercialización
Las siguientes reacciones adversas han sido identificadas durante el uso posterior a la aprobación de regímenes que contienen sofosbuvir. Debido a que las reacciones posteriores a la comercialización se informan voluntariamente en una población de tamaño incierto, no siempre es posible estimar de manera confiable su frecuencia o establecer una relación causal con la exposición al medicamento.
Trastornos hepatobiliares
Descompensación hepática, insuficiencia hepática con regímenes que contienen inhibidores de la proteasa NS3/4A [ver Advertencias y precauciones (5.2)].
Trastornos cardíacos
Se ha reportado bradicardia sintomática grave en pacientes que toman amiodarona y que iniciaron tratamiento con un régimen que contiene sofosbuvir [ver Advertencias y precauciones (5.3) y Interacciones farmacológicas (7.3)].
7 INTERACCIONES FARMACOLÓGICAS
7.1 Potencial de otros medicamentos para afectar a VOSEVI
Sofosbuvir, velpatasvir y voxilaprevir son sustratos de los transportadores de fármacos P-gp y BCRP, mientras que GS-331007 (metabolito circulante predominante de sofosbuvir) no lo es. Voxilaprevir también es sustrato de OATP1B1 y OATP1B3. In vitro, se observó un lento metabolismo de velpatasvir por CYP2B6, CYP2C8 y CYP3A4 y de voxilaprevir por CYP1A2, CYP2C8 y principalmente CYP3A4.
Los medicamentos que son inductores de P-gp y/o inductores moderados o potentes de CYP2B6, CYP2C8 o CYP3A4 (p. ej., hierba de San Juan, carbamazepina) pueden disminuir significativamente las concentraciones plasmáticas de sofosbuvir, velpatasvir y/o voxilaprevir, lo que conduce a una reducción del efecto terapéutico de VOSEVI. No se recomienda el uso de estos agentes con VOSEVI [ver Advertencias y Precauciones (5.4) y Farmacología Clínica (12.3)]. VOSEVI puede coadministrarse con inhibidores de P-gp, BCRP y CYP. No se recomienda el uso de inhibidores de OATP que puedan aumentar sustancialmente la exposición a voxilaprevir (p. ej., ciclosporina) con VOSEVI [ver Farmacología Clínica (12.3)].
7.2 Potencial de VOSEVI para afectar a otros medicamentos
Velpatasvir y voxilaprevir son inhibidores de los transportadores de fármacos P-gp, BCRP, OATP1B1 y OATP1B3. Velpatasvir también es un inhibidor de OATP2B1. La coadministración de VOSEVI con medicamentos que son sustratos de estos transportadores puede alterar la exposición de tales medicamentos. No se recomienda la coadministración de VOSEVI con sustratos de BCRP (p. ej., metotrexato, mitoxantrona, imatinib, irinotecan, lapatinib, rosuvastatina, sulfasalazina, topotecán) [ver Farmacología Clínica (12.3)].
7.3 Interacciones farmacológicas establecidas y potencialmente significativas
La eliminación de la infección por VHC con antivirales de acción directa puede llevar a cambios en la función hepática, lo que puede afectar al uso seguro y eficaz de los medicamentos concomitantes. Por ejemplo, se han notificado casos de alteración del control de la glucosa en sangre que han dado lugar a hipoglucemia sintomática grave en pacientes diabéticos en informes de casos poscomercialización y estudios epidemiológicos publicados. El manejo de la hipoglucemia en estos casos requirió la interrupción o modificación de la dosis de los medicamentos concomitantes utilizados para el tratamiento de la diabetes.
Se recomienda un monitoreo frecuente de los parámetros de laboratorio relevantes (p. ej., Relación Normalizada Internacional [INR] en pacientes que toman warfarina, niveles de glucosa en sangre en pacientes diabéticos) o concentraciones de medicamentos concomitantes como sustratos del citocromo P450 con un índice terapéutico estrecho (p. ej., ciertos inmunosupresores) para garantizar un uso seguro y eficaz. Puede ser necesario ajustar las dosis de los medicamentos concomitantes.
La Tabla 3 proporciona una lista de interacciones farmacológicas establecidas o potencialmente significativas desde el punto de vista clínico. Las interacciones farmacológicas descritas se basan en estudios realizados con VOSEVI, los componentes de VOSEVI (sofosbuvir, velpatasvir y/o voxilaprevir), o son interacciones farmacológicas predichas que pueden ocurrir con VOSEVI [ver Contraindicaciones (4), Advertencias y Precauciones (5.3, 5.4), y Farmacología Clínica (12.3)].
| Clase de fármaco concomitante: Nombre del fármaco | Efecto sobre la concentración† | Efecto clínico/Recomendación |
|---|---|---|
| Agentes reductores de ácido: | ↓ velpatasvir | La solubilidad de velpatasvir disminuye a medida que aumenta el pH. Se espera que los fármacos que aumentan el pH gástrico disminuyan la concentración de velpatasvir. |
| Antiácidos (p. ej., hidróxido de aluminio y magnesio) | Separe la administración de antiácidos y VOSEVI por 4 horas. | |
| Antagonistas de los receptores H2 (p. ej., famotidina)‡ | Los antagonistas de los receptores H2 se pueden administrar simultáneamente o separados de VOSEVI a una dosis que no exceda las dosis comparables con famotidina 40 mg dos veces al día. | |
| Inhibidores de la bomba de protones (p. ej., omeprazol)‡ | Se puede administrar omeprazol 20 mg con VOSEVI. No se ha estudiado el uso con otros inhibidores de la bomba de protones. | |
| Antiarrítmicos: | ||
| amiodarona | Efecto sobre las concentraciones de amiodarona, sofosbuvir, velpatasvir y voxilaprevir desconocido | La coadministración de amiodarona con VOSEVI puede resultar en bradicardia sintomática grave. Se desconoce el mecanismo de este efecto. No se recomienda la coadministración de amiodarona con VOSEVI; si la coadministración es necesaria, se recomienda monitorización cardíaca [ver Advertencias y precauciones (5.3)]. |
| digoxina‡ | ↑ digoxina | Se recomienda monitorizar la concentración terapéutica de digoxina cuando se coadministra con VOSEVI. Consultar la información de prescripción de digoxina para recomendaciones de monitorización y modificación de dosis para aumentos de concentración de magnitud incierta. |
| Anticoagulantes: | ||
| dabigatrán etexilato‡ | ↑ dabigatrán | Se recomienda monitorización clínica de dabigatrán cuando se coadministra con VOSEVI. Consultar la información de prescripción de dabigatrán etexilato para recomendaciones de modificación de dosis en caso de insuficiencia renal moderada. |
| Anticonvulsivantes: | ||
| carbamazepina‡ fenitoína fenobarbital |
↓ sofosbuvir ↓ velpatasvir ↓ voxilaprevir |
No se recomienda la coadministración. |
| Antimicobacterianos: | ||
| rifampicina‡ | ↓ sofosbuvir ↓ velpatasvir ↑ voxilaprevir (dosis única) ↓ voxilaprevir (dosis múltiple) |
La coadministración con rifampicina está contraindicada [ver Contraindicaciones (4)]. |
| rifabutina‡ rifapentina |
↓ sofosbuvir ↓ velpatasvir ↓ voxilaprevir |
No se recomienda la coadministración. |
| Antirretrovirales: | ||
| atazanavir‡ lopinavir |
↑ voxilaprevir | No se recomienda la coadministración de VOSEVI con regímenes que contienen atazanavir o lopinavir. |
| tipranavir/ritonavir | ↓ sofosbuvir ↓ velpatasvir |
No se recomienda la coadministración. El efecto sobre voxilaprevir es desconocido. |
| efavirenz‡ | ↓ velpatasvir ↓ voxilaprevir |
No se recomienda la coadministración de VOSEVI con regímenes que contienen efavirenz. |
| tenofovir disoproxil fumarato (tenofovir DF)‡ | ↑ tenofovir | Monitorizar las reacciones adversas asociadas a tenofovir en pacientes que reciben VOSEVI concomitantemente con un régimen que contiene tenofovir DF. Consultar la información de prescripción del producto que contiene tenofovir DF para recomendaciones sobre monitorización renal. |
| Suplementos herbales: | ||
| Hierba de San Juan | ↓ sofosbuvir ↓ velpatasvir ↓ voxilaprevir |
No se recomienda la coadministración. |
| Inhibidores de la HMG-CoA reductasa:> | ||
| pravastatina‡ | ↑ pravastatina | La administración concomitante de VOSEVI con pravastatina ha demostrado aumentar la concentración de pravastatina, lo que se asocia con un mayor riesgo de miopatía, incluyendo rabdomiólisis. La pravastatina puede administrarse con VOSEVI a una dosis que no exceda los 40 mg de pravastatina. |
| rosuvastatina‡ | ↑ rosuvastatina | La administración concomitante de VOSEVI con rosuvastatina puede aumentar significativamente la concentración de rosuvastatina, lo que se asocia con un mayor riesgo de miopatía, incluyendo rabdomiólisis. No se recomienda la administración concomitante de VOSEVI con rosuvastatina. |
| pitavastatina | ↑ pitavastatina | La administración concomitante con VOSEVI puede aumentar la concentración de pitavastatina y no se recomienda, debido a un mayor riesgo de miopatía, incluyendo rabdomiólisis. |
| atorvastatina‡ fluvastatina lovastatina simvastatina |
↑ atorvastatina ↑ fluvastatina ↑ lovastatina ↑ simvastatina |
La administración concomitante con VOSEVI puede aumentar las concentraciones de atorvastatina, fluvastatina, lovastatina y simvastatina. El aumento de las concentraciones de estatinas puede incrementar el riesgo de miopatía, incluyendo rabdomiólisis. Utilizar la dosis más baja aprobada de estatina. Si se necesitan dosis más altas, utilizar la dosis más baja necesaria de estatina en base a una evaluación de riesgo/beneficio. |
| Inmunosupresores: | ||
| ciclosporina‡ | ↑ voxilaprevir | Se ha demostrado que la administración concomitante de voxilaprevir con ciclosporina aumenta sustancialmente la concentración plasmática de voxilaprevir, cuya seguridad no ha sido establecida. No se recomienda la administración concomitante de VOSEVI con ciclosporina. |
7.4 Medicamentos sin interacciones clínicamente significativas con VOSEVI
Según los estudios de interacción farmacológica realizados con los componentes de VOSEVI (sofosbuvir, velpatasvir y/o voxilaprevir) o VOSEVI, no se han observado interacciones clínicamente significativas con los siguientes medicamentos [ver Farmacología Clínica (12.3)]:
- VOSEVI: cobicistat, darunavir, elvitegravir, emtricitabina, etinilestradiol/norgestimato, gemfibrozilo, rilpivirina, ritonavir, tenofovir alafenamida, voriconazol
- Sofosbuvir/velpatasvir: dolutegravir, ketoconazol, raltegravir
- Sofosbuvir: metadona, tacrolimus
8 USO EN POBLACIONES ESPECÍFICAS
8.1 Embarazo
Resumen de riesgos
No hay datos humanos adecuados disponibles para establecer si VOSEVI representa o no un riesgo para los resultados del embarazo. En estudios de reproducción en animales, no se observó evidencia de resultados adversos del desarrollo con los componentes de VOSEVI (sofosbuvir, velpatasvir o voxilaprevir) con exposiciones mayores que las observadas en humanos con la dosis recomendada en humanos (RHD) [ver Datos]. Durante la organogénesis en el ratón, la rata y el conejo, las exposiciones sistémicas (AUC) de velpatasvir fueron aproximadamente 23 (ratones), 4 (ratas) y 0,5 (conejos) veces la exposición en humanos con la RHD, mientras que las exposiciones de voxilaprevir fueron aproximadamente 141 (ratas) y 4 (conejos) veces la exposición en humanos con la RHD. Las exposiciones del metabolito circulante predominante de sofosbuvir (GS-331007) fueron aproximadamente 6 (ratas) y 16 (conejos) veces la exposición en humanos con la RHD. En los estudios de desarrollo pre/postnatal en ratas, las exposiciones sistémicas maternas (AUC) de cada componente de VOSEVI fueron aproximadamente 7 (metabolito de sofosbuvir GS-331007), 3 (velpatasvir) y 238 (voxilaprevir) veces la exposición en humanos con la RHD.
El riesgo base de defectos congénitos mayores y aborto espontáneo para la población indicada es desconocido. En la población general de los EE.UU., el riesgo base estimado de defectos congénitos mayores y aborto espontáneo en embarazos clínicamente reconocidos es de 2-4% y 15-20%, respectivamente.
Datos
Sofosbuvir: El sofosbuvir se administró por vía oral a ratas preñadas (hasta 500 mg/kg/día) y conejas (hasta 300 mg/kg/día) en los días de gestación 6 a 18 y 6 a 19, respectivamente, y también a ratas (dosis orales de hasta 500 mg/kg/día) desde el día de gestación 6 hasta el día de lactancia/post-parto 20. No se observaron efectos significativos en el desarrollo embrionario-fetal (ratas y conejos) o pre/postnatal (ratas) con las dosis más altas probadas. Las exposiciones sistémicas (AUC) del metabolito circulante predominante de sofosbuvir (GS-331007) durante la gestación fueron aproximadamente 6 (ratas) y 16 (conejos) veces la exposición en humanos con la RHD.
Velpatasvir: El velpatasvir se administró por vía oral a ratones preñados (hasta 1000 mg/kg/día), ratas (hasta 200 mg/kg/día) y conejas (hasta 300 mg/kg/día) desde los días de gestación 6 a 15, 6 a 17 y 7 a 20, respectivamente, y también a ratas (dosis orales de hasta 200 mg/kg) en el día de gestación 6 hasta el día de lactancia/post-parto 20. No se observaron efectos significativos en el desarrollo embrionario-fetal (ratones, ratas y conejos) o pre/postnatal (ratas) con las dosis más altas probadas. Las exposiciones sistémicas (AUC) de velpatasvir durante la gestación fueron aproximadamente 23 (ratones), 4 (ratas) y 0,5 (conejos) veces la exposición en humanos con la RHD.
Voxilaprevir: El voxilaprevir se administró por vía oral a ratas preñadas (hasta 100 mg/kg/día) y conejas (hasta 600 mg/kg/día) desde los días de gestación 6 a 17 y 7 a 19, respectivamente, y también a ratas (dosis orales de hasta 100 mg/kg) en el día de gestación 6 hasta el día de lactancia/post-parto 20. No se observaron efectos significativos en el desarrollo embrionario-fetal (ratas y conejos) o pre/postnatal (ratas) con las dosis más altas probadas. Las exposiciones sistémicas (AUC) de voxilaprevir durante la gestación fueron aproximadamente 141 (ratas) y 4 (conejos) veces la exposición en humanos con la RHD.
8.2 Lactancia
Resumen de riesgos
No se sabe si los componentes de VOSEVI y sus metabolitos están presentes en la leche materna humana, afectan a la producción de leche materna o tienen efectos sobre el lactante amamantado. Cuando los componentes de VOSEVI se administraron a ratas lactantes, se detectó GS-331007 (el metabolito circulante predominante de sofosbuvir) y velpatasvir en la leche, mientras que se detectó voxilaprevir en el plasma de las crías lactantes probablemente debido a la presencia de voxilaprevir en la leche. No se observaron efectos significativos de ninguno de los medicamentos en las crías de ratas lactantes [ver Datos].
Se deben considerar los beneficios del desarrollo y de la salud de la lactancia materna junto con la necesidad clínica de VOSEVI de la madre y cualquier posible efecto adverso sobre el niño lactante por VOSEVI o por la condición materna subyacente.
Datos
Sofosbuvir: No se observaron efectos significativos del sofosbuvir en el crecimiento o desarrollo postnatal de las crías lactantes con la dosis más alta probada en ratas. La exposición sistémica materna (AUC) del metabolito circulante predominante de sofosbuvir (GS-331007) fue aproximadamente 7 veces la exposición en humanos con la RHD, con una exposición de aproximadamente 2% de la exposición materna observada en crías lactantes el día 10 de lactancia. En un estudio de lactancia, los metabolitos de sofosbuvir (principalmente GS-331007) se excretaron en la leche de ratas lactantes tras la administración de una dosis oral única de sofosbuvir (20 mg/kg) el día 2 de lactancia, con concentraciones de leche de aproximadamente 10% de las concentraciones plasmáticas maternas observadas 1 hora después de la dosis.
Velpatasvir: No se observaron efectos significativos del velpatasvir en el crecimiento o desarrollo postnatal de las crías lactantes con la dosis más alta probada en ratas. La exposición sistémica materna (AUC) de velpatasvir fue aproximadamente 3 veces la exposición en humanos con la RHD. El velpatasvir estuvo presente en la leche (aproximadamente 173% de las concentraciones plasmáticas maternas) de ratas lactantes tras una dosis oral única de velpatasvir (30 mg/kg), y la exposición sistémica (AUC) en crías lactantes fue aproximadamente 4% de la exposición materna el día 10 de lactancia.
Voxilaprevir: No se observaron efectos significativos del voxilaprevir en el crecimiento o desarrollo postnatal de las crías lactantes con la dosis más alta probada en ratas. La exposición sistémica materna (AUC) de voxilaprevir fue aproximadamente 238 veces la exposición en humanos con la RHD, con una exposición de aproximadamente 58% de la exposición materna observada en crías lactantes el día 10 de lactancia.
8.4 Uso pediátrico
La seguridad y eficacia de VOSEVI no se han establecido en pacientes pediátricos.
8.5 Uso geriátrico
Los ensayos clínicos de VOSEVI incluyeron 74 sujetos de 65 años o más (17% del número total de sujetos en los ensayos clínicos de Fase 3 POLARIS-1 y POLARIS-4). No se observaron diferencias generales en la seguridad o eficacia entre estos sujetos y sujetos más jóvenes, y otra experiencia clínica reportada no ha identificado diferencias en las respuestas entre los ancianos y los pacientes más jóvenes, pero no se puede descartar una mayor sensibilidad de algunos individuos mayores. No se requiere ajuste de dosis de VOSEVI en pacientes geriátricos [ver Farmacología Clínica (12.3)].
8.6 Insuficiencia renal
No se recomienda ajuste de dosis de VOSEVI para pacientes con insuficiencia renal leve, moderada o grave, incluyendo enfermedad renal en etapa terminal que requiere diálisis [ver Dosificación y Administración (2.3) y Farmacología Clínica (12.3)].
8.7 Insuficiencia hepática
No se recomienda ajuste de dosis de VOSEVI para pacientes con insuficiencia hepática leve (Child-Pugh A). VOSEVI no se recomienda en pacientes con insuficiencia hepática moderada o grave (Child-Pugh B o C) debido a las exposiciones más altas de voxilaprevir (hasta 6 veces en sujetos no infectados por VHC); la seguridad y eficacia no se han establecido en pacientes infectados por VHC con insuficiencia hepática moderada o grave [ver Dosificación y Administración (2.4) y Farmacología Clínica (12.3)]. Se han reportado casos postcomercialización de descompensación/insuficiencia hepática en estos pacientes [ver Advertencias y Precauciones (5.2)].
10 SOBREDOSIS
No existe un antídoto específico para la sobredosis con VOSEVI. Si ocurre una sobredosis, se debe monitorear al paciente para detectar signos de toxicidad. El tratamiento de la sobredosis con VOSEVI consiste en medidas de apoyo generales, como el monitoreo de los signos vitales y la observación del estado clínico del paciente. La hemodiálisis puede eliminar eficientemente el metabolito circulante predominante de sofosbuvir, GS-331007, con una tasa de extracción del 53%. Es poco probable que la hemodiálisis resulte en una eliminación significativa de velpatasvir o voxilaprevir, ya que velpatasvir y voxilaprevir se unen en gran medida a las proteínas plasmáticas.
11 DESCRIPCIÓN
VOSEVI es una tableta de combinación de dosis fija que contiene sofosbuvir, velpatasvir y voxilaprevir para administración oral. Sofosbuvir es un inhibidor análogo de nucleótidos de la polimerasa NS5B del VHC, velpatasvir es un inhibidor de NS5A y voxilaprevir es un inhibidor de la proteasa NS3/4A.
Cada tableta contiene 400 mg de sofosbuvir, 100 mg de velpatasvir y 100 mg de voxilaprevir. Las tabletas incluyen los siguientes ingredientes inactivos: dióxido de silicio coloidal, copovidona, croscarmelosa sódica, lactosa monohidrato, estearato de magnesio y celulosa microcristalina. Las tabletas están recubiertas con un material de recubrimiento que contiene los siguientes ingredientes inactivos: óxido férrico rojo, óxido de hierro amarillo, polietilenglicol, alcohol polivinílico, talco y dióxido de titanio.
Sofosbuvir: El nombre IUPAC para sofosbuvir es (S)-Isopropil 2-((S)-(((2R,3R,4R,5R)-5-(2,4-dioxo-3,4-dihidropirimidin-1(2H)-il)-4-fluoro-3-hidroxi-4-metiltetrahidrofuran-2-il)metoxi)-(fenoxi)fosforil amino)propanoato. Tiene una fórmula molecular de C22H29FN3O9P y un peso molecular de 529,45. Tiene la siguiente fórmula estructural:
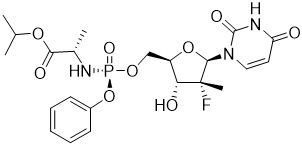
Sofosbuvir es un sólido cristalino de color blanco a blanco amarillento con una solubilidad de al menos 2 mg/ml en el rango de pH de 2 a 7,7 a 37 °C y es ligeramente soluble en agua.
Velpatasvir: El nombre IUPAC para velpatasvir es metil {(1R)-2-[(2S,4S)-2-(5-{2-[(2S,5S)-1-{(2S)-2-[(metoxicarbonil)amino]-3-metilbutanoil}-5-metilpirrolidin-2-il]-1,11-dihidro[2]benzopiranol[4′,3′:6,7]nafta[1,2-d]imidazol-9-il}-1H-imidazol-2-il)-4-(metoximetil)pirrolidin-1-il]-2-oxo-1-feniletiil}carbamato. Tiene una fórmula molecular de C49H54N8O8 y un peso molecular de 883,0. Tiene la siguiente fórmula estructural:
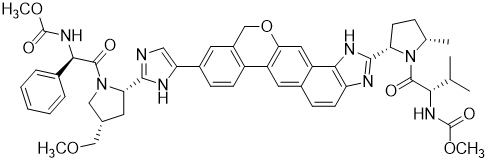
Velpatasvir es prácticamente insoluble (menos de 0,1 mg/ml) por encima de pH 5, ligeramente soluble (3,6 mg/ml) a pH 2 y soluble (más de 36 mg/ml) a pH 1,2.
Voxilaprevir: El nombre IUPAC para voxilaprevir es (1aR,5S,8S,9S,10R,22aR)-5-terc-butil-N-{(1R,2R)-2-(difluorometil)-1-[(1-metilciclopropanilsulfonil) carbamato]}ciclopropil}-9-etil-18,18-difluoro-14-metoxi-3,6-dioxo-1,1a,3,4,5,6,9,10,18,19,20,21,22,22a-tetradecahidro-8H-7,10-metanocicloprop[18,19][1,10,3,6]dioxadiazaciclononadecino[11,12-b]quinoxalina-8-carboxamida. Tiene una fórmula molecular de C40H52F4N6O9S y un peso molecular de 868,9. Tiene la siguiente fórmula estructural:
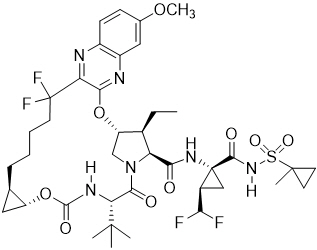
Voxilaprevir es un sólido de color blanco a marrón claro. Es ligeramente higroscópico a higroscópico. Voxilaprevir es prácticamente insoluble (menos de 0,1 mg/ml) por debajo de pH 6,8.
12 FARMACOLOGÍA CLÍNICA
12.1 Mecanismo de Acción
VOSEVI es una combinación de dosis fija de sofosbuvir, velpatasvir y voxilaprevir que son agentes antivirales de acción directa contra el virus de la hepatitis C [ver Microbiología (12.4)].
12.2 Farmacodinámica
Electrofisiología Cardíaca
Se evaluó el efecto de sofosbuvir 400 mg (dosis recomendada) y 1200 mg (3 veces la dosis recomendada) sobre el intervalo QTc en un ensayo QT integral activo-controlado (moxifloxacino 400 mg). A una dosis 3 veces la dosis recomendada, el sofosbuvir no prolonga el QTc a un nivel clínicamente relevante.
Se evaluó el efecto de velpatasvir 500 mg (5 veces la dosis recomendada) en un ensayo QT integral activo-controlado (moxifloxacino 400 mg). A una dosis 5 veces la dosis recomendada, el velpatasvir no prolonga el intervalo QTc a un nivel clínicamente relevante.
Se evaluó el efecto de voxilaprevir 900 mg (9 veces la dosis recomendada) en un ensayo QT integral activo-controlado (moxifloxacino 400 mg). A una dosis 9 veces la dosis recomendada, el voxilaprevir no prolonga el intervalo QTc a un nivel clínicamente relevante.
12.3 Farmacocinética
Las propiedades farmacocinéticas de los componentes de VOSEVI se proporcionan en la Tabla 4. Los parámetros farmacocinéticos de múltiples dosis de sofosbuvir y su metabolito GS-331007, velpatasvir y voxilaprevir se proporcionan en la Tabla 5.
| Sofosbuvir | Velpatasvir | Voxilaprevir | |
|---|---|---|---|
| CES1 = carboxilesterasa 1; HINT1 = proteína triada de histidina 1 de unión a nucleótidos. | |||
|
|||
| Absorción | |||
| Tmax (h) | 2 | 4 | 4 |
| Efecto de los alimentos (relativo al ayuno)* | ↑ 64% a 144% | ↑ 40% a 166% | ↑ 112% a 435% |
| Distribución | |||
| % Unido a proteínas plasmáticas humanas | 61–65 | >99 | >99 |
| Relación sangre-plasma | 0.7 | 0.5–0.7 | 0.5–0.8 |
| Metabolismo | |||
| Metabolismo | Catepsina A CES1 HINT1 |
CYP2B6 CYP2C8 CYP3A4 |
CYP3A4 |
| Eliminación | |||
| Vía principal de eliminación | SOF: metabolismo GS-331007†: filtración glomerular y secreción tubular activa |
Excreción biliar | Excreción biliar |
| t1/2 (h)‡ | SOF: 0.5 GS-331007†: 29 |
17 | 33 |
| % De dosis excretada en orina§ | 80¶ | 0.4 | 0 |
| % De dosis excretada en heces§ | 14 | 94 (77%# como principal) | 94 (40%# como principal) |
| Parámetro Media (%CV) |
Sofosbuvir* | GS-331007† | Velpatasvir‡ | Voxilaprevir§ |
|---|---|---|---|---|
| CV = coeficiente de variación; NA = no aplicable. | ||||
| Cmax (nanogramos por mL) |
678 (35,4) | 744 (28,3) | 311 (56,1) | 192 (85,8) |
| AUCtau (nanogramos∙hr por mL) |
1665 (30,1) | 12834 (29,0) | 4041 (48,6) | 2577 (73,7) |
| Ctrough (nanogramos por mL) |
NA | NA | 51 (64,7) | 47 (82,0) |
El AUC0–24 y la Cmax de sofosbuvir y GS-331007 fueron similares en sujetos adultos sanos y sujetos con infección por VHC. En relación con sujetos sanos (N=137), el AUC0–24 y la Cmax de velpatasvir fueron 41% y 39% menores, respectivamente, en sujetos infectados por VHC. En relación con sujetos sanos (N=63), el AUC0–24 y la Cmax de voxilaprevir fueron 260% mayores en sujetos infectados por VHC.
El AUC de sofosbuvir y GS-331007 es aproximadamente proporcional a la dosis en el rango de 200 mg a 1200 mg. El AUC de velpatasvir aumenta de manera mayor que proporcional de 5 a 50 mg y de manera menor que proporcional de 50 a 450 mg en voluntarios sanos. Sin embargo, velpatasvir exhibió un aumento aproximadamente proporcional a la dosis en las exposiciones de 25 mg a 150 mg en pacientes infectados por VHC. El AUC de voxilaprevir aumenta de manera mayor que proporcional en el rango de dosis de 100 a 900 mg cuando se administra con alimentos.
Poblaciones específicas
Pacientes pediátricos: La farmacocinética de VOSEVI en pacientes pediátricos no se ha establecido [ver Uso en poblaciones específicas (8.4)].
Pacientes de edad avanzada: El análisis farmacocinético poblacional en sujetos infectados por VHC mostró que dentro del rango de edad analizado (18 a 85 años), la edad no tuvo un efecto clínicamente relevante en la exposición a sofosbuvir, GS-331007, velpatasvir o voxilaprevir [ver Uso en poblaciones específicas (8.5)].
Pacientes con insuficiencia renal:
La farmacocinética de sofosbuvir se estudió en sujetos negativos para VHC con insuficiencia renal leve (TFGe entre 50 y menos de 80 mL/min/1,73 m2), moderada (TFGe entre 30 y menos de 50 mL/min/1,73 m2), insuficiencia renal grave (TFGe menor de 30 mL/min/1,73 m2), y sujetos con ERCT que requieren hemodiálisis después de una dosis única de 400 mg de sofosbuvir. En relación con sujetos con función renal normal (TFGe mayor de 80 mL/min/1,73 m2), el AUC0–inf de sofosbuvir fue 61%, 107% y 171% mayor en sujetos con insuficiencia renal leve, moderada y grave, mientras que el AUC0–inf de GS-331007 fue 55%, 88% y 451% mayor, respectivamente. En sujetos con ERCT, en relación con sujetos con función renal normal, el AUC0–inf de sofosbuvir y GS-331007 fue 28% y 1280% mayor cuando se administró sofosbuvir 1 hora antes de la hemodiálisis en comparación con 60% y 2070% mayor cuando se administró sofosbuvir 1 hora después de la hemodiálisis, respectivamente. Una sesión de hemodiálisis de 4 horas eliminó aproximadamente el 18% de la dosis administrada de sofosbuvir [ver Dosificación y administración (2.3) y Uso en poblaciones específicas (8.6)].
La farmacocinética de velpatasvir se estudió con una dosis única de 100 mg de velpatasvir en sujetos negativos para VHC con insuficiencia renal grave (TFGe menor de 30 mL/min por Cockcroft-Gault). No se observaron diferencias clínicamente relevantes en la farmacocinética de velpatasvir entre sujetos sanos y sujetos con insuficiencia renal grave.
La farmacocinética de voxilaprevir se estudió con una dosis única de 100 mg de voxilaprevir en sujetos negativos para VHC con insuficiencia renal grave (TFGe < 30 mL/min por Cockcroft-Gault). No se observaron diferencias clínicamente relevantes en la farmacocinética de voxilaprevir entre sujetos sanos y sujetos con insuficiencia renal grave.
La farmacocinética de sofosbuvir, GS-331007 y velpatasvir se estudió en sujetos con VHC e insuficiencia renal terminal que requerían diálisis tratados con sofosbuvir/velpatasvir 400/100 mg una vez al día durante 12 semanas. Los resultados fueron consistentes con los observados en sujetos sin VHC con insuficiencia renal terminal que requerían diálisis. La farmacocinética de voxilaprevir no se ha estudiado en sujetos con insuficiencia renal terminal. Sin embargo, no se espera que la exposición a voxilaprevir después de la administración de VOSEVI se vea alterada significativamente en sujetos con VHC e insuficiencia renal terminal que requieren diálisis en comparación con sujetos con función renal normal.
Pacientes con deterioro hepático:
La farmacocinética de sofosbuvir se estudió después de la dosificación de 400 mg de sofosbuvir durante 7 días en sujetos con VHC y deterioro hepático moderado y grave (Child-Pugh B y C). En comparación con sujetos con función hepática normal, el AUC0-24 de sofosbuvir fue 126% y 143% más alta en sujetos con deterioro hepático moderado y grave, respectivamente, mientras que el AUC0-24 de GS-331007 fue 18% y 9% más alta, respectivamente. El análisis farmacocinético poblacional en sujetos con VHC indicó que la cirrosis compensada (Child-Pugh A) no tuvo un efecto clínicamente relevante sobre la exposición a sofosbuvir y GS-331007.
La farmacocinética de velpatasvir se estudió con una dosis única de 100 mg de velpatasvir en sujetos sin VHC con deterioro hepático moderado y grave (Child-Pugh B y C). La exposición plasmática a velpatasvir (AUCinf) fue similar en sujetos con deterioro hepático moderado, deterioro hepático grave y sujetos control con función hepática normal. El análisis farmacocinético poblacional en sujetos con VHC indicó que la cirrosis compensada (Child-Pugh A) no tuvo un efecto clínicamente relevante sobre la exposición a velpatasvir.
La farmacocinética de voxilaprevir se estudió con una dosis única de 100 mg de voxilaprevir en sujetos sin VHC con deterioro hepático moderado y grave (Child-Pugh B y C). En comparación con sujetos con función hepática normal, el AUCinf de voxilaprevir fue 299% y 500% más alta en sujetos con deterioro hepático moderado y grave, respectivamente. El análisis farmacocinético poblacional en sujetos con VHC indicó que los sujetos con cirrosis compensada (Child-Pugh A) tuvieron 73% más exposición a voxilaprevir que aquellos sin cirrosis [véanse Dosificación y Administración (2.4) y Uso en Poblaciones Específicas (8.7)].
Estudios de interacción farmacológica
Después de la administración oral de VOSEVI, el sofosbuvir se absorbe rápidamente y está sujeto a una extensa extracción hepática de primer paso (hidrólisis seguida de fosforilación secuencial) para formar el trifosfato farmacológicamente activo. En estudios de farmacología clínica, tanto el sofosbuvir como el principal metabolito circulante GS-331007 (metabolito nucleótido defosforilado) se monitorearon con fines de análisis farmacocinéticos.
Sofosbuvir, velpatasvir y voxilaprevir son sustratos de los transportadores de medicamentos P-gp y BCRP, mientras que GS-331007 no lo es. Voxilaprevir y, en menor medida, velpatasvir también son sustratos de OATP1B1 y OATP1B3. In vitro, se observó una lenta rotación metabólica de velpatasvir por CYP2B6, CYP2C8 y CYP3A4 y de voxilaprevir por CYP1A2, CYP2C8 y principalmente CYP3A4. Los inductores de P-gp y/o inductores de moderados a potentes de CYP2B6, CYP2C8 o CYP3A4 (p.ej., hierba de San Juan, carbamazepina) pueden disminuir significativamente las concentraciones plasmáticas de sofosbuvir, velpatasvir y/o voxilaprevir, lo que conduce a un efecto terapéutico reducido de VOSEVI [véanse Contraindicaciones (4), Advertencias y Precauciones (5.4), y Interacciones Farmacológicas (7.3)]. La coadministración con medicamentos que inhiben P-gp y/o BCRP puede aumentar las concentraciones plasmáticas de sofosbuvir, velpatasvir y/o voxilaprevir sin aumentar la concentración plasmática de GS-331007. La coadministración con medicamentos que inhiben OATP puede aumentar las concentraciones plasmáticas de voxilaprevir. Los medicamentos que inhiben CYP2B6, CYP2C8 o CYP3A4 pueden aumentar la concentración plasmática de velpatasvir y/o voxilaprevir.
Sofosbuvir y GS-331007 no son inhibidores de los transportadores de medicamentos P-gp, BCRP, OATP1B1, OATP1B3 u OCT1 y GS-331007 no es inhibidor de OAT1, OAT3, OCT2 o MATE1. Sofosbuvir y GS-331007 no son inhibidores ni inductores de las enzimas CYP o UGT1A1.
Velpatasvir es un inhibidor de los transportadores de medicamentos P-gp, BCRP, OATP1B1, OATP1B3 y OATP2B1, y su participación en las interacciones farmacológicas con estos transportadores se limita principalmente al proceso de absorción. En concentraciones clínicamente relevantes, velpatasvir no es un inhibidor de los transportadores hepáticos OATP1A2 u OCT1, los transportadores renales OCT2, OAT1, OAT3 o MATE1, ni de las enzimas CYP o UGT1A1.
Voxilaprevir es un inhibidor de los transportadores de medicamentos P-gp, BCRP, OATP1B1 y OATP1B3, y su participación en las interacciones farmacológicas con estos transportadores se limita principalmente al proceso de absorción. En concentraciones clínicamente relevantes, voxilaprevir no es un inhibidor de los transportadores hepáticos OCT1, los transportadores renales OCT2, OAT1, OAT3 o MATE1, ni de las enzimas CYP o UGT1A1.
Los efectos de los medicamentos coadministrados sobre la exposición a sofosbuvir, GS-331007, velpatasvir y voxilaprevir se muestran en la Tabla 6. Los efectos de sofosbuvir, velpatasvir, voxilaprevir, sofosbuvir/velpatasvir o VOSEVI sobre la exposición a los medicamentos coadministrados se muestran en la Tabla 7 [véanse Interacciones Farmacológicas (7)].
| Medicamento coadministrado | Sofosbuvir (SOF)/ Velpatasvir (VEL)/Voxilaprevir (VOX) | N | Razón de medias geométricas (IC 90%) de sofosbuvir, GS-331007, velpatasvir y voxilaprevir PK con/sin medicamento coadministrado Sin efecto=1.00 |
|||||
|---|---|---|---|---|---|---|---|---|
| Medicamento | Dosis (mg) |
Componente activo |
Dosis (mg) |
|||||
| Componente | Cmax | ABC | Cmin | |||||
| NA = no disponible/no aplicable, ND = no dosificado. | ||||||||
| Atazanavir + ritonavir | 300 + 100 dosis única | SOF/VEL/VOX | 400/100/100 dosis única | 15 | sofosbuvir | 1.29 (1.09, 1.52) |
1.40 (1.25, 1.57) |
NA |
| GS-331007 | 1.05 (0.99, 1.12) |
1.25 (1.16, 1.36) |
NA | |||||
| velpatasvir | 1.29 (1.07, 1.56) |
1.93 (1.58, 2.36) |
NA | |||||
| voxilaprevir | 4.42 (3.65, 5.35) |
4.31 (3.76, 4.93) |
NA | |||||
| Carbamazepina | 300 dos veces al día | SOF | 400 dosis única | 24 | sofosbuvir | 0.52 (0.43, 0.62) |
0.52 (0.46, 0.59) |
NA |
| GS-331007 | 1.04 (0.97, 1.11) |
0.99 (0.94, 1.04) |
NA | |||||
| Ciclosporina | 600 dosis única | SOF | 400 dosis única | 19 | sofosbuvir | 2.54 (1.87, 3.45) |
4.53 (3.26, 6.30) |
NA |
| GS-331007 | 0.60 (0.53, 0.69) |
1.04 (0.90, 1.20) |
NA | |||||
| VEL | 100 dosis única | 12 | velpatasvir | 1.56 (1.22, 2.01) |
2.03 (1.51, 2.71) |
NA | ||
| VOX | 100 dosis única | 25 | voxilaprevir | 19.02 (14.12, 25.62) |
9.39 (7.37, 11.96) |
NA | ||
| Darunavir + ritonavir + emtricitabina/ tenofovir DF | 800 + 100 + 200/300 una vez al día | SOF/VEL/VOX + VOX | 400/100/100 + 100 una vez al día |
29 | sofosbuvir | 0.70 (0.62, 0.78) |
0.78 (0.73, 0.83) |
NA |
| GS-331007 | 1.06 (1.01, 1.10) |
1.15 (1.12, 1.19) |
NA | |||||
| velpatasvir | 0.78 (0.73, 0.84) |
0.95 (0.88, 1.02) |
1.16 (1.07, 1.26) |
|||||
| voxilaprevir | 1.72 (1.51, 1.97) |
2.43 (2.15, 2.75) |
4.00 (3.44, 4.65) |
|||||
>
(0.80, 0.98)
(0.85, 0.99)
(0.93, 1.10)
(0.97, 1.01)
(0.97, 1.01)
(0.86, 1.02)
(0.84, 0.98)
(0.82, 0.94)
(1.14, 1.67)
(0.83, 1.14)
(0.80, 0.93)
(0.85, 0.96)
(0.95, 1.07)
(0.43, 0.64)
(0.39, 0.57)
(0.36, 0.52)
(1.09, 1.48)
(1.12, 1.32)
(1.25, 1.32)
(1.39, 1.47)
(0.89, 1.04)
(1.06, 1.27)
(1.30, 1.64)
(1.63, 2.26)
(2.30, 3.19)
(3.68, 5.50)
(1.02, 1.64)
(1.35, 2.18)
(0.68, 1.33)
(1.00, 1.69)
(0.65, 0.83)
(0.89, 1.22)
(0.65, 0.91)
(0.67, 0.79)
(1.20, 1.34)
(0.94, 1.01)
(0.38, 0.49)
(0.41, 0.52)
(0.69, 0.85)
(0.74, 0.87)
VOX
(0.83, 1.06)
(0.77, 0.87)
(1.13, 1.26)
(0.97, 1.01)
(0.43, 0.55)
(0.43, 0.55)
(0.96, 1.22)
(0.88, 1.03)
(0.53, 0.77)
(0.63, 0.91)
(1.03, 1.27)
(0.95, 1.12)
(0.19, 0.29)
(0.24, 0.32)
(1.14, 1.34)
(0.88, 1.03)
(0.23, 0.37)
(0.15, 0.22)
(0.76, 1.10)
(0.23, 0.31)
(1.05, 1.56)
(1.17, 1.83)
(8.23, 14.98)
(6.20, 10.09)
(0.65, 1.43)
(0.81, 1.57)
(0.83, 1.14)
(0.87, 1.13)
(0.98, 1.31)
(1.66, 2.03)
No se observó ningún efecto sobre los parámetros farmacocinéticos de sofosbuvir, GS-331007, velpatasvir o voxilaprevir con la combinación de emtricitabina, rilpivirina y tenofovir alafenamida; famotidina; gemfibrozil; o la combinación de raltegravir, emtricitabina y tenofovir DF.
| Medicamento coadministrado | Sofosbuvir (SOF)/ Velpatasvir (VEL)/Voxilaprevir (VOX) | N | Razón de media geométrica (IC 90%) del medicamento coadministrado PK con/sin sofosbuvir, velpatasvir, voxilaprevir o VOSEVI Sin efecto=1.00 |
||||
|---|---|---|---|---|---|---|---|
| Medicamento | Dosis (mg) |
Componente activo | Dosis (mg) |
||||
| Cmax | ABC | Cmin | |||||
| NA = no disponible/no aplicable. | |||||||
|
|||||||
| Atorvastatina | 40 dosis única | SOF/VEL | 400/100 una vez al día | 26 | 1.68 (1.49, 1.89) |
1.54 (1.45, 1.64) |
NA |
| Ciclosporina | 600 dosis única | SOF | 400 dosis única | 19 | 1.06 (0.94, 1.18) |
0.98 (0.85, 1.14) |
NA |
| VEL | 100 dosis única | 12 | 0.92 (0.82, 1.02) |
0.88 (0.78, 1.00) |
NA | ||
| VOX | 100 dosis única | 24 | 0.95 (0.88, 1.03) |
0.94 (0.84, 1.06) |
NA | ||
| Dabigatrán etexilato | 75 dosis única | SOF/VEL/VOX + VOX | 400/100/100 + 100 una vez al día | 36 | 2.87 (2.61, 3.15) |
2.61 (2.41, 2.82) |
NA |
| Darunavir + ritonavir + emtricitabina/tenofovir DF† | darunavir 800 una vez al día |
SOF/VEL/VOX + VOX | 400/100/100 + 100 una vez al día |
29 | 0.89 (0.85, 0.94) |
0.86 (0.81, 0.91) |
0.66 (0.58, 0.74) |
| ritonavir 100 una vez al día | 1.60 (1.47, 1.75) |
1.45 (1.35, 1.57) |
0.80 (0.72, 0.89) |
||||
| emtricitabina 200 una vez al día | 0.88 (0.82, 0.94) |
0.99 (0.96, 1.03) |
1.20 (1.15, 1.26) |
||||
| tenofovir DF 300 una vez al día | 1.48 (1.36, 1.61) |
1.39 (1.32, 1.46) |
1.47 (1.38, 1.56) |
||||
| Digoxina | 0.25 dosis única | VEL | 100 una vez al día | 21 | 1.88 (1.71, 2.08) |
1.34 (1.13, 1.60) |
NA |
| Efavirenz/emtricitabina/tenofovir DF‡ | efavirenz 600 una vez al día |
SOF/VEL | 400/100 una vez al día | 15 | 0.81 (0.74, 0.89) |
0.85 (0.80, 0.91) |
0.90 (0.85, 0.95) |
| emtricitabina 200 una vez al día | 1.07 (0.98, 1.18) |
1.07 (1.00, 1.14) |
1.10 (0.97, 1.25) |
||||
| tenofovir DF 300 una vez al día | 1.77 (1.53, 2.04) |
1.81 (1.68, 1.94) |
2.21 (2.00, 2.43) |
||||
| Elvitegravir/cobicistat/ emtricitabina/tenofovir alafenamida§ | elvitegravir 150 una vez al día | SOF/VEL/VOX + VOX | 400/100/100 + 100 una vez al día | 29 | 0.79 (0.75, 0.85) |
0.94 (0.88, 1.00) |
1.32 (1.17, 1.49) |
| cobicistat 150 una vez al día | 1.23 (1.18, 1.28) |
1.50 (1.44, 1.58) |
3.50 (3.01, 4.07) |
||||
| emtricitabina 200 una vez al día | 0.87 (0.84, 0.91) |
0.96 (0.94, 0.99) |
1.14 (1.09, 1.20) |
||||
| tenofovir alafenamida 10 una vez al día | 0.79 (0.68, 0.92) |
0.93 (0.85, 1.01) |
NA | ||||
| Emtricitabina/rilpivirina/tenofovir alafenamida¶ | emtricitabina 200 una vez al día | SOF/VEL/VOX + VOX | 400/100/100 + 100 una vez al día | 30 | 0.88 (0.83, 0.93) |
0.93 (0.90, 0.96) |
1.07 (1.01, 1.14) |
| rilpivirina 25 una vez al día | 0.79 (0.74, 0.84) |
0.80 (0.76, 0.85) |
0.82 (0.77, 0.87) |
||||
| tenofovir alafenamida 25 una vez al día | 1.32 (1.17, 1.48) |
1.52 (1.43, 1.61) |
NA | ||||
| Pravastatina | 40 dosis única | SOF/VEL/VOX + VOX | 400/100/100 + 100 una vez al día | 19 | 1.89 (1.53, 2.34) |
2.16 (1.79, 2.60) |
NA |
| Rosuvastatina | 10 dosis única | SOF/VEL/VOX + VOX | 400/100/100 + 100 una vez al día | 19 | 18.88 (16.23, 21.96) |
7.39 (6.68, 8.18) |
NA |
| Raltegravir + emtricitabina/tenofovir DF | emtricitabina 200 una vez al día | SOF/VEL | 400/100 una vez al día | 30 | 1.08 (1.04, 1.12) |
1.05 (1.03, 1.07) |
1.02 (0.97, 1.08) |
| tenofovir DF 300 una vez al día | 1.46 (1.39, 1.54) |
1.40 (1.34, 1.45) |
1.70 (1.61, 1.79) |
||||
| raltegravir 400 dos veces al día | 1.03 (0.74, 1.43) |
0.97 (0.73, 1.28) |
0.79 (0.42, 1.48) |
||||
| Tacrolimus | 5 dosis única | SOF | 400 una vez al día | 16 | 0.73 (0.59, 0.90) |
1.09 (0.84, 1.40) |
NA |
No se observó efecto sobre los parámetros farmacocinéticos de los siguientes medicamentos coadministrados con VOSEVI (etinilestradiol/norgestimato) o sus componentes sofosbuvir/velpatasvir (dolutegravir) o sofosbuvir (metadona).
12.4 Microbiología
Mecanismo de Acción
Sofosbuvir es un inhibidor de la polimerasa NS5B de ARN dependiente de ARN del VHC, que se requiere para la replicación viral. Sofosbuvir es un profármaco de nucleótido que sufre metabolismo intracelular para formar el trifostato análogo de uridina farmacológicamente activo (GS-461203), que puede incorporarse al ARN del VHC por la polimerasa NS5B y actúa como terminador de cadena. En un ensayo bioquímico, GS-461203 inhibió la actividad de la polimerasa de la NS5B recombinante de los genotipos 1b, 2a, 3a y 4a del VHC con un valor de CI50 que varió de 0.36 a 3.3 μM. GS-461203 no es un inhibidor de las polimerasas de ADN y ARN humanas ni un inhibidor de la polimerasa de ARN mitocondrial.
Velpatasvir es un inhibidor de la proteína NS5A del VHC, que se requiere para la replicación viral. Los estudios de selección de resistencia en cultivo celular y de resistencia cruzada indican que velpatasvir tiene como modo de acción la diana NS5A.
Voxilaprevir es un inhibidor no covalente y reversible de la proteasa NS3/4A, que es necesaria para la escisión proteolítica de la poliproteína codificada por el VHC (en formas maduras de las proteínas NS3, NS4A, NS4B, NS5A y NS5B) y es esencial para la replicación viral. En un ensayo de inhibición bioquímica, voxilaprevir inhibió la actividad proteolítica de las enzimas NS3/4A recombinantes de aislados clínicos de los genotipos 1b y 3a del VHC con valores de Ki de 38 y 66 pM, respectivamente.
Actividad Antiviral
En ensayos de replicón de VHC, sofosbuvir tuvo valores EC50 medios de 15-110 nM contra aislados de laboratorio completos o quiméricos y aislados clínicos de los subtipos 1a, 1b, 2a, 2b, 3a, 4a, 4d, 5a y 6a. Velpatasvir tuvo valores EC50 medios de 0,002-0,13 nM contra aislados de laboratorio completos o quiméricos y aislados clínicos de los subtipos 1a, 1b, 2a, 2b, 3a, 4a, 4d, 4r, 5a, 6a y 6e. Voxilaprevir tuvo valores EC50 medios de 0,2-6,6 nM contra aislados de laboratorio completos o quiméricos y aislados clínicos de los subtipos 1a, 1b, 2a, 2b, 3a, 4a, 4d, 4r, 5a, 6a, 6e y 6n.
La evaluación de sofosbuvir en combinación con velpatasvir o voxilaprevir, así como la combinación de velpatasvir y voxilaprevir, no mostró ningún efecto antagónico en la reducción de los niveles de ARN del VHC en células de replicón.
Resistencia
En cultivo celular
Se han seleccionado replicones de VHC con susceptibilidad reducida a sofosbuvir en cultivo celular para múltiples genotipos, incluyendo 1b, 2a, 2b, 3a, 4a, 5a y 6a. La susceptibilidad reducida a sofosbuvir se asoció con la sustitución de resistencia S282T del inhibidor de la polimerasa NS5B análogo de nucleótidos, en todos los genotipos de replicón examinados. Una sustitución M289L emergió junto con la sustitución S282T en replicones de genotipos 2a, 5 y 6. La mutagénesis dirigida al sitio de la sustitución S282T en replicones de genotipo 1 a 6 confirió una susceptibilidad reducida de 2 a 18 veces a sofosbuvir.
Se seleccionaron variantes de replicón de VHC de genotipo 1a, 1b, 2a, 3a, 4a, 5a y 6a con susceptibilidad reducida a velpatasvir en cultivo celular. Las variantes de replicón desarrollaron sustituciones de aminoácidos en las posiciones asociadas a resistencia a inhibidores de NS5A 24, 28, 30, 31, 32, 58, 92 y 93. El análisis fenotípico de replicones mutantes dirigidos al sitio de las sustituciones seleccionadas de NS5A mostró que la sustitución única Y93H/N y la combinación de L31V + Y93H/N en genotipo 1a, la combinación de L31V + Y93H en genotipo 1b, la sustitución única Y93H/S en genotipo 3a, y las sustituciones únicas L31V y P32A/L/Q/R en genotipo 6 confirieron una reducción mayor de 100 veces en la susceptibilidad a velpatasvir. En el replicón de genotipo 2a, las sustituciones únicas F28S e Y93H mostraron una susceptibilidad reducida de 91 y 46 veces, respectivamente, a velpatasvir. La sustitución única Y93H confirió una susceptibilidad reducida de 3 veces a velpatasvir en replicones de genotipo 4a. Las combinaciones de estas sustituciones de NS5A a menudo mostraron mayores reducciones en la susceptibilidad a velpatasvir que las sustituciones únicas solas.
Se seleccionaron variantes de replicón de VHC de genotipo 1a, 1b, 2a, 3a, 4a, 5a y 6a con susceptibilidad reducida a voxilaprevir en cultivo celular. Se seleccionaron sustituciones de aminoácidos en las posiciones asociadas a resistencia al inhibidor de proteasa NS3/4A 41, 156 y 168. La mutagénesis dirigida al sitio de las sustituciones asociadas a resistencia de NS3 mostró que las sustituciones que confieren una reducción mayor de 100 veces en la susceptibilidad a voxilaprevir fueron A156L/T en genotipo 1a, A156T/V en genotipo 1b, A156L/V en genotipo 2a, A156T/V en genotipo 3a, y A156L/T/V en genotipo 4. Las combinaciones de estas sustituciones de NS3 a menudo mostraron mayores reducciones en la susceptibilidad a voxilaprevir que las sustituciones únicas solas.
En ensayos clínicos
De los 263 sujetos con experiencia con inhibidores de NS5A tratados con VOSEVI durante 12 semanas en POLARIS-1, 7 de 263 (3%) sujetos (2 con genotipo 1a, 4 con genotipo 3a y 1 con genotipo 4d) no lograron alcanzar RVS12 y calificaron para análisis de resistencia; 6 recayeron y 1 experimentó un fracaso virológico. Todos los fracasos virológicos tenían cirrosis y todos habían recibido previamente un régimen de AAD que contenía sofosbuvir; 3 fueron tratados previamente con ledipasvir/sofosbuvir, 2 fueron tratados previamente con sofosbuvir/velpatasvir, y 2 fueron tratados previamente con daclatasvir y sofosbuvir. Seis de los 7 fracasos virológicos tenían sustituciones asociadas a resistencia a inhibidores de NS5A en la posición 30 o 93 al inicio. Todos los 7 fracasos virológicos tenían sustituciones asociadas a resistencia de NS5A al fracaso usando un umbral de sensibilidad del 1% de la población viral.
De los 2 sujetos con fracaso virológico de genotipo 1a, un sujeto con fracaso virológico en la semana 12 tenía virus con la sustitución asociada a resistencia de NS5A Q30T al inicio y al fracaso y emergencia de las sustituciones asociadas a resistencia de NS5A L31M e Y93H en el fracaso; el otro sujeto tenía virus con la sustitución asociada a resistencia de NS5A Y93N al inicio y la recaída y la emergencia de K24R de bajo nivel (1,2%) en NS5A y V36A (2%) en NS3 en la recaída.
De los 4 sujetos con fracaso virológico de genotipo 3a, un sujeto tenía virus con la sustitución asociada a resistencia de NS5A E92K emergente. Dos sujetos tenían virus con Y93H en la recaída que se enriqueció desde el inicio. El sujeto restante tenía virus con la sustitución asociada a resistencia de NS5A A30K al inicio y la recaída y la emergencia de sustituciones de bajo nivel Q41K (2%), V55A (3%) y R155M (1%) en NS3 en la recaída.
El sujeto de genotipo 4d que recayó tenía virus con la sustitución asociada a resistencia de NS5A Y93H emergente.
No emergieron sustituciones asociadas a resistencia al inhibidor análogo de nucleótidos de NS5B entre los sujetos con fracaso virológico de POLARIS-1.
En POLARIS-4, de los 182 sujetos con experiencia con AAD que no habían recibido un inhibidor de NS5A tratados con VOSEVI durante 12 semanas, 1 sujeto (genotipo 1a) de 182 (1%) sujetos recayó y calificó para análisis de resistencia. La sustitución asociada a resistencia de NS5A M28T (7,5%) emergió en este sujeto en la recaída. No se observaron sustituciones del inhibidor de proteasa NS3/4A o del inhibidor de NS5B análogo de nucleótidos en este sujeto en la recaída.
Persistencia de las sustituciones asociadas a resistencia
No hay datos disponibles sobre la persistencia de las sustituciones asociadas a resistencia de sofosbuvir, velpatasvir o voxilaprevir. Se ha encontrado que las sustituciones asociadas a resistencia a inhibidores de NS5A observadas con la administración de otros inhibidores de NS5A persisten durante más de 1 año en la mayoría de los pacientes. Se desconoce el impacto clínico a largo plazo de la emergencia o persistencia del virus que contiene sustituciones asociadas a resistencia de sofosbuvir, velpatasvir o voxilaprevir.
Efecto de las variantes basales de VHC en la respuesta al tratamiento
Se realizaron análisis para explorar la asociación entre las tasas de RVS12 y las sustituciones asociadas a la resistencia preexistente a los inhibidores de la proteasa NS3/4A y a los inhibidores de NS5A en la línea de base para los sujetos en POLARIS-1 y POLARIS-4. Las posiciones de aminoácidos consideradas en los análisis de resistencia incluyeron las posiciones NS3 36, 41, 43, 54, 55, 56, 155, 156 y 168, y las posiciones NS5A 24, 28, 30, 31, 58, 92 o 93. Las sustituciones de aminoácidos asociadas a la resistencia en la línea de base, que pueden incluir polimorfismos naturales o sustituciones emergentes del tratamiento previo en relación con referencias específicas de subtipo, se identificaron mediante análisis de secuenciación de nueva generación utilizando un umbral de sensibilidad del 15% de la población viral.
En general, la presencia de sustituciones asociadas a la resistencia a los inhibidores de la proteasa NS3/4A, a los inhibidores de NS5A y a los inhibidores de la polimerasa NS5B de análogos de nucleótidos en la línea de base no alteró las tasas de RVS para los sujetos con experiencia en AAD en los ensayos POLARIS-1 y POLARIS-4 que recibieron 12 semanas de VOSEVI. Para los sujetos tratados con VOSEVI durante 12 semanas, las tasas de RVS12 en sujetos con o sin sustituciones asociadas a la resistencia de NS3 y NS5A en la línea de base en los ensayos POLARIS-1 y POLARIS-4 fueron todas iguales o superiores al 97%.
En POLARIS 1, que incluyó a sujetos con experiencia con inhibidores de NS5A, el 79% (206/260) de los sujetos tenían sustituciones asociadas a la resistencia de NS5A en la línea de base en todos los genotipos. Las sustituciones asociadas a la resistencia de NS5A más prevalentes se encontraban en las posiciones primarias de aminoácidos asociados a la resistencia 30 (97/206; 47%), 31 (58/206; 28%) y 93 (103/206; 50%). El cincuenta y cinco por ciento (n=113/206) de los sujetos tenía una sola sustitución asociada a la resistencia de NS5A, mientras que se detectaron 2 sustituciones asociadas a la resistencia en 65/206 sujetos (32%) y 3 o más en 28/206 sujetos (14%). La prevalencia general de sustituciones asociadas a la resistencia del inhibidor de la proteasa NS3/4A en todos los genotipos fue del 15% (37/248). Las sustituciones asociadas a la resistencia de NS3 más prevalentes se encontraban en las posiciones 36 (5/17; 29%) y 168 (7/17; 41%) en el genotipo 1a y en la posición 56 en el genotipo 1b (8/12; 67%). Se detectaron sustituciones en las posiciones 36, 56 o 168 en 1-2 sujetos para cada genotipo 2, 3 o 4.
En POLARIS-4, que incluyó a sujetos con experiencia en AAD que no habían recibido un inhibidor de NS5A, el 32% (57/177) de los sujetos que recibieron 12 semanas de VOSEVI tenían sustituciones asociadas a la resistencia al inhibidor de NS5A en la línea de base. La mayoría de los sujetos tenían una sola sustitución asociada a la resistencia de NS5A (n=40; 70%). La sustitución asociada a la resistencia de NS5A más prevalente se encontraba en la posición de aminoácido 31 (n=27; 47%). La prevalencia general de sustituciones asociadas a la resistencia del inhibidor de la proteasa NS3/4A en la línea de base fue del 12% (21/169). Las sustituciones asociadas a la resistencia de NS3 más prevalentes se encontraban en las posiciones 55 (5/10) y 168 (3/10) en el genotipo 1a, la posición 56 en el genotipo 1b (3/5) y el genotipo 2 (3/3), y en la posición 168 en el genotipo 4 (3/3).
Se logró una RVS12 en 18 de 19 (95%) sujetos que tenían sustituciones asociadas a la resistencia al inhibidor de la polimerasa NS5B de análogos de nucleótidos en la línea de base en POLARIS-1, incluidos 2 sujetos que tenían virus con la sustitución asociada a la resistencia al inhibidor de la polimerasa NS5B de análogos de nucleótidos S282T además de sustituciones asociadas a la resistencia de NS5A en la línea de base. En POLARIS-4, un total de 14 sujetos tenían virus con sustituciones asociadas a la resistencia al inhibidor de la polimerasa NS5B de análogos de nucleótidos en la línea de base y todos lograron RVS12.
Resistencia Cruzada
Es posible la resistencia cruzada entre los inhibidores de la proteasa NS3/4A del VHC y entre los inhibidores de NS5A del VHC por clase. Sofosbuvir, velpatasvir y voxilaprevir fueron activos contra las sustituciones asociadas con la resistencia a otras clases de AAD con diferentes mecanismos de acción (por ejemplo, voxilaprevir fue totalmente activo contra el virus con sustituciones asociadas a la resistencia de NS5A y sustituciones asociadas a la resistencia al inhibidor de NS5B de análogos de nucleótidos).
13 TOXICOLOGÍA NO CLÍNICA
13.1 Carcinogénesis, Mutagénesis, Deterioro de la Fertilidad
Carcinogénesis y Mutagénesis
Sofosbuvir: Sofosbuvir no fue genotóxico en una batería de ensayos in vitro o in vivo, incluyendo mutagenicidad bacteriana, aberración cromosómica usando linfocitos de sangre periférica humana y ensayos de micronúcleos en ratones in vivo.
Sofosbuvir no fue carcinogénico en un estudio de 2 años en ratones (hasta 200 mg/kg/día en machos y 600 mg/kg/día en hembras) y en un estudio de 2 años en ratas (hasta 750 mg/kg/día), resultando en exposiciones del metabolito circulante predominante GS-331007 de aproximadamente 4 y 17 veces (en ratones machos y hembras, respectivamente) y 9 veces (en ratas) la exposición en humanos a la dosis humana recomendada (RHD).
Velpatasvir: Velpatasvir no fue genotóxico en una batería de ensayos in vitro o in vivo, incluyendo mutagenicidad bacteriana, aberración cromosómica usando linfocitos de sangre periférica humana y ensayos de micronúcleos en ratas in vivo.
Velpatasvir no fue carcinogénico en un estudio de 6 meses en ratones transgénicos rasH2 (hasta 1000 mg/kg/día) y un estudio de carcinogenicidad de 2 años en ratas (hasta 200 mg/kg/día). La exposición de VEL en el estudio de 2 años en ratas fue aproximadamente 6 veces la exposición en humanos a la RHD.
Voxilaprevir: Voxilaprevir no fue genotóxico en una batería de ensayos in vitro o in vivo, incluyendo mutagenicidad bacteriana, aberración cromosómica usando linfocitos de sangre periférica humana y ensayos de micronúcleos en ratas in vivo.
No se han realizado estudios de carcinogenicidad para voxilaprevir.
Deterioro de la Fertilidad
Sofosbuvir: Sofosbuvir no tuvo efectos sobre la viabilidad embrionaria-fetal o sobre la fertilidad cuando se evaluó en ratas. En la dosis más alta evaluada, la exposición AUC al metabolito circulante predominante GS-331007 fue aproximadamente 4 veces la exposición en humanos a la RHD.
14 ESTUDIOS CLÍNICOS
14.1 Descripción de los Ensayos Clínicos
La eficacia de VOSEVI fue evaluada en dos ensayos de Fase 3 en sujetos con experiencia en el uso de antivirales de acción directa (DAA) con infección por VHC de genotipo 1, 2, 3, 4, 5 o 6 sin cirrosis o con cirrosis compensada, como se resume en la Tabla 8.
| Ensayo | Población | Brazos del estudio y grupos comparadores (Número de sujetos tratados) |
|---|---|---|
| DAA: antiviral de acción directa; SOF: sofosbuvir; VEL: velpatasvir | ||
|
||
| POLARIS-1* (NCT02607735) |
Genotipo 1, 2, 3, 4, 5 o 6 con experiencia con inhibidores de NS5A†, sin cirrosis o con cirrosis compensada |
VOSEVI 12 semanas (263) Placebo 12 semanas (152) |
| POLARIS-4‡ (NCT02639247) |
Genotipo 1, 2, 3 o 4 con experiencia con DAA§ que no han recibido un inhibidor de NS5A, sin cirrosis o con cirrosis compensada |
VOSEVI 12 semanas (182) SOF/VEL 12 semanas (151) |
Los valores de ARN del VHC en suero se midieron durante los ensayos clínicos utilizando la prueba COBAS AmpliPrep/COBAS Taqman HCV (versión 2.0) con un límite inferior de cuantificación (LLOQ) de 15 UI/mL. La respuesta viral sostenida (RVS12), definida como ARN del VHC menor que LLOQ a las 12 semanas después del cese del tratamiento, fue el criterio de valoración principal en ambos ensayos. La recaída se define como ARN del VHC mayor o igual que LLOQ después de la respuesta al final del tratamiento entre los sujetos que completaron el tratamiento. El fracaso virológico en el tratamiento se define como breakthrough, rebote o no respuesta.
14.2 Ensayos Clínicos en Adultos con Experiencia en el uso de DAA para el VHC
Adultos con Experiencia con Inhibidores de NS5A Sin Cirrosis o Con Cirrosis Compensada (POLARIS-1)
POLARIS-1 fue un ensayo aleatorizado, doble ciego, controlado con placebo que evaluó 12 semanas de tratamiento con VOSEVI en comparación con 12 semanas de placebo en sujetos con experiencia en el uso de DAA con infección por VHC de genotipo 1, 2, 3, 4, 5 o 6 sin cirrosis o con cirrosis compensada que previamente no respondieron a un régimen que contenía un inhibidor de NS5A. Los sujetos con infección por VHC de genotipo 1 fueron aleatorizados 1:1 a cada grupo. Los sujetos con infección por VHC de genotipo 2, 3, 4, 5 o 6 fueron asignados al grupo de VOSEVI. La aleatorización se estratificó por la presencia o ausencia de cirrosis.
Las características demográficas y basales estuvieron generalmente equilibradas entre los grupos de tratamiento. De los 415 sujetos tratados, la mediana de edad fue de 59 años (rango: 27 a 84); el 77% de los sujetos eran hombres; el 81% eran blancos; el 14% eran negros; el 6% eran hispanos o latinos; el 33% tenía un índice de masa corporal basal de al menos 30 kg/m2; la mayoría de los sujetos tenían infección por VHC de genotipo 1 (72%) o genotipo 3 (19%); el 82% tenía un genotipo IL28B no CC (CT o TT); el 74% tenía niveles basales de ARN del VHC de al menos 800,000 UI/mL; y el 41% tenía cirrosis compensada. En el ensayo POLARIS-1, los regímenes previos de DAA contenían los siguientes inhibidores de NS5A: ledipasvir (51%), daclatasvir (27%), ombitasvir (11%), velpatasvir (7%) y elbasvir (3%).
La Tabla 9 presenta la RVS12 por genotipo del VHC para el ensayo POLARIS-1. Ningún sujeto en el grupo placebo logró RVS12.
| VOSEVI 12 Semanas (N=263) |
|||||||||
|---|---|---|---|---|---|---|---|---|---|
| Total (todos los GTs)* (N=263) |
GT-1 | GT-2 (N=5) |
GT-3 (N=78) |
GT-4 (N=22) |
GT-5 (N=1) |
GT-6 (N=6) |
|||
| GT-1a (N=101) | GT-1b (N=45) | Total† (N=150) | |||||||
| GT: genotipo | |||||||||
|
|||||||||
| RVS12 | 96% (253/263) |
96% (97/101) |
100% (45/45) |
97% (146/150) |
100% (5/5) |
95% (74/78) |
91% (20/22) |
100% (1/1) |
100% (6/6) |
| Resultado para sujetos sin RVS | |||||||||
| Falla virológica durante el tratamiento | <1% (1/263) |
1% (1/101) |
0/45 | 1% (1/150) |
0/5 | 0/78 | 0/22 | 0/1 | 0/6 |
| Recaída‡ | 2% (6/261) |
1% (1/100) |
0/45 | 1% (1/149) |
0/5 | 5% (4/78) |
5% (1/21) |
0/1 | 0/6 |
| Otro§ | 1% (3/263) |
2% (2/101) |
0/45 | 1% (2/150) |
0/5 | 0/78 | 5% (1/22) |
0/1 | 0/6 |
Adultos con experiencia a AAD sin cirrosis o con cirrosis compensada que no habían recibido un inhibidor de NS5A (POLARIS-4)
POLARIS-4 fue un ensayo aleatorizado, abierto que evaluó 12 semanas de tratamiento con VOSEVI y 12 semanas de tratamiento con SOF/VEL en sujetos con infección por VHC genotipo 1, 2, 3 o 4 sin cirrosis o con cirrosis compensada que previamente habían fallado un régimen que contenía AAD que no incluía un inhibidor de NS5A. Se excluyó a los sujetos cuya única exposición a AAD era un inhibidor de proteasa NS3/4A. Los sujetos con infección por VHC genotipo 1, 2 o 3 se aleatorizaron en una proporción de 1:1 a cada grupo. La aleatorización se estratificó por el genotipo de VHC y por la presencia o ausencia de cirrosis. Los sujetos con infección por VHC genotipo 4 se inscribieron en el grupo de VOSEVI. No se inscribió a ningún sujeto con genotipo 5 o 6.
Las características demográficas y al inicio del estudio estuvieron en general equilibradas entre los grupos de tratamiento. De los 333 sujetos tratados, la edad mediana fue de 58 años (rango: 24 a 85); el 77% de los sujetos eran hombres; 87% eran blancos, 9% eran negros; 8% eran hispanos o latinos; 35% tenían un índice de masa corporal basal de al menos 30 kg/m2; 81% tenían genotipos IL28B no CC (CT o TT); 75% tenían niveles basales de ARN de VHC de al menos 800,000 UI/ml; y 46% tenían cirrosis compensada. En el ensayo POLARIS-4, los regímenes previos con AAD contenían sofosbuvir (85%) con lo siguiente: peginterferon alfa y ribavirina o ribavirina (69%), inhibidor de proteasa NS3/4A de VHC (boceprevir, simeprevir o telaprevir; 15%), y AAD en investigación (<1%). Del 15% de sujetos sin exposición previa a sofosbuvir, la mayoría recibieron AAD de VHC en investigación o inhibidores de proteasa NS3/4A aprobados, con o sin peginterferon alfa y ribavirina.
El tratamiento con VOSEVI durante 12 semanas dio lugar a tasas de RVS12 (respuesta viral sostenida 12 semanas después del tratamiento) numéricamente más altas que el tratamiento con sofosbuvir/velpatasvir durante 12 semanas en sujetos con infección por VHC (virus de la hepatitis C) de genotipos 1a y 3. Se observaron tasas de RVS12 comparables en sujetos con infección por VHC de genotipos 1b y 2 tratados con VOSEVI durante 12 semanas o con sofosbuvir/velpatasvir durante 12 semanas. No hay datos comparativos disponibles para los genotipos 4, 5 y 6 del VHC. Dados estos datos, no se ha demostrado el beneficio adicional de VOSEVI sobre sofosbuvir/velpatasvir para estos genotipos y VOSEVI solo está indicado para el tratamiento de la infección por VHC de genotipos 1a o 3 en adultos que previamente recibieron sofosbuvir sin un inhibidor de la NS5A.
La Tabla 10 presenta los datos de resultados virológicos comparativos para sujetos con genotipos 1, 2 y 3 del VHC con exposición previa a un régimen que contenía sofosbuvir.
| *Sujetos con exposición previa a un régimen que contiene SOF | VOSEVI 12 Semanas (N=139) |
SOF/VEL 12 Semanas (N=125) |
|---|---|---|
| General (Genotipos 1, 2 y 3) | ||
| RVS12 | 97% (135/139) | 88% (110/125) |
| Sin lograr RVS12 | ||
| Falla virológica durante el tratamiento | 0% (0/139) | 1% (1/125) |
| Recaída* | 1% (1/139) | 10% (13/124) |
| Otros† | 2% (3/139) | 1% (1/125) |
| Genotipo 1 | ||
| RVS12 | 96% (52/54) | 85% (34/40) |
| Sin lograr RVS12 | ||
| Falla virológica durante el tratamiento | 0% (0/54) | 0% (0/40) |
| Recaída* | 2% (1/54) | 13% (5/40) |
| Otros† | 2% (1/54) | 3% (1/40) |
| Genotipo 1a | ||
| RVS12 | 97% (35/36) | 82% (23/28) |
| Sin lograr RVS12 | ||
| Falla virológica durante el tratamiento | 0% (0/36) | 0% (0/28) |
| Recaída* | 3% (1/36) | 18% (5/28) |
| Otros† | 0% (0/36) | 0% (0/28) |
| Genotipo 1b | ||
| RVS12 | 94% (17/18) | 92% (11/12) |
| Sin lograr RVS12 | ||
| Falla virológica durante el tratamiento | 0% (0/18) | 0% (0/12) |
| Recaída* | 0% (0/18) | 0% (0/12) |
| Otros† | 6% (1/18) | 8% (1/12) |
| Genotipo 2 | ||
| RVS12 | 100% (31/31) | 97% (32/33) |
| Sin lograr RVS12 | ||
| Falla virológica durante el tratamiento | 0% (0/31) | 3% (1/33) |
| Recaída* | 0% (0/31) | 0% (0/32) |
| Otros† | 0% (0/31) | 0% (0/33) |
| Genotipo 3 | ||
| RVS12 | 96% (52/54) | 85% (44/52) |
| Sin lograr RVS12 | ||
| Fracaso virológico durante el tratamiento | 0% (0/54) | 0% (0/52) |
| Recaída* | 0% (0/54) | 15% (8/52) |
| Otro† | 4% (2/54) | 0% (0/52) |
En POLARIS-4, VOSEVI se administró durante 12 semanas a 18 sujetos con VHC genotipo 4 (con o sin cirrosis) que habían estado previamente expuestos a un régimen que contenía SOF sin un inhibidor de NS5A. Todos los sujetos alcanzaron RVS12.
16 PRESENTACIÓN / ALMACENAMIENTO Y MANIPULACIÓN
Cada tableta de VOSEVI contiene 400 mg de sofosbuvir, 100 mg de velpatasvir y 100 mg de voxilaprevir. Las tabletas son beiges, con forma de cápsula, recubiertas con película y grabadas con “GSI” en un lado y “ ” en el otro. Cada frasco contiene 28 tabletas (NDC 61958-2401-1), una bobina de poliéster, un desecante de gel de sílice y está cerrado con un cierre resistente a los niños.
” en el otro. Cada frasco contiene 28 tabletas (NDC 61958-2401-1), una bobina de poliéster, un desecante de gel de sílice y está cerrado con un cierre resistente a los niños.
17 INFORMACIÓN DE ASESORAMIENTO PARA EL PACIENTE
Aconsejar al paciente que lea la información del paciente aprobada por la FDA (Información para el Paciente).
Riesgo de reactivación del virus de la hepatitis B en pacientes coinfectados con VHC y VHB
Informar a los pacientes que puede ocurrir una reactivación del VHB en pacientes coinfectados con VHB durante o después del tratamiento de la infección por el virus de la hepatitis C. Aconsejar a los pacientes que le comenten a su proveedor de atención médica si tienen antecedentes de infección por hepatitis B [ver Advertencias y precauciones (5.1)].
Riesgo de descompensación/insuficiencia hepática en pacientes con evidencia de enfermedad hepática avanzada
Aconsejar a los pacientes que busquen evaluación médica de inmediato si presentan síntomas de problemas hepáticos agravados como náuseas, cansancio, amarillamiento de la piel o la parte blanca de los ojos, sangrado o hematomas más fácilmente de lo normal, confusión, pérdida de apetito, diarrea, orina oscura o de color café, heces oscuras o con sangre, hinchazón del área del estómago (abdomen) o dolor en la parte superior derecha del área del estómago, somnolencia o vómitos con sangre [ver Advertencias y precauciones (5.2)].
Bradicardia sintomática grave cuando se administra conjuntamente con amiodarona
Aconsejar a los pacientes que busquen evaluación médica de inmediato si presentan síntomas de bradicardia como casi desmayarse o desmayarse, mareos o vértigo, malestar general, debilidad, cansancio excesivo, dificultad para respirar, dolor en el pecho, confusión o problemas de memoria [ver Advertencias y precauciones (5.3), Reacciones adversas (6.2) y Interacciones farmacológicas (7.3)].
Interacciones farmacológicas
Informar a los pacientes que VOSEVI puede interactuar con otros medicamentos. Aconsejar a los pacientes que informen a su proveedor de atención médica sobre el uso de cualquier otro medicamento con o sin receta o productos a base de hierbas, incluyendo la hierba de San Juan [ver Advertencias y precauciones (5.3, 5.4) e Interacciones farmacológicas (7)].
Administración
Aconsejar a los pacientes que tomen VOSEVI una vez al día en un horario regular con alimentos. Informar a los pacientes que es importante no omitir o saltarse dosis y tomar VOSEVI durante el tiempo que recomiende el médico.
SECCIÓN NO CLASIFICADA DE SPL
Fabricado y distribuido por:
Gilead Sciences, Inc.
Foster City, CA 94404
VOSEVI, ATRIPLA, GENVOYA, HARVONI, y ODEFSEY son marcas comerciales de Gilead Sciences, Inc., o sus empresas relacionadas. Todas las demás marcas comerciales a las que se hace referencia aquí son propiedad de sus respectivos propietarios.
© 2019 Gilead Sciences, Inc. Todos los derechos reservados.
209195-GS-003
INSERTO DE PAQUETE PARA EL PACIENTE
| Esta información para el paciente ha sido aprobada por la Administración de Alimentos y Medicamentos de los EE. UU. | Revisada: 11/2019 | ||
| Información para el paciente VOSEVI® (voh-SEV-ee) (sofosbuvir, velpatasvir y voxilaprevir) tabletas |
|||
| ¿Cuál es la información más importante que debo saber sobre VOSEVI? VOSEVI puede causar efectos secundarios graves, incluyendo: Reactivación del virus de la hepatitis B: Antes de comenzar el tratamiento con VOSEVI, su proveedor de atención médica le hará análisis de sangre para verificar la infección por el virus de la hepatitis B. Si alguna vez tuvo infección por el virus de la hepatitis B, el virus de la hepatitis B podría reactivarse durante o después del tratamiento de la hepatitis C con VOSEVI. La reactivación del virus de la hepatitis B (llamada reactivación) puede causar problemas hepáticos graves, incluyendo insuficiencia hepática y muerte. Su proveedor de atención médica lo vigilará si está en riesgo de reactivación del virus de la hepatitis B durante el tratamiento y después de que deje de tomar VOSEVI. Para más información sobre los efectos secundarios, consulte la sección “¿Cuáles son los posibles efectos secundarios de VOSEVI?“ |
|||
| ¿Qué es VOSEVI? VOSEVI es un medicamento recetado que se usa para tratar a adultos con infección crónica (duradera) por el virus de la hepatitis C (VHC) sin cirrosis o con cirrosis compensada que tienen:
No se sabe si VOSEVI es seguro y eficaz en niños. |
|||
| No tome VOSEVI: si también toma cualquier medicamento que contenga rifampicina (Rifater®, Rifamate®, Rimactane®, Rifadin®) | |||
Antes de tomar VOSEVI, informe a su proveedor de atención médica sobre todas sus afecciones médicas, incluyendo si usted:
Informe a su proveedor de atención médica sobre todos los medicamentos que toma, incluyendo medicamentos recetados y de venta libre, vitaminas y suplementos herbales. VOSEVI y otros medicamentos pueden afectarse mutuamente. Esto puede hacer que tenga demasiado o muy poco VOSEVI u otros medicamentos en su cuerpo. Esto puede afectar la forma en que VOSEVI u otros medicamentos funcionan o puede causar efectos secundarios.
|
|||
¿Cómo debo tomar VOSEVI?
|
|||
| ¿Cuáles son los posibles efectos secundarios de VOSEVI? VOSEVI puede causar efectos secundarios graves, incluyendo:
|
|||
|
|
||
|
|||
> |
|
||
Estos no son todos los posibles efectos secundarios de VOSEVI. |
|||
¿Cómo debo almacenar VOSEVI?
Mantenga VOSEVI y todos los medicamentos fuera del alcance de los niños. |
|||
| Información general sobre el uso seguro y eficaz de VOSEVI A veces se prescriben medicamentos para fines distintos de los enumerados en un folleto de Información para el Paciente. No use VOSEVI para una afección para la cual no fue recetado. No le dé VOSEVI a otras personas, incluso si tienen los mismos síntomas que usted. Puede dañarlos. Puede pedirle a su farmacéutico o proveedor de atención médica información sobre VOSEVI que esté escrita para profesionales de la salud. |
|||
| ¿Cuáles son los ingredientes de VOSEVI? Ingredientes activos: sofosbuvir, velpatasvir y voxilaprevir Ingredientes inactivos: dióxido de silicio coloidal, copovidona, croscarmelosa sódica, lactosa monohidrato, estearato de magnesio y celulosa microcristalina. El recubrimiento de la tableta contiene: óxido férrico-férrico, óxido rojo de hierro, óxido amarillo de hierro, polietilenglicol, alcohol polivinílico, talco y dióxido de titanio. Fabricado y distribuido por: Gilead Sciences, Inc., Foster City, CA 94404 Para más información, llame al 1-800-445-3235 o visite www.VOSEVI.com. VOSEVI es una marca registrada de Gilead Sciences, Inc., o sus empresas relacionadas. Todas las demás marcas comerciales a las que se hace referencia en este documento son propiedad de sus respectivos propietarios. ©2019 Gilead Sciences, Inc. Todos los derechos reservados. 209195-GS-003 |
|||
PANEL PRINCIPAL DE EXHIBICIÓN – Etiqueta de la botella de 28 tabletas
NDC 61958-2401-1
28 tabletas
Vosevi™
(sofosbuvir, velpatasvir,
y voxilaprevir) tabletas
400 mg / 100 mg / 100 mg
Tome 1 tableta una vez al día
Nota para el farmacéutico:
No cubrir el recuadro de ALERTA con la etiqueta de la farmacia.
ALERTA: Infórmese sobre los medicamentos que
NO DEBEN tomarse con Vosevi