Fabricante de medicamentos: Eli Lilly and Company (Updated: 2024-11-13)
ASPECTOS DESTACADOS DE LA INFORMACIÓN DE PRESCRIPCIÓN
VERZENIO® (abemaciclib) comprimidos, para administración oral
Aprobación inicial en EE. UU.: 2017
INDICACIONES Y USO
VERZENIO® es un inhibidor de la cinasa indicado para:
- en combinación con terapia endocrina (tamoxifeno o un inhibidor de la aromatasa) para el tratamiento adyuvante de pacientes adultas con cáncer de mama precoz, receptor hormonal (RH)-positivo, receptor 2 del factor de crecimiento epidérmico humano (HER2)-negativo, ganglio linfático positivo, con alto riesgo de recurrencia. (1.1, 14.1)
- en combinación con un inhibidor de la aromatasa como terapia inicial basada en endocrinología para el tratamiento de pacientes adultas con cáncer de mama avanzado o metastásico, receptor hormonal (RH)-positivo, receptor 2 del factor de crecimiento epidérmico humano (HER2)-negativo. (1.2)
- en combinación con fulvestrant para el tratamiento de pacientes adultas con cáncer de mama avanzado o metastásico, receptor hormonal (RH)-positivo, receptor 2 del factor de crecimiento epidérmico humano (HER2)-negativo, con progresión de la enfermedad después de la terapia endocrina. (1.2)
- como monoterapia para el tratamiento de pacientes adultas con cáncer de mama avanzado o metastásico, RH-positivo, HER2-negativo, con progresión de la enfermedad después de la terapia endocrina y quimioterapia previa en el contexto metastásico. (1.2)
POSOLOGÍA Y ADMINISTRACIÓN
Los comprimidos de VERZENIO se administran por vía oral con o sin alimentos. (2.1)
- Dosis inicial recomendada en combinación con fulvestrant, tamoxifeno o un inhibidor de la aromatasa: 150 mg dos veces al día. (2.1)
- Dosis inicial recomendada como monoterapia: 200 mg dos veces al día. (2.1)
- Puede ser necesaria la interrupción de la dosificación o la reducción de la dosis en función de la seguridad y la tolerabilidad individuales. (2.2)
PRESENTACIONES Y CONCENTRACIONES
Comprimidos: 50 mg, 100 mg, 150 mg y 200 mg. (3)
CONTRAINDICACIONES
Ninguna. (4)
ADVERTENCIAS Y PRECAUCIONES
- Diarrea: VERZENIO puede causar casos graves de diarrea, asociados con deshidratación e infección. Indique a los pacientes que, ante el primer signo de heces blandas, inicien un tratamiento antidiarreico, aumenten la ingesta de líquidos por vía oral y notifiquen a su médico. (2.2, 5.1)
- Neutropenia: Controle los hemogramas completos antes de iniciar el tratamiento con VERZENIO, cada 2 semanas durante los 2 primeros meses, mensualmente durante los 2 meses siguientes y según esté clínicamente indicado. (2.2, 5.2)
- Enfermedad pulmonar intersticial (EPI)/Neumonitis: Se han notificado casos graves y mortales de EPI/neumonitis. Controle los síntomas clínicos o los cambios radiológicos que indiquen EPI/neumonitis. Suspenda permanentemente VERZENIO en todos los pacientes con EPI o neumonitis de grado 3 o 4. (2.2, 5.3)
- Hepatotoxicidad: Se han observado aumentos en los niveles de transaminasas séricas. Realice pruebas de función hepática (PFL) antes de iniciar el tratamiento con VERZENIO. Controle las PFL cada dos semanas durante los dos primeros meses, mensualmente durante los 2 meses siguientes y según esté clínicamente indicado. (2.2, 5.4)
- Tromboembolismo venoso: Controle a los pacientes para detectar signos y síntomas de trombosis y embolia pulmonar y trátelos según sea médicamente apropiado. (2.2, 5.5)
- Toxicidad embriofetal: Puede causar daño fetal. Avise a las pacientes del riesgo potencial para el feto y del uso de métodos anticonceptivos eficaces. (5.6, 8.1, 8.3)
REACCIONES ADVERSAS
Las reacciones adversas más frecuentes (incidencia ≥20%) fueron diarrea, neutropenia, náuseas, dolor abdominal, infecciones, fatiga, anemia, leucopenia, disminución del apetito, vómitos, cefalea, alopecia y trombocitopenia. (6)
Para notificar SOSPECHAS DE REACCIONES ADVERSAS, póngase en contacto con Eli Lilly and Company en el 1-800-LillyRx (1-800-545-5979) o con la FDA en el 1-800-FDA-1088 o en www.fda.gov/medwatch.
INTERACCIONES MEDICAMENTOSAS
Consulte el apartado 17 para obtener información sobre el ASESORAMIENTO AL PACIENTE y el etiquetado del paciente aprobado por la FDA.
Revisado: 11/2024
Tabla de contenido
INFORMACIÓN COMPLETA DE PRESCRIPCIÓN: CONTENIDO*
1 INDICACIONES Y USO
1.1 Cáncer de mama precoz
1.2 Cáncer de mama avanzado o metastásico
2 POSOLOGÍA Y ADMINISTRACIÓN
2.1 Dosis y régimen recomendados
2.2 Modificación de la dosis
3 FORMAS Y CONCENTRACIONES FARMACÉUTICAS
4 CONTRAINDICACIONES
5 ADVERTENCIAS Y PRECAUCIONES
5.1 Diarrea
5.2 Neutropenia
5.3 Enfermedad pulmonar intersticial (EPI) o neumonitis
5.4 Hepatotoxicidad
5.5 Tromboembolismo venoso
5.6 Toxicidad embriofetal
6 REACCIONES ADVERSAS
6.1 Experiencia en estudios clínicos
6.2 Experiencia postcomercialización
7 INTERACCIONES MEDICAMENTOSAS
7.1 Efecto de otros medicamentos sobre VERZENIO
8 USO EN POBLACIONES ESPECÍFICAS
8.1 Embarazo
8.2 Lactancia
8.3 Mujeres y hombres en edad fértil
8.4 Uso pediátrico
8.5 Uso geriátrico
8.6 Insuficiencia renal
8.7 Insuficiencia hepática
11 DESCRIPCIÓN
12 FARMACOLOGÍA CLÍNICA
12.1 Mecanismo de acción
12.2 Farmacodinamia
12.3 Farmacocinética
13 TOXICOLOGÍA NO CLÍNICA
13.1 Carcinogénesis, mutagénesis, deterioro de la fertilidad
13.2 Toxicología y/o farmacología animal
14 ESTUDIOS CLÍNICOS
14.1 Cáncer de mama precoz
14.2 Cáncer de mama avanzado o metastásico
16 PRESENTACIÓN/CONSERVACIÓN Y MANIPULACIÓN
17 INFORMACIÓN PARA EL PACIENTE
- *
- Las secciones o subsecciones omitidas de la información completa de prescripción no se enumeran.
1 INDICACIONES Y USO
1.1 Cáncer de mama precoz
VERZENIO® (abemaciclib) está indicado:
- en combinación con terapia endocrina (tamoxifeno o un inhibidor de la aromatasa) para el tratamiento adyuvante de pacientes adultas con cáncer de mama precoz, receptor hormonal (RH)-positivo, receptor 2 del factor de crecimiento epidérmico humano (HER2)-negativo, ganglio-positivo, con alto riesgo de recurrencia [véase Estudios Clínicos (14.1)].
1.2 Cáncer de mama avanzado o metastásico
VERZENIO (abemaciclib) está indicado:
- en combinación con un inhibidor de la aromatasa como terapia inicial basada en endocrinología para el tratamiento de pacientes adultas con cáncer de mama avanzado o metastásico, receptor hormonal (RH)-positivo, receptor 2 del factor de crecimiento epidérmico humano (HER2)-negativo.
- en combinación con fulvestrant para el tratamiento de pacientes adultas con cáncer de mama avanzado o metastásico, receptor hormonal (RH)-positivo, receptor 2 del factor de crecimiento epidérmico humano (HER2)-negativo con progresión de la enfermedad después de la terapia endocrina.
- como monoterapia para el tratamiento de pacientes adultas con cáncer de mama avanzado o metastásico, RH-positivo, HER2-negativo con progresión de la enfermedad después de la terapia endocrina y quimioterapia previa en el contexto metastásico.
2 DOSIS Y ADMINISTRACIÓN
2.1 Dosis y régimen recomendados
- Cuando se usa en combinación con fulvestrant, tamoxifeno o un inhibidor de la aromatasa, la dosis recomendada de VERZENIO es de 150 mg administrada por vía oral dos veces al día. Consulte la información completa de prescripción para obtener la dosis recomendada del fulvestrant, tamoxifeno o inhibidor de la aromatasa que se esté utilizando.
- Las mujeres pre/perimenopáusicas y los hombres tratados con la combinación de VERZENIO más un inhibidor de la aromatasa deben recibir tratamiento con un agonista de la hormona liberadora de gonadotropina (GnRH) de acuerdo con las normas actuales de la práctica clínica.
- Las mujeres pre/perimenopáusicas tratadas con la combinación de VERZENIO más fulvestrant deben recibir tratamiento con un GnRH de acuerdo con las normas actuales de la práctica clínica.
- Cuando se usa como monoterapia, la dosis recomendada de VERZENIO es de 200 mg administrada por vía oral dos veces al día.
- Para el cáncer de mama precoz, continúe con VERZENIO hasta completar 2 años de tratamiento o hasta la recurrencia de la enfermedad o una toxicidad inaceptable.
- Para el cáncer de mama avanzado o metastásico, continúe el tratamiento hasta la progresión de la enfermedad o una toxicidad inaceptable.
VERZENIO puede tomarse con o sin alimentos [véase Farmacología clínica (12.3)].
Indique a los pacientes que tomen sus dosis de VERZENIO aproximadamente a la misma hora todos los días.
Si el paciente vomita u olvida una dosis de VERZENIO, indíquele que tome la siguiente dosis a la hora programada. Indique a los pacientes que traguen los comprimidos de VERZENIO enteros y que no los mastiquen, trituren ni partan antes de tragarlos. Indique a los pacientes que no ingieran los comprimidos de VERZENIO si están rotos, agrietados o de alguna otra manera no intactos.
2.2 Modificación de la dosis
Modificaciones de la dosis para reacciones adversas
Las modificaciones de la dosis de VERZENIO recomendadas para las reacciones adversas se proporcionan en las tablas 1–7. Suspenda VERZENIO para los pacientes que no puedan tolerar 50 mg dos veces al día.
| Nivel de dosis | Dosis de VERZENIO Combinación con fulvestrant, tamoxifeno o un inhibidor de la aromatasa |
Dosis de VERZENIO para monoterapia |
| Dosis inicial recomendada | 150 mg dos veces al día | 200 mg dos veces al día |
| Primera reducción de la dosis | 100 mg dos veces al día | 150 mg dos veces al día |
| Segunda reducción de la dosis | 50 mg dos veces al día | 100 mg dos veces al día |
| Tercera reducción de la dosis | no aplicable | 50 mg dos veces al día |
|
Abreviatura: CTCAE = Criterios de terminología común para eventos adversos. |
|
|
a Si se requieren factores de crecimiento de células sanguíneas, suspenda la dosis de VERZENIO durante al menos 48 horas después de la última dosis del factor de crecimiento de células sanguíneas y hasta que la toxicidad se resuelva a ≤Grado 2. Reanude con la dosis inferior siguiente a menos que ya se haya realizado para la toxicidad que llevó al uso del factor de crecimiento. El uso del factor de crecimiento según las directrices de tratamiento actuales. |
|
| Controle los hemogramas completos antes de comenzar el tratamiento con VERZENIO, cada 2 semanas durante los primeros 2 meses, mensualmente durante los siguientes 2 meses y según esté clínicamente indicado. | |
| Grado CTCAE | Modificaciones de la dosis de VERZENIO |
| Grado 1 o 2 | No se requiere modificación de la dosis. |
| Grado 3 | Suspenda la dosis hasta que la toxicidad se resuelva a ≤Grado 2. No se requiere reducción de la dosis. |
| Grado 3 recurrente o Grado 4 | Suspenda la dosis hasta que la toxicidad se resuelva a ≤Grado 2. Reanude con la dosis inferior siguiente. |
| Ante el primer signo de heces blandas, iniciar tratamiento con agentes antidiarreicos y aumentar la ingesta de líquidos orales. | |
| Grado CTCAE | Modificaciones de la dosis de VERZENIO |
| Grado 1 | No se requiere modificación de la dosis. |
| Grado 2 | Si la toxicidad no se resuelve en 24 horas a ≤Grado 1, suspender la dosis hasta su resolución. No se requiere reducción de la dosis. |
| Grado 2 que persiste o recidiva después de reanudar la misma dosis a pesar de las medidas de apoyo máximas | Suspender la dosis hasta que la toxicidad se resuelva a ≤Grado 1. Reanudar con la dosis inmediatamente inferior. |
| Grado 3 o 4 o requiere hospitalización | Suspender la dosis hasta que la toxicidad se resuelva a ≤Grado 1. Reanudar con la dosis inmediatamente inferior. |
|
Abreviaturas: ALT = alanina aminotransferasa, AST = aspartato aminotransferasa, ULN = límite superior de la normalidad. |
|
| Controlar ALT, AST y bilirrubina sérica antes de iniciar el tratamiento con VERZENIO, cada 2 semanas durante los 2 primeros meses, mensualmente durante los 2 meses siguientes y según indicación clínica. | |
| Grado CTCAE para ALT y AST | Modificaciones de la dosis de VERZENIO |
| Grado 1 (>ULN-3.0 x ULN) Grado 2 (>3.0-5.0 x ULN), SIN aumento de bilirrubina total por encima de 2 x ULN |
No se requiere modificación de la dosis. |
| Grado 2 persistente o recurrente, o Grado 3 (>5.0-20.0 x ULN), SIN aumento de bilirrubina total por encima de 2 x ULN | Suspender la dosis hasta que la toxicidad se resuelva a los valores basales o al Grado 1. Reanudar con la dosis inmediatamente inferior. |
| Elevación de AST y/o ALT >3 x ULN CON bilirrubina total >2 x ULN, en ausencia de colestasis | Interrumpir VERZENIO. |
| Grado 4 (>20.0 x ULN) | Interrumpir VERZENIO. |
| Grado CTCAE | Modificaciones de la dosis de VERZENIO |
| Grado 1 o 2 | No se requiere modificación de la dosis. |
| Toxicidad de Grado 2 persistente o recurrente que no se resuelve con las medidas de apoyo máximas en un plazo de 7 días a los valores basales o al Grado 1 | Suspender la dosis hasta que la toxicidad se resuelva a los valores basales o ≤Grado 1. Reanudar con la dosis inmediatamente inferior. |
| Grado 3 o 4 | Interrumpir VERZENIO. |
| Grado CTCAE | Modificaciones de la dosis de VERZENIO |
| Cáncer de mama precoz | |
| Cualquier grado | Suspender la dosis y tratar según indicación clínica. Reanudar VERZENIO cuando el paciente esté clínicamente estable. |
| Cáncer de mama avanzado o metastásico | |
| Grado 1 o 2 | No se requiere modificación de la dosis. |
| Grado 3 o 4 | Suspender la dosis y tratar según indicación clínica. Reanudar VERZENIO cuando el paciente esté clínicamente estable. |
|
a Excluyendo diarrea, toxicidad hematológica, hepatotoxicidad, EIP/neumonitis y TEP. |
|
| Grado CTCAE | Modificaciones de la dosis de VERZENIO |
| Grado 1 o 2 | No se requiere modificación de la dosis. |
| Toxicidad de Grado 2 persistente o recurrente que no se resuelve con las medidas de apoyo máximas dentro de 7 días a la línea de base o Grado 1 | Suspender la dosis hasta que la toxicidad se resuelva a la línea de base o ≤Grado 1. Reanudar con la dosis inferior siguiente. |
| Grado 3 o 4 | Suspender la dosis hasta que la toxicidad se resuelva a la línea de base o ≤Grado 1. Reanudar con la dosis inferior siguiente. |
Consulte la información completa de prescripción para fulvestrant, tamoxifeno o un inhibidor de la aromatasa coadministrados para obtener información sobre modificaciones de la dosis y otra información de seguridad relevante.
Modificación de la dosis para su uso con inhibidores potentes y moderados del CYP3A
Evite el uso concomitante del inhibidor potente del CYP3A ketoconazol.
Con el uso concomitante de inhibidores potentes del CYP3A que no sean ketoconazol, en pacientes con dosis iniciales recomendadas de 200 mg dos veces al día o 150 mg dos veces al día, reduzca la dosis de VERZENIO a 100 mg dos veces al día. En pacientes que han tenido una reducción de la dosis a 100 mg dos veces al día debido a reacciones adversas, reduzca aún más la dosis de VERZENIO a 50 mg dos veces al día. Si un paciente que toma VERZENIO suspende un inhibidor del CYP3A, aumente la dosis de VERZENIO (después de 3-5 semividas del inhibidor) a la dosis que se usaba antes de comenzar el inhibidor potente [véase Interacciones medicamentosas (7.1) y Farmacología clínica (12.3)].
Con el uso concomitante de inhibidores moderados del CYP3A, controle las reacciones adversas y considere reducir la dosis de VERZENIO en incrementos de 50 mg según se muestra en la Tabla 1, si es necesario.
Modificación de la dosis para pacientes con insuficiencia hepática grave
Para pacientes con insuficiencia hepática grave (Child Pugh-C), reduzca la frecuencia de dosificación de VERZENIO a una vez al día [véase Uso en poblaciones específicas (8.7) y Farmacología clínica (12.3)].
Consulte la información completa de prescripción para el fulvestrant, tamoxifeno o inhibidor de la aromatasa coadministrados para conocer los requisitos de modificación de la dosis para la insuficiencia hepática grave.
3 FORMAS DE DOSIFICACIÓN Y CONCENTRACIONES
Comprimidos de 50 mg: comprimido ovalado beige con “Lilly” grabado en relieve en un lado y “50” en el otro lado.
Comprimidos de 100 mg: comprimido ovalado blanco o casi blanco con “Lilly” grabado en relieve en un lado y “100” en el otro lado.
Comprimidos de 150 mg: comprimido ovalado amarillo con “Lilly” grabado en relieve en un lado y “150” en el otro lado.
Comprimidos de 200 mg: comprimido ovalado beige con “Lilly” grabado en relieve en un lado y “200” en el otro lado.
4 CONTRAINDICACIONES
Ninguna.
5 ADVERTENCIAS Y PRECAUCIONES
5.1 Diarrea
En pacientes tratados con VERZENIO se produjo diarrea grave asociada con deshidratación e infección.
En cuatro ensayos clínicos en 3691 pacientes, la diarrea se produjo en un 81% a un 90% de los pacientes que recibieron VERZENIO. La diarrea de grado 3 se produjo en un 8% a un 20% de los pacientes que recibieron VERZENIO [véase Reacciones adversas (6.1)].
La mayoría de los pacientes experimentaron diarrea durante el primer mes de tratamiento con VERZENIO. El tiempo medio hasta el inicio del primer episodio de diarrea osciló entre 6 y 8 días; y la duración media de la diarrea de grado 2 y de grado 3 osciló entre 6 y 11 días y entre 5 y 8 días, respectivamente. En los ensayos, entre el 19% y el 26% de los pacientes con diarrea requirieron una interrupción de la dosis de VERZENIO y entre el 13% y el 23% requirieron una reducción de la dosis.
Indique a los pacientes que inicien un tratamiento antidiarreico como loperamida a la primera señal de heces blandas, que aumenten la ingesta de líquidos por vía oral y que notifiquen a su proveedor de atención médica para obtener más instrucciones y un seguimiento adecuado [véase Información para el paciente (17)]. En caso de diarrea de grado 3 o 4, o diarrea que requiera hospitalización, interrumpa el tratamiento con VERZENIO hasta que la toxicidad se resuelva a ≤grado 1, y luego reanude el tratamiento con VERZENIO a la dosis inmediatamente inferior [véase Posología y administración (2.2)].
5.2 Neutropenia
Se produjo neutropenia, incluida la neutropenia febril y la sepsis neutropénica mortal, en pacientes tratados con VERZENIO.
En cuatro ensayos clínicos en 3691 pacientes, la neutropenia se produjo en un 37% a un 46% de los pacientes que recibieron VERZENIO. Se produjo una disminución de grado ≥3 en el recuento de neutrófilos (según los hallazgos de laboratorio) en un 19% a un 32% de los pacientes que recibieron VERZENIO. En los ensayos, el tiempo medio hasta el primer episodio de neutropenia de grado ≥3 osciló entre 29 y 33 días, y la duración media de la neutropenia de grado ≥3 osciló entre 11 y 16 días [véase Reacciones adversas (6.1)].
Se ha notificado neutropenia febril en <1% de los pacientes expuestos a VERZENIO en los ensayos. Se observaron dos muertes por sepsis neutropénica en MONARCH 2. Informe a los pacientes que informen inmediatamente cualquier episodio de fiebre a su proveedor de atención médica [véase Información para el paciente (17)].
Controle los hemogramas completos antes de iniciar el tratamiento con VERZENIO, cada 2 semanas durante los 2 primeros meses, mensualmente durante los 2 meses siguientes y según esté clínicamente indicado. Se recomienda la interrupción de la dosis, la reducción de la dosis o el retraso en el inicio de los ciclos de tratamiento para los pacientes que presenten neutropenia de grado 3 o 4 [véase Posología y administración (2.2)].
5.3 Enfermedad pulmonar intersticial (EPI) o neumonitis
Puede producirse enfermedad pulmonar intersticial (EPI) o neumonitis grave, potencialmente mortal o mortal en pacientes tratados con VERZENIO y otros inhibidores de CDK4/6. En pacientes tratados con VERZENIO con cáncer de mama precoz (monarchE, N=2791), el 3% de los pacientes experimentaron EPI o neumonitis de cualquier grado: el 0,4% fueron de grado 3 o 4 y hubo una muerte (0,1%). En pacientes tratados con VERZENIO con cáncer de mama avanzado o metastásico (N=900) (MONARCH 1, MONARCH 2, MONARCH 3), el 3,3% de los pacientes tratados con VERZENIO presentaron EPI o neumonitis de cualquier grado: el 0,6% presentaron grado 3 o 4, y el 0,4% presentaron resultados mortales. Se han observado casos adicionales de EPI o neumonitis en el período posterior a la comercialización, con notificaciones de muertes [véase Reacciones adversas (6.2)].
Controle a los pacientes para detectar síntomas pulmonares indicativos de EPI o neumonitis. Los síntomas pueden incluir hipoxia, tos, disnea o infiltrados intersticiales en las exploraciones radiológicas. Las causas infecciosas, neoplásicas y de otro tipo de dichos síntomas deben excluirse mediante las investigaciones apropiadas.
Se recomienda la interrupción de la dosis o la reducción de la dosis para los pacientes que presenten EPI o neumonitis de grado 2 persistente o recurrente. Suspenda permanentemente VERZENIO en todos los pacientes con EPI o neumonitis de grado 3 o 4 [véase Posología y administración (2.2)].
5.4 Hepatotoxicidad
Se notificaron ALT (2% a 6%) y AST (2% a 3%) de grado ≥3 en pacientes que recibieron VERZENIO.
En tres ensayos clínicos en 3559 pacientes (monarchE, MONARCH 2, MONARCH 3), el tiempo medio hasta el inicio del aumento de ALT de grado ≥3 osciló entre 57 y 87 días y el tiempo medio hasta la resolución a grado <3 fue de 13 a 14 días. El tiempo medio hasta el inicio del aumento de AST de grado ≥3 osciló entre 71 y 185 días y el tiempo medio hasta la resolución a grado <3 osciló entre 11 y 15 días.
Controle las pruebas de función hepática (PFL) antes de iniciar el tratamiento con VERZENIO, cada 2 semanas durante los 2 primeros meses, mensualmente durante los 2 meses siguientes y según esté clínicamente indicado. Se recomienda la interrupción de la dosis, la reducción de la dosis, la suspensión de la dosis o el retraso en el inicio de los ciclos de tratamiento para los pacientes que presenten elevación persistente o recurrente de transaminasas hepáticas de grado 2 o de cualquier grado 3 o 4 [véase Posología y administración (2.2)].
5.5 Tromboembolismo venoso
En tres ensayos clínicos en 3559 pacientes (monarchE, MONARCH 2, MONARCH 3), se notificaron acontecimientos tromboembólicos venosos en un 2% a un 5% de los pacientes tratados con VERZENIO. Los acontecimientos tromboembólicos venosos incluyeron trombosis venosa profunda, embolia pulmonar, trombosis venosa pélvica, trombosis del seno venoso cerebral, trombosis de la vena subclavia y axilar y trombosis de la vena cava inferior. En los ensayos clínicos, se han notificado muertes por tromboembolismo venoso en pacientes tratados con VERZENIO.
VERZENIO no se ha estudiado en pacientes con cáncer de mama precoz que tenían antecedentes de tromboembolismo venoso. Controle a los pacientes para detectar signos y síntomas de trombosis venosa y embolia pulmonar y trátelos según sea médicamente apropiado. Se recomienda la interrupción de la dosis para los pacientes con cáncer de mama precoz con cualquier grado de acontecimiento tromboembólico venoso y para los pacientes con cáncer de mama avanzado o metastásico con un acontecimiento tromboembólico venoso de grado 3 o 4 [véase Posología y administración (2.2)].
5.6 Toxicidad embriofetal
Según los hallazgos de los estudios en animales y el mecanismo de acción, VERZENIO puede causar daño fetal cuando se administra a una mujer embarazada. En estudios de reproducción en animales, la administración de abemaciclib a ratas embarazadas durante el período de organogénesis provocó teratogenicidad y disminución del peso fetal a exposiciones maternas similares a la exposición clínica humana en función del área bajo la curva (AUC) a la dosis máxima recomendada en humanos.
Avise a las mujeres embarazadas del riesgo potencial para el feto. Avise a las mujeres en edad fértil que utilicen un método anticonceptivo eficaz durante el tratamiento con VERZENIO y durante 3 semanas después de la última dosis [véase Uso en poblaciones específicas (8.1, 8.3) y Farmacología clínica (12.1)].
6 REACCIONES ADVERSAS
Las siguientes reacciones adversas se discuten con mayor detalle en otras secciones del etiquetado:
- Diarrea [ver Advertencias y Precauciones (5.1)].
- Neutropenia [ver Advertencias y Precauciones (5.2)].
- Enfermedad pulmonar intersticial (ILD) o neumonitis [ver Advertencias y Precauciones (5.3)].
- Hepatotoxicidad [ver Advertencias y Precauciones (5.4)].
- Tromboembolismo venoso [ver Advertencias y Precauciones (5.5)].
6.1 Experiencia en estudios clínicos
Debido a que los ensayos clínicos se llevan a cabo en condiciones muy variadas, las tasas de reacciones adversas observadas en los ensayos clínicos de un fármaco no se pueden comparar directamente con las tasas en los ensayos clínicos de otro fármaco y pueden no reflejar las tasas observadas en la práctica.
La población de seguridad descrita en las Advertencias y Precauciones refleja la exposición a VERZENIO en 3691 pacientes de cuatro ensayos clínicos: monarchE, MONARCH 1, MONARCH 2 y MONARCH 3. La población de seguridad incluye la exposición a VERZENIO como agente único a 200 mg dos veces al día en 132 pacientes en MONARCH 1 y a VERZENIO a 150 mg dos veces al día en 3559 pacientes administrados en combinación con fulvestrant, tamoxifeno o un inhibidor de la aromatasa en monarchE, MONARCH 2 y MONARCH 3. La duración mediana de la exposición varió de 4.5 meses en MONARCH 1 a 24 meses en monarchE. Las reacciones adversas más comunes (incidencia ≥20%) en todos los ensayos clínicos fueron: diarrea, neutropenia, náuseas, dolor abdominal, infecciones, fatiga, anemia, leucopenia, disminución del apetito, vómitos, dolor de cabeza, alopecia y trombocitopenia.
Cáncer de mama en estadio inicial
monarchE: VERZENIO en combinación con tamoxifeno o un inhibidor de la aromatasa como tratamiento adyuvante
Pacientes adultos con cáncer de mama en estadio inicial, HR-positivo, HER2-negativo, con ganglios positivos y un alto riesgo de recurrencia
La seguridad de VERZENIO se evaluó en monarchE, un estudio de 5591 pacientes adultos que recibieron VERZENIO más terapia endocrina (tamoxifeno o un inhibidor de la aromatasa) o terapia endocrina (tamoxifeno o un inhibidor de la aromatasa) sola [ver Estudios Clínicos (14.1)]. Los pacientes fueron asignados aleatoriamente para recibir 150 mg de VERZENIO por vía oral, dos veces al día, más tamoxifeno o un inhibidor de la aromatasa, o tamoxifeno o un inhibidor de la aromatasa, durante dos años o hasta que se cumplieran los criterios de interrupción. La duración mediana del tratamiento con VERZENIO fue de 24 meses.
Las reacciones adversas de Grado 3 o 4 más frecuentemente reportadas (≥5%) fueron neutropenia, leucopenia, diarrea y linfopenia.
Ocurrieron reacciones adversas fatales en el 0.8% de los pacientes que recibieron VERZENIO más terapia endocrina (tamoxifeno o un inhibidor de la aromatasa), incluyendo: insuficiencia cardíaca (0.1%), paro cardíaco, infarto de miocardio, fibrilación ventricular, hemorragia cerebral, accidente cerebrovascular, neumonitis, hipoxia, diarrea y trombosis de la arteria mesentérica (0.03% cada una).
Se informó la interrupción permanente del tratamiento con VERZENIO debido a una reacción adversa en el 19% de los pacientes que recibieron VERZENIO más tamoxifeno o un inhibidor de la aromatasa. Del grupo de pacientes que recibió tamoxifeno o un inhibidor de la aromatasa, el 1% interrumpió permanentemente debido a una reacción adversa. Las reacciones adversas más comunes que llevaron a la interrupción de VERZENIO fueron diarrea (5%), fatiga (2%) y neutropenia (0.9%).
La interrupción de la dosis de VERZENIO debido a una reacción adversa ocurrió en el 62% de los pacientes que recibieron VERZENIO más tamoxifeno o inhibidores de la aromatasa. Las reacciones adversas que llevaron a la interrupción de la dosis de VERZENIO en ≥5% de los pacientes fueron diarrea (20%), neutropenia (16%), leucopenia (7%) y fatiga (5%).
La reducción de la dosis de VERZENIO debido a una reacción adversa ocurrió en el 44% de los pacientes que recibieron VERZENIO más terapia endocrina (tamoxifeno o un inhibidor de la aromatasa). Las reacciones adversas que llevaron a la reducción de la dosis de VERZENIO en ≥5% fueron diarrea (17%), neutropenia (8%) y fatiga (5%).
Las reacciones adversas más comunes reportadas (≥20%) en el brazo de VERZENIO más tamoxifeno o un inhibidor de la aromatasa y ≥2% más altas que el brazo de tamoxifeno o un inhibidor de la aromatasa fueron: diarrea, infecciones, neutropenia, fatiga, leucopenia, náuseas, anemia y dolor de cabeza. Las reacciones adversas se muestran en Tabla 8 y las anormalidades de laboratorio se muestran en Tabla 9.
|
a Incluye las siguientes reacciones adversas fatales: diarrea (n = 1) e infecciones (n = 4) |
||||||
|
b Incluye las siguientes reacciones adversas fatales: infecciones (n = 5) |
||||||
|
c Incluye úlcera bucal, inflamación de la mucosa, dolor orofaríngeo, estomatitis. |
||||||
|
d Incluye todos los términos preferidos reportados que son parte de la clase de órgano del sistema de Infecciones e Infestaciones. Las infecciones más comunes (> 5%) incluyen infección del tracto respiratorio superior, infección del tracto urinario y nasofaringitis. |
||||||
|
e Incluye astenia, fatiga. |
||||||
|
f Incluye erupción exfoliativa, erupción mucocutánea, erupción, erupción eritematosa, erupción folicular, erupción generalizada, erupción macular, erupción maculopapular, erupción maculovesicular, erupción morbiliforme, erupción papular, erupción papuloescamosa, erupción pruriginosa, erupción vesicular, erupción vulvovaginal. |
||||||
| VERZENIO Plus Tamoxifeno o un Inhibidor de la Aromatasa N=2791 |
Tamoxifeno o un Inhibidor de la Aromatasa N=2800 |
|||||
| Todos los Gradosa % |
Grado 3 % |
Grado 4 % |
Todos los Gradosb % |
Grado 3 % |
Grado 4 % |
|
| Trastornos Gastrointestinales | ||||||
| Diarrea | 84 | 8 | 0 | 9 | 0.2 | 0 |
| Náuseas | 30 | 0.5 | 0 | 9 | <0.1 | 0 |
| Vómitos | 18 | 0.5 | 0 | 4.6 | 0.1 | 0 |
| Estomatitisc | 14 | 0.1 | 0 | 5 | 0 | 0 |
| Infecciones e Infestaciones | ||||||
| Infeccionesd | 51 | 4.9 | 0.6 | 39 | 2.7 | 0.1 |
| Trastornos Generales y Alteraciones en el Sitio de Administración | ||||||
| Fatigae | 41 | 2.9 | 0 | 18 | 0.1 | 0 |
| Trastornos del Sistema Nervioso | ||||||
| Dolor de cabeza | 20 | 0.3 | 0 | 15 | 0.2 | 0 |
| Mareos | 11 | 0.1 | 0 | 7 | <0.1 | 0 |
| Trastornos del Metabolismo y la Nutrición | ||||||
| Disminución del apetito | 12 | 0.6 | 0 | 2.4 | <0.1 | 0 |
| Trastornos de la Piel y del Tejido Subcutáneo | ||||||
| Rashf | 11 | 0.4 | 0 | 4.5 | 0 | 0 |
| Alopecia | 11 | 0 | 0 | 2.7 | 0 | 0 |
Las reacciones adversas clínicamente relevantes en <10% de los pacientes que recibieron VERZENIO en combinación con tamoxifeno o un inhibidor de la aromatasa en monarchE incluyen:
- Prurito-9%
- Dispepsia-8%
- Trastorno ungueal-6% (incluye trastorno del lecho ungueal, inflamación del lecho ungueal, decoloración ungueal, trastorno ungueal, distrofia ungueal, pigmentación ungueal, estrías ungueales, toxicidad ungueal, onicálgia, onicoclasis, onicólisis, oniquamadesis)
- Aumento de la lagrimación-6%
- Disgeusia-5%
- Enfermedad pulmonar intersticial (EPI)/neumonitis-3% (incluye neumonitis, neumonitis por radiación, enfermedad pulmonar intersticial, fibrosis pulmonar, neumonía organizada, fibrosis por radiación – pulmón, opacidad pulmonar, sarcoidosis)
- Eventos tromboembólicos venosos (ETV)-3% (incluye trombosis en el sitio de catéter, trombosis venosa cerebral, trombosis venosa profunda, trombosis relacionada con el dispositivo, embolia, trombosis de la vena hepática, oclusión de la vena yugular, trombosis de la vena yugular, trombosis de la vena ovárica, trombosis de la vena porta, embolia pulmonar, trombosis de la vena subclavia, trombosis venosa en extremidades)
| VERZENIO Más Tamoxifeno o un Inhibidor de la Aromatasa N=2791 |
Tamoxifeno o un Inhibidor de la Aromatasa N=2800 |
|||||
| Todos los grados % |
Grado 3 % |
Grado 4 % |
Todos los grados % |
Grado 3 % |
Grado 4 % |
|
| Creatinina aumentada | 99 | 0.5 | 0 | 91 | <0.1 | 0 |
| Leucocitos disminuidos | 89 | 19 | <0.1 | 28 | 1.1 | 0 |
| Recuento de neutrófilos disminuido | 84 | 18 | 0.7 | 23 | 1.6 | 0.3 |
| Anemia | 68 | 1.0 | 0 | 17 | 0.1 | 0 |
| Recuento de linfocitos disminuido | 59 | 13 | 0.2 | 24 | 2.4 | 0.1 |
| Recuento de plaquetas disminuido | 37 | 0.7 | 0.2 | 10 | 0.1 | 0.1 |
| Alanina aminotransferasa aumentada | 37 | 2.5 | <0.1 | 24 | 1.2 | 0 |
| Aspartato aminotransferasa aumentada | 31 | 1.5 | <0.1 | 18 | 0.9 | 0 |
| Hipopotasemia | 11 | 1.2 | 0.1 | 3.8 | 0.1 | 0.1 |
Cáncer de mama avanzado o metastásico
MONARCH 3: VERZENIO en combinación con un inhibidor de la aromatasa (Anastrozol o Letrozol) como terapia endocrina inicial
Mujeres posmenopáusicas con cáncer de mama localmente recurrente o metastásico, HR-positivo, HER2-negativo sin terapia sistémica previa en este contexto de la enfermedad
La seguridad de VERZENIO se evaluó en MONARCH 3, un estudio de 488 mujeres que recibieron VERZENIO más un inhibidor de la aromatasa o placebo más un inhibidor de la aromatasa [véase Estudios clínicos (14.2)]. Las pacientes fueron asignadas aleatoriamente para recibir 150 mg de VERZENIO o placebo por vía oral dos veces al día, más la elección del médico de anastrozol o letrozol una vez al día. La duración media del tratamiento fue de 15,1 meses para el brazo de VERZENIO y de 13,9 meses para el brazo de placebo.
Las reacciones adversas de Grado 3 o 4 más frecuentemente notificadas (≥5%) fueron neutropenia, diarrea, leucopenia, aumento de ALT y anemia.
Se notificaron muertes durante el tratamiento o durante el seguimiento de 30 días, independientemente de la causalidad, en 11 casos (3%) de pacientes tratadas con VERZENIO más un inhibidor de la aromatasa frente a 3 casos (2%) de pacientes tratadas con placebo más un inhibidor de la aromatasa. Las causas de muerte para las pacientes que recibieron VERZENIO más un inhibidor de la aromatasa incluyeron: 3 (0,9%) muertes de pacientes debido a la enfermedad subyacente, 3 (0,9%) debido a infección pulmonar, 3 (0,9%) debido a TEP, 1 (0,3%) debido a neumonitis y 1 (0,3%) debido a infarto cerebral.
La interrupción permanente del tratamiento debido a una reacción adversa se notificó en el 13% de las pacientes que recibieron VERZENIO más un inhibidor de la aromatasa y en el 3% de las pacientes que recibieron placebo más un inhibidor de la aromatasa. Las reacciones adversas que llevaron a la interrupción permanente para las pacientes que recibieron VERZENIO más un inhibidor de la aromatasa fueron diarrea (2%), aumento de ALT (2%), infección (1%), eventos tromboembólicos venosos (TEP) (1%), neutropenia (0,9%), insuficiencia renal (0,9%), aumento de AST (0,6%), disnea (0,6%), fibrosis pulmonar (0,6%) y anemia, erupción cutánea, disminución de peso y trombocitopenia (cada una 0,3%).
La interrupción de la dosis de VERZENIO debido a una reacción adversa se produjo en el 56% de las pacientes que recibieron VERZENIO más anastrozol o letrozol. Las reacciones adversas que llevaron a interrupciones de la dosis de VERZENIO en ≥5% de las pacientes fueron neutropenia (16%) y diarrea (15%).
Las reducciones de dosis debido a una reacción adversa se produjeron en el 43% de las pacientes que recibieron VERZENIO más anastrozol o letrozol. Las reacciones adversas que llevaron a reducciones de dosis en ≥5% de las pacientes fueron diarrea y neutropenia. Las reducciones de dosis de VERZENIO debido a diarrea de cualquier grado se produjeron en el 13% de las pacientes que recibieron VERZENIO más un inhibidor de la aromatasa en comparación con el 2% de las pacientes que recibieron placebo más un inhibidor de la aromatasa. Las reducciones de dosis de VERZENIO debido a neutropenia de cualquier grado se produjeron en el 11% de las pacientes que recibieron VERZENIO más un inhibidor de la aromatasa en comparación con el 0,6% de las pacientes que recibieron placebo más un inhibidor de la aromatasa.
Las reacciones adversas más frecuentes notificadas (≥20%) en el brazo de VERZENIO y ≥2% que en el brazo de placebo fueron: diarrea, neutropenia, fatiga, infecciones, náuseas, dolor abdominal, anemia, vómitos, alopecia, disminución del apetito y leucopenia. Las reacciones adversas se muestran en la Tabla 10 y las alteraciones de laboratorio en la Tabla 11. La incidencia de diarrea fue mayor durante el primer mes de administración de VERZENIO. El tiempo medio hasta el inicio del primer episodio de diarrea fue de 8 días, y la duración media de la diarrea para los Grados 2 y para el Grado 3 fue de 11 días y 8 días, respectivamente. La mayoría de los episodios de diarrea se recuperaron o resolvieron (88%) con tratamiento de apoyo y/o reducciones de dosis [véase Posología y administración (2.2) e Información para el paciente (17)]. El 19% de las pacientes con diarrea requirieron una omisión de la dosis y el 13% requirieron una reducción de la dosis. El tiempo medio hasta la primera reducción de dosis debido a diarrea fue de 38 días.
|
a Incluye todos los términos preferidos notificados que forman parte de la clase de órganos del sistema Infecciones e infestaciones. Las infecciones más comunes (>1%) incluyen infección de las vías respiratorias superiores, infección pulmonar y faringitis. |
||||||
| VERZENIO más Anastrozol o Letrozol N=327 |
Placebo más Anastrozol o Letrozol N=161 |
|||||
| Todos los grados % |
Grado 3 % |
Grado 4 % |
Todos los grados % |
Grado 3 % |
Grado 4 % |
|
| Trastornos gastrointestinales | ||||||
| Diarrea | 81 | 9 | 0 | 30 | 1.2 | 0 |
| Náuseas | 39 | 0.9 | 0 | 20 | 1.2 | 0 |
| Dolor abdominal | 29 | 1.2 | 0 | 12 | 1.2 | 0 |
| Vómitos | 28 | 1.2 | 0 | 12 | 1.9 | 0 |
| Estreñimiento | 16 | 0.6 | 0 | 12 | 0 | 0 |
| Infecciones e Infestaciones | ||||||
| Infeccionesa | 39 | 4.0 | 0.9 | 29 | 2.5 | 0.6 |
| Trastornos generales y alteraciones en el lugar de administración | ||||||
| Fatiga | 40 | 1.8 | 0 | 32 | 0 | 0 |
| Enfermedad tipo influenza | 10 | 0 | 0 | 8 | 0 | 0 |
| Trastornos de la piel y del tejido subcutáneo | ||||||
| Alopecia | 27 | 0 | 0 | 11 | 0 | 0 |
| Erupción | 14 | 0.9 | 0 | 5 | 0 | 0 |
| Prurito | 13 | 0 | 0 | 9 | 0 | 0 |
| Trastornos del metabolismo y de la nutrición | ||||||
| Disminución del apetito | 24 | 1.2 | 0 | 9 | 0.6 | 0 |
| Pruebas | ||||||
| Pérdida de peso | 10 | 0.6 | 0 | 3.1 | 0.6 | 0 |
| Trastornos respiratorios, torácicos y mediastínicos | ||||||
| Tos | 13 | 0 | 0 | 9 | 0 | 0 |
| Disnea | 12 | 0.6 | 0.3 | 6 | 0.6 | 0 |
| Trastornos del sistema nervioso | ||||||
| Mareo | 11 | 0.3 | 0 | 9 | 0 | 0 |
Las reacciones adversas adicionales en MONARCH 3 incluyen eventos tromboembólicos venosos (trombosis venosa profunda, embolia pulmonar y trombosis venosa pélvica), que se informaron en el 5 % de los pacientes tratados con VERZENIO más anastrozol o letrozol en comparación con el 0,6 % de los pacientes tratados con anastrozol o letrozol más placebo.
| VERZENIO más Anastrozol o Letrozol N=327 |
Placebo más Anastrozol o Letrozol N=161 |
|||||
| Anormalidad de laboratorio | Todos los grados % |
Grado 3 % |
Grado 4 % |
Todos los grados % |
Grado 3 % |
Grado 4 % |
| Creatinina aumentada | 98 | 2.2 | 0 | 84 | 0 | 0 |
| Leucocitos disminuidos | 82 | 13 | 0 | 27 | 0.6 | 0 |
| Anemia | 82 | 1.6 | 0 | 28 | 0 | 0 |
| Neutrófilos disminuidos | 80 | 19 | 2.9 | 21 | 2.6 | 0 |
| Linfocitos disminuidos | 53 | 7 | 0.6 | 26 | 1.9 | 0 |
| Plaquetas disminuidas | 36 | 1.3 | 0.6 | 12 | 0.6 | 0 |
| Alanina aminotransferasa aumentada | 48 | 6 | 0.6 | 25 | 1.9 | 0 |
| Aspartato aminotransferasa aumentada | 37 | 3.8 | 0 | 23 | 0.6 | 0 |
Aumento de Creatinina
Se ha demostrado que el abemaciclib aumenta la creatinina sérica debido a la inhibición de los transportadores de secreción tubular renal, sin afectar la función glomerular [ver Farmacología Clínica (12.3)]. En los estudios clínicos, los aumentos en la creatinina sérica (aumento medio, 0,2-0,3 mg/dL) se produjeron dentro del primer ciclo de 28 días de dosificación de VERZENIO, se mantuvieron elevados pero estables durante el período de tratamiento y fueron reversibles tras la interrupción del tratamiento. Se pueden considerar marcadores alternativos como BUN, cistatina C o FG calculada, que no se basan en la creatinina, para determinar si la función renal está deteriorada.
MONARCH 2: VERZENIO en combinación con Fulvestrant
Mujeres con cáncer de mama avanzado o metastásico, HR-positivo, HER2-negativo, con progresión de la enfermedad durante o después de la terapia endocrina adyuvante o metastásica previa
La seguridad de VERZENIO (150 mg dos veces al día) más fulvestrant (500 mg) versus placebo más fulvestrant se evaluó en MONARCH 2 [ver Estudios Clínicos (14.2)]. Los datos que se describen a continuación reflejan la exposición a VERZENIO en 441 pacientes con cáncer de mama avanzado HR-positivo, HER2-negativo que recibieron al menos una dosis de VERZENIO más fulvestrant en MONARCH 2.
La duración media del tratamiento fue de 12 meses para las pacientes que recibieron VERZENIO más fulvestrant y de 8 meses para las pacientes que recibieron placebo más fulvestrant.
Las reacciones adversas de Grado 3 o 4 más frecuentemente notificadas (≥5%) fueron neutropenia, diarrea, leucopenia, anemia e infecciones.
Se notificaron muertes durante el tratamiento o durante el seguimiento de 30 días, independientemente de la causalidad, en 18 casos (4%) de pacientes tratados con VERZENIO más fulvestrant versus 10 casos (5%) de pacientes tratados con placebo más fulvestrant. Las causas de muerte para las pacientes que recibieron VERZENIO más fulvestrant incluyeron: 7 (2%) muertes de pacientes debido a la enfermedad subyacente, 4 (0,9%) debido a sepsis, 2 (0,5%) debido a neumonitis, 2 (0,5%) debido a hepatotoxicidad y una (0,2%) debido a infarto cerebral.
La interrupción permanente del tratamiento del estudio debido a una reacción adversa se notificó en el 9% de las pacientes que recibieron VERZENIO más fulvestrant y en el 3% de las pacientes que recibieron placebo más fulvestrant. Las reacciones adversas que llevaron a la interrupción permanente para las pacientes que recibieron VERZENIO más fulvestrant fueron infección (2%), diarrea (1%), hepatotoxicidad (1%), fatiga (0,7%), náuseas (0,2%), dolor abdominal (0,2%), lesión renal aguda (0,2%) e infarto cerebral (0,2%).
La interrupción de la dosis de VERZENIO debido a una reacción adversa se produjo en el 52% de las pacientes que recibieron VERZENIO más fulvestrant. Las reacciones adversas que llevaron a interrupciones de la dosis de VERZENIO en ≥5% de las pacientes fueron diarrea (19%) y neutropenia (16%).
Las reducciones de la dosis debido a una reacción adversa se produjeron en el 43% de las pacientes que recibieron VERZENIO más fulvestrant. Las reacciones adversas que llevaron a reducciones en ≥5% de las pacientes fueron diarrea y neutropenia. Las reducciones de la dosis de VERZENIO debido a diarrea de cualquier grado se produjeron en el 19% de las pacientes que recibieron VERZENIO más fulvestrant en comparación con el 0,4% de las pacientes que recibieron placebo y fulvestrant. Las reducciones de la dosis de VERZENIO debido a neutropenia de cualquier grado se produjeron en el 10% de las pacientes que recibieron VERZENIO más fulvestrant en comparación con ninguna paciente que recibió placebo más fulvestrant.
Las reacciones adversas más frecuentes notificadas (≥20%) en el brazo de VERZENIO fueron: diarrea, fatiga, neutropenia, náuseas, infecciones, dolor abdominal, anemia, leucopenia, disminución del apetito, vómitos y dolor de cabeza. Las reacciones adversas se muestran en la Tabla 12 y las anomalías de laboratorio en la Tabla 13.
|
a Incluye dolor abdominal, dolor abdominal superior, dolor abdominal inferior, malestar abdominal, sensibilidad abdominal. |
||||||
|
b Incluye infección del tracto respiratorio superior, infección del tracto urinario, infección pulmonar, faringitis, conjuntivitis, sinusitis, infección vaginal, sepsis. |
||||||
|
c Incluye astenia, fatiga. |
||||||
| VERZENIO más Fulvestrant N=441 |
Placebo más Fulvestrant N=223 |
|||||
| Todos los Grados % |
Grado 3 % |
Grado 4 % |
Todos los Grados % |
Grado 3 % |
Grado 4 % |
|
| Trastornos Gastrointestinales | ||||||
| Diarrea | 86 | 13 | 0 | 25 | 0.4 | 0 |
| Náuseas | 45 | 2.7 | 0 | 23 | 0.9 | 0 |
| Dolor abdominala | 35 | 2.5 | 0 | 16 | 0.9 | 0 |
| Vómitos | 26 | 0.9 | 0 | 10 | 1.8 | 0 |
| Estomatitis | 15 | 0.5 | 0 | 10 | 0 | 0 |
| Infecciones e Infestaciones | ||||||
| Infeccionesb | 43 | 5 | 0.7 | 25 | 3.1 | 0.4 |
| Trastornos generales y alteraciones en el lugar de administración | ||||||
| Fatigac | 46 | 2.7 | 0 | 32 | 0.4 | 0 |
| Edema periférico | 12 | 0 | 0 | 7 | 0 | 0 |
| Pirexia | 11 | 0.5 | 0.2 | 6 | 0.4 | 0 |
| Trastornos del metabolismo y de la nutrición | ||||||
| Disminución del apetito | 27 | 1.1 | 0 | 12 | 0.4 | 0 |
| Trastornos respiratorios, torácicos y mediastínicos | ||||||
| Tos | 13 | 0 | 0 | 11 | 0 | 0 |
| Trastornos de la piel y del tejido subcutáneo | ||||||
| Alopecia | 16 | 0 | 0 | 1.8 | 0 | 0 |
| Prurito | 13 | 0 | 0 | 6 | 0 | 0 |
| Rash | 11 | 1.1 | 0 | 4.5 | 0 | 0 |
| Trastornos del sistema nervioso | ||||||
| Dolor de cabeza | 20 | 0.7 | 0 | 15 | 0.4 | 0 |
| Disgeusia | 18 | 0 | 0 | 2.7 | 0 | 0 |
| Mareo | 12 | 0.7 | 0 | 6 | 0 | 0 |
| Exploraciones complementarias | ||||||
| Disminución de peso | 10 | 0.2 | 0 | 2.2 | 0.4 | 0 |
Otras reacciones adversas en MONARCH 2 incluyen eventos tromboembólicos venosos (trombosis venosa profunda, embolia pulmonar, trombosis del seno venoso cerebral, trombosis de la vena subclavia, trombosis de la vena axilar y trombosis venosa profunda de la vena cava inferior), que se informaron en el 5 % de los pacientes tratados con VERZENIO más fulvestrant en comparación con el 0,9 % de los pacientes tratados con fulvestrant más placebo.
| VERZENIO más Fulvestrant N=441 |
Placebo más Fulvestrant N=223 |
|||||
| Todos los grados % |
Grado 3 % |
Grado 4 % |
Todos los grados % |
Grado 3 % |
Grado 4 % |
|
| Creatinina aumentada | 98 | 1.2 | 0 | 74 | 0 | 0 |
| Leucocitos disminuidos | 90 | 23 | 0.7 | 33 | 0.9 | 0 |
| Recuento de neutrófilos disminuido | 87 | 29 | 3.5 | 30 | 3.7 | 0.5 |
| Anemia | 84 | 2.6 | 0 | 34 | 0.5 | 0 |
| Recuento de linfocitos disminuido | 63 | 12 | 0.2 | 32 | 1.8 | 0 |
| Recuento de plaquetas disminuido | 53 | 0.9 | 1.2 | 15 | 0 | 0 |
| Alanina aminotransferasa aumentada | 41 | 3.9 | 0.7 | 32 | 1.4 | 0 |
| Aspartato aminotransferasa aumentada | 37 | 3.9 | 0 | 25 | 3.7 | 0.5 |
Creatinina aumentada
Se ha demostrado que el abemaciclib aumenta la creatinina sérica debido a la inhibición de los transportadores de secreción tubular renal, sin afectar la función glomerular [ver Farmacología clínica (12.3)]. En los estudios clínicos, los aumentos en la creatinina sérica (aumento medio, 0,2-0,3 mg/dL) se produjeron dentro del primer ciclo de 28 días de dosificación de VERZENIO, permanecieron elevados pero estables durante el período de tratamiento y fueron reversibles tras la interrupción del tratamiento. Se pueden considerar marcadores alternativos como BUN, cistatina C o tasa de filtración glomerular (TFG) calculada, que no se basan en la creatinina, para determinar si la función renal está deteriorada.
MONARCH 1: VERZENIO administrado como monoterapia en cáncer de mama metastásico
Pacientes con cáncer de mama metastásico HR-positivo, HER2-negativo que recibieron terapia endocrina previa y 1-2 regímenes de quimioterapia en el contexto metastásico
La seguridad de VERZENIO se evaluó en MONARCH 1, un estudio de un solo brazo, abierto y multicéntrico en 132 mujeres con cáncer de mama metastásico HR-positivo, HER2-negativo medible [ver Estudios clínicos (14.2)]. Las pacientes recibieron 200 mg de VERZENIO por vía oral dos veces al día hasta el desarrollo de una enfermedad progresiva o toxicidad inmanejable. La duración media del tratamiento fue de 4,5 meses.
Las reacciones adversas de Grado 3 o 4 más frecuentemente notificadas (≥5%) fueron diarrea, neutropenia, fatiga y leucopenia.
Se notificaron muertes debidas a reacciones adversas durante el tratamiento o durante el seguimiento de 30 días en el 2% de las pacientes. La causa de la muerte en estas pacientes se debió a infección (2 pacientes) o neumonitis (1 paciente).
Diez pacientes (8%) interrumpieron el tratamiento del estudio debido a reacciones adversas por (1 paciente cada una): dolor abdominal, trombosis arterial, aumento de la aspartato aminotransferasa (AST), aumento de la creatinina en sangre, enfermedad renal crónica, diarrea, prolongación del QT en el ECG, fatiga, fractura de cadera y linfopenia.
La interrupción de la dosis de VERZENIO debido a una reacción adversa se produjo en el 58% de las pacientes. Las reacciones adversas más frecuentes (≥5%) que llevaron a interrupciones de la dosis fueron diarrea (24%), neutropenia (16%), fatiga (10%), vómitos (6%) y náuseas (5%).
El cuarenta y nueve por ciento de las pacientes tuvieron reducciones de dosis debido a una reacción adversa. Las reacciones adversas más frecuentes que llevaron a reducciones de dosis fueron diarrea (20%), neutropenia (11%) y fatiga (9%).
Las reacciones adversas más frecuentes notificadas (≥20%) fueron: diarrea, fatiga, náuseas, disminución del apetito, dolor abdominal, neutropenia, vómitos, infecciones, anemia, cefalea y trombocitopenia. Las reacciones adversas se muestran en la Tabla 14 y las anormalidades de laboratorio en la Tabla 15.
|
a Incluye astenia, fatiga. |
|||
| VERZENIO N=132 |
|||
| Todos los grados % |
Grado 3 % |
Grado 4 % |
|
| Trastornos gastrointestinales | |||
| Diarrea | 90 | 20 | 0 |
| Náuseas | 64 | 4.5 | 0 |
| Dolor abdominal | 39 | 2.3 | 0 |
| Vómitos | 35 | 1.5 | 0 |
| Estreñimiento | 17 | 0.8 | 0 |
| Boca seca | 14 | 0 | 0 |
| Estomatitis | 14 | 0 | 0 |
| Infecciones e infestaciones | |||
| Infecciones | 31 | 4.5 | 0 |
| Trastornos generales y afecciones en el sitio de administración | |||
| Fatigaa | 65 | 13 | 0 |
| Pirexia | 11 | 0 | 0 |
| Trastornos del metabolismo y de la nutrición | |||
| Disminución del apetito | 45 | 3.0 | 0 |
| Deshidratación | 10 | 2.3 | 0 |
| Trastornos respiratorios, torácicos y mediastínicos | |||
| Tos | 19 | 0 | 0 |
| Trastornos musculoesqueléticos y del tejido conjuntivo | |||
| Artralgia | 15 | 0 | 0 |
| Trastornos del sistema nervioso | |||
| Cefalea | 20 | 0 | 0 |
| Disgeusia | 12 | 0 | 0 |
| Mareo | 11 | 0 | 0 |
| Trastornos de la piel y del tejido subcutáneo | |||
| Alopecia | 12 | 0 | 0 |
| Pruebas | |||
| Disminución de peso | 14 | 0 | 0 |
| VERZENIO N=132 |
|||
| Todos los grados % |
Grado 3 % |
Grado 4 % |
|
| Creatinina aumentada | 99 | 0.8 | 0 |
| Leucocitos disminuidos | 91 | 28 | 0 |
| Conteo de neutrófilos disminuido | 88 | 22 | 4.6 |
| Anemia | 69 | 0 | 0 |
| Conteo de linfocitos disminuido | 42 | 13 | 0.8 |
| Conteo de plaquetas disminuido | 41 | 2.3 | 0 |
| ALT aumentada | 31 | 3.1 | 0 |
| AST aumentada | 30 | 3.8 | 0 |
Creatinina aumentada
Se ha demostrado que el abemaciclib aumenta la creatinina sérica debido a la inhibición de los transportadores de secreción tubular renal, sin afectar la función glomerular [ver Farmacología clínica (12.3)]. En estudios clínicos, los aumentos en la creatinina sérica (aumento medio, 0.2-0.3 mg/dL) ocurrieron dentro del primer ciclo de 28 días de dosificación de VERZENIO, permanecieron elevados pero estables durante el período de tratamiento y fueron reversibles después de la interrupción del tratamiento. Se pueden considerar marcadores alternativos como BUN, cistatina C o TFG calculada, que no se basan en la creatinina, para determinar si la función renal está deteriorada.
6.2 Experiencia postcomercialización
Las siguientes reacciones adversas se han identificado durante el uso posterior a la aprobación de VERZENIO. Debido a que estas reacciones se notifican voluntariamente a partir de una población de tamaño incierto, no siempre es posible estimar de manera confiable su frecuencia o establecer una relación causal con la exposición al fármaco.
Trastornos respiratorios: Enfermedad pulmonar intersticial (EPI)/neumonitis [ver Advertencias y precauciones (5.3)].
7 INTERACCIONES MEDICAMENTOSAS
7.1 Efecto de otros medicamentos sobre VERZENIO
Inhibidores de CYP3A
Los inhibidores potentes y moderados de CYP3A4 aumentaron la exposición a abemaciclib y sus metabolitos activos en una medida clínicamente significativa y pueden provocar un aumento de la toxicidad.
Ketoconazol
Evite el uso concomitante de ketoconazol. Se predice que el ketoconazol aumentará el AUC de abemaciclib hasta en 16 veces [ver Farmacología clínica (12.3)].
Otros inhibidores potentes de CYP3A
En pacientes con dosis iniciales recomendadas de 200 mg dos veces al día o 150 mg dos veces al día, reduzca la dosis de VERZENIO a 100 mg dos veces al día con el uso concomitante de inhibidores potentes de CYP3A distintos del ketoconazol. En pacientes que han tenido una reducción de la dosis a 100 mg dos veces al día debido a reacciones adversas, reduzca aún más la dosis de VERZENIO a 50 mg dos veces al día con el uso concomitante de inhibidores potentes de CYP3A. Si un paciente que toma VERZENIO suspende un inhibidor potente de CYP3A, aumente la dosis de VERZENIO (después de 3-5 semividas del inhibidor) a la dosis que se usaba antes de comenzar el inhibidor. Los pacientes deben evitar los productos de pomelo [ver
Posología y administración (2.2) y Farmacología clínica (12.3)].
Inhibidores moderados de CYP3A
Con el uso concomitante de inhibidores moderados de CYP3A, controle las reacciones adversas y considere la posibilidad de reducir la dosis de VERZENIO en incrementos de 50 mg según se muestra en la Tabla 1, si es necesario.
Inductores potentes y moderados de CYP3A
La administración conjunta de inductores potentes o moderados de CYP3A disminuyó las concentraciones plasmáticas de abemaciclib y sus metabolitos activos y puede provocar una reducción de la actividad. Evite el uso concomitante de inductores potentes o moderados de CYP3A y considere agentes alternativos [ver Farmacología clínica (12.3)].
8 USO EN POBLACIONES ESPECÍFICAS
8.1 Embarazo
Resumen del riesgo
Basándose en los hallazgos en animales y en su mecanismo de acción, VERZENIO puede causar daño fetal cuando se administra a una mujer embarazada [ver Farmacología clínica (12.1)]. No hay datos humanos disponibles que informen sobre el riesgo asociado al fármaco. Se debe advertir a las mujeres embarazadas sobre el riesgo potencial para el feto. En estudios de reproducción en animales, la administración de abemaciclib durante la organogénesis fue teratogénica y causó una disminución del peso fetal a exposiciones maternas similares a la exposición clínica humana basada en el AUC a la dosis máxima recomendada en humanos (ver Datos). Se debe advertir a las mujeres embarazadas sobre el riesgo potencial para el feto.
Se desconoce el riesgo de base de defectos congénitos importantes y aborto espontáneo para la población indicada. Sin embargo, el riesgo de base en la población general de EE. UU. de defectos congénitos importantes es del 2 al 4 % y de aborto espontáneo del 15 al 20 % de los embarazos clínicamente reconocidos.
Datos
Datos en animales
En un estudio de desarrollo embriofetal, ratas embarazadas recibieron dosis orales de abemaciclib de hasta 15 mg/kg/día durante el período de organogénesis. Las dosis ≥4 mg/kg/día causaron una disminución del peso corporal fetal y un aumento de la incidencia de malformaciones y variaciones cardiovasculares y esqueléticas. Estos hallazgos incluyeron la ausencia de la arteria innominada y el arco aórtico, la arteria subclavia mal posicionada, la esternobra no osificada, la osificación bífida del centro torácico y las costillas rudimentarias o nodulares. A 4 mg/kg/día en ratas, las exposiciones sistémicas maternas fueron aproximadamente iguales a la exposición humana (AUC) a la dosis recomendada.
8.2 Lactancia
Resumen del riesgo
No hay datos sobre la presencia de abemaciclib en la leche materna, ni sobre sus efectos en el niño amamantado o en la producción de leche. Debido a la posibilidad de reacciones adversas graves en los lactantes amamantados por VERZENIO, se debe aconsejar a las mujeres en período de lactancia que no amamanten durante el tratamiento con VERZENIO y durante 3 semanas después de la última dosis.
8.3 Mujeres y hombres en edad fértil
Basándose en estudios en animales, VERZENIO puede causar daño fetal cuando se administra a una mujer embarazada [ver Uso en poblaciones específicas (8.1)].
Prueba de embarazo
Verificar el estado del embarazo en mujeres en edad fértil antes de iniciar el tratamiento con VERZENIO.
Infertilidad
Hombres
Basándose en los hallazgos en animales, VERZENIO puede afectar la fertilidad en hombres en edad fértil [ver Toxicología no clínica (13.1)].
8.4 Uso pediátrico
No se ha establecido la seguridad y eficacia de VERZENIO en pacientes pediátricos.
8.5 Uso geriátrico
De los 2791 pacientes tratados con VERZENIO en monarchE, el 15 % tenía 65 años o más y el 2,7 % tenía 75 años o más.
De los 900 pacientes que recibieron VERZENIO en MONARCH 1, MONARCH 2 y MONARCH 3, el 38 % tenía 65 años o más y el 10 % tenía 75 años o más. Las reacciones adversas más comunes (≥5 %) de grado 3 o 4 en pacientes ≥65 años en MONARCH 1, 2 y 3 fueron: neutropenia, diarrea, fatiga, náuseas, deshidratación, leucopenia, anemia, infecciones y aumento de ALT.
No se observaron diferencias generales en la seguridad o eficacia de VERZENIO entre estos pacientes y los pacientes más jóvenes.
8.6 Insuficiencia renal
No se requiere ajuste de la dosis para pacientes con insuficiencia renal leve o moderada (CLcr ≥30-89 mL/min, estimado por Cockcroft-Gault [C-G]). Se desconoce la farmacocinética de abemaciclib en pacientes con insuficiencia renal grave (CLcr <30 mL/min, C-G), enfermedad renal en etapa terminal o en pacientes en diálisis [ver Farmacología clínica (12.3)].
8.7 Insuficiencia hepática
No son necesarios ajustes de dosis en pacientes con insuficiencia hepática leve o moderada (Child-Pugh A o B).
Reducir la frecuencia de dosificación al administrar VERZENIO a pacientes con insuficiencia hepática grave (Child-Pugh C) [ver Posología y administración (2.2) y Farmacología clínica (12.3)].
11 DESCRIPCIÓN
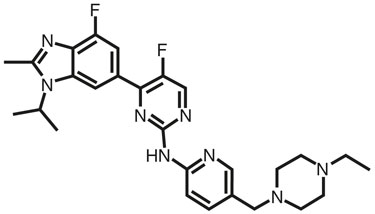
El abemaciclib es un inhibidor de la cinasa para administración oral. Es un polvo blanco a amarillo con la fórmula empírica C27H32F2N8 y un peso molecular de 506,59.
El nombre químico del abemaciclib es 2-pirimidinamina, N-[5-[(4-etil-1-piperazinil)metil]-2-piridinil]-5-fluoro-4-[4-fluoro-2-metil-1-(1-metiletil)-1H-bencimidazol-6-il]-. El abemaciclib tiene la siguiente estructura:
Los comprimidos de VERZENIO (abemaciclib) se presentan como comprimidos ovalados de liberación inmediata, de color blanco, beige o amarillo. Los excipientes inactivos son los siguientes: Excipientes: celulosa microcristalina 102, celulosa microcristalina 101, lactosa monohidrato, croscarmelosa sódica, estearil fumarato sódico, dióxido de silicio. Ingredientes de la mezcla de color: alcohol polivinílico, dióxido de titanio, polietilenglicol, talco, óxido de hierro amarillo y óxido de hierro rojo.
12 FARMACOLOGÍA CLÍNICA
12.1 Mecanismo de acción
Abemaciclib es un inhibidor de las cinasas dependientes de ciclina 4 y 6 (CDK4 y CDK6). Estas cinasas se activan al unirse a las D-ciclinas. En las líneas celulares de cáncer de mama con receptor de estrógenos positivo (ER+), la ciclina D1 y CDK4/6 promueven la fosforilación de la proteína retinoblastoma (Rb), la progresión del ciclo celular y la proliferación celular. In vitro, la exposición continua a abemaciclib inhibió la fosforilación de Rb y bloqueó la progresión de la fase G1 a la fase S del ciclo celular, lo que provocó senescencia y apoptosis. En modelos de xenotrasplante de cáncer de mama, la administración diaria de abemaciclib sin interrupción como agente único o en combinación con antiestrógenos provocó una reducción del tamaño del tumor.
12.3 Farmacocinética
La farmacocinética de abemaciclib se caracterizó en pacientes con tumores sólidos, incluido el cáncer de mama, y en sujetos sanos.
Tras la administración de dosis únicas y repetidas dos veces al día de 50 mg (0,3 veces la dosis recomendada aprobada de 150 mg) a 200 mg de abemaciclib, el aumento de la exposición plasmática (AUC) y Cmax fue aproximadamente proporcional a la dosis. Se alcanzó el estado estacionario en un plazo de 5 días tras la administración repetida dos veces al día, y la razón de acumulación media geométrica estimada fue de 2,3 (CV del 50%) y 3,2 (CV del 59%) en función de Cmax y AUC, respectivamente.
Absorción
La biodisponibilidad absoluta de abemaciclib después de una dosis oral única de 200 mg es del 45% (CV del 19%). La Tmax mediana de abemaciclib es de 8,0 horas (intervalo: 4,1-24,0 horas).
Efecto de los alimentos
Una comida alta en grasas y calorías (aproximadamente de 800 a 1000 calorías con 150 calorías de proteínas, 250 calorías de carbohidratos y de 500 a 600 calorías de grasas) administrada a sujetos sanos aumentó el AUC de abemaciclib más sus metabolitos activos en un 9% y aumentó la Cmax en un 26%.
Distribución
In vitro, abemaciclib se unió a las proteínas plasmáticas humanas, a la albúmina sérica y a la alfa-1-glicoproteína ácida de forma independiente de la concentración desde 152 ng/mL hasta 5066 ng/mL. En un estudio clínico, la fracción unida media (desviación estándar, DE) fue del 96,3% (1,1) para abemaciclib, del 93,4% (1,3) para M2, del 96,8% (0,8) para M18 y del 97,8% (0,6) para M20. La media geométrica del volumen de distribución sistémico es de aproximadamente 690,3 L (CV del 49%).
En pacientes con cáncer avanzado, incluido el cáncer de mama, las concentraciones de abemaciclib y sus metabolitos activos M2 y M20 en el líquido cefalorraquídeo son comparables a las concentraciones plasmáticas no unidas.
Eliminación
La media geométrica del aclaramiento hepático (CL) de abemaciclib en pacientes fue de 26,0 L/h (CV del 51%), y la semivida de eliminación plasmática media de abemaciclib en pacientes fue de 18,3 horas (CV del 72%).
Metabolismo
El metabolismo hepático es la principal vía de aclaramiento de abemaciclib. Abemaciclib se metaboliza a varios metabolitos principalmente por el citocromo P450 (CYP) 3A4, con la formación de N-desetilobemaciclib (M2) que representa la principal vía metabólica. Los metabolitos adicionales incluyen hidroxyabemaciclib (M20), hidroxi-N-desetilobemaciclib (M18) y un metabolito oxidativo (M1). M2, M18 y M20 son equipotentes a abemaciclib y sus AUC representaron el 25%, el 13% y el 26% de los analitos circulantes totales en plasma, respectivamente.
Poblaciones específicas
Edad, sexo y peso corporal
Basándose en un análisis farmacocinético poblacional en pacientes con cáncer, la edad (intervalo de 24 a 91 años), el sexo (134 hombres y 856 mujeres) y el peso corporal (intervalo de 36 a 175 kg) no tuvieron ningún efecto en la exposición a abemaciclib.
Pacientes con insuficiencia renal
En un análisis farmacocinético poblacional de 990 individuos, en el que 381 individuos tenían insuficiencia renal leve (60 mL/min ≤ CLcr <90 mL/min) y 126 individuos tenían insuficiencia renal moderada (30 mL/min ≤ CLcr <60 mL/min), la insuficiencia renal leve y moderada no tuvo ningún efecto en la exposición a abemaciclib [véase Uso en poblaciones específicas (8.6)]. Se desconoce el efecto de la insuficiencia renal grave (CLcr <30 mL/min) en la farmacocinética de abemaciclib.
Pacientes con insuficiencia hepática
Después de una dosis oral única de 200 mg de abemaciclib, el AUC0-INF no unido ajustado por potencia relativa de abemaciclib más sus metabolitos activos (M2, M18, M20) en plasma aumentó 1,2 veces en sujetos con insuficiencia hepática leve (Child-Pugh A, n=9), 1,1 veces en sujetos con insuficiencia hepática moderada (Child-Pugh B, n=10) y 2,4 veces en sujetos con insuficiencia hepática grave (Child-Pugh C, n=6) en relación con los sujetos con función hepática normal (n=10) [ver Uso en poblaciones específicas (8.7)]. En sujetos con insuficiencia hepática grave, la semivida de eliminación plasmática media de abemaciclib aumentó a 55 horas en comparación con 24 horas en sujetos con función hepática normal.
Estudios de interacción medicamentosa
Efectos de otros medicamentos sobre abemaciclib
Inhibidores potentes del CYP3A: Se predice que el ketoconazol (un inhibidor potente del CYP3A) aumentará el AUC de abemaciclib hasta en 16 veces.
La administración conjunta de dosis de 500 mg dos veces al día de claritromicina (un inhibidor potente del CYP3A) con una dosis única de 50 mg de VERZENIO (0,3 veces la dosis recomendada aprobada de 150 mg) aumentó el AUC0-INF no unido ajustado por potencia relativa de abemaciclib más sus metabolitos activos (M2, M18 y M20) en 2,5 veces en relación con el abemaciclib solo en pacientes con cáncer.
Inhibidores moderados del CYP3A: Se predice que el verapamilo y el diltiazem (inhibidores moderados del CYP3A) aumentarán el AUC no unido ajustado por potencia relativa de abemaciclib más sus metabolitos activos (M2, M18 y M20) aproximadamente en 1,6 veces y 2,4 veces, respectivamente.
Inductores potentes del CYP3A: La administración conjunta de dosis diarias de 600 mg de rifampicina (un inductor potente del CYP3A) con una dosis única de 200 mg de VERZENIO disminuyó el AUC0-INF no unido ajustado por potencia relativa de abemaciclib más sus metabolitos activos (M2, M18 y M20) aproximadamente en un 70% en sujetos sanos.
Inductores moderados del CYP3A: Se predice que el efavirenz, el bosentán y el modafinilo (inductores moderados del CYP3A) disminuirán el AUC no unido ajustado por potencia relativa de abemaciclib más sus metabolitos activos (M2, M18 y M20) en un 53%, 41% y 29%, respectivamente.
Loperamida: La administración conjunta de una dosis única de 8 mg de loperamida con una dosis única de 400 mg de abemaciclib en sujetos sanos aumentó el AUC0-INF no unido ajustado por potencia relativa de abemaciclib más sus metabolitos activos (M2 y M20) en un 12%, lo que no se considera clínicamente relevante.
Efectos de abemaciclib sobre otros medicamentos
Loperamida: En un estudio clínico de interacción farmacológica en sujetos sanos, la administración conjunta de una dosis única de 8 mg de loperamida con una dosis única de 400 mg de abemaciclib (2,7 veces la dosis recomendada aprobada de 150 mg) aumentó el AUC0-INF de loperamida en un 9% y la Cmax en un 35% en relación con la loperamida sola. Estos aumentos en la exposición a la loperamida no se consideran clínicamente relevantes.
Metformina: En un estudio clínico de interacción farmacológica en sujetos sanos, la administración conjunta de una dosis única de 1000 mg de metformina, un sustrato clínicamente relevante de los transportadores renales OCT2, MATE1 y MATE2-K, con una dosis única de 400 mg de abemaciclib (2,7 veces la dosis recomendada aprobada de 150 mg) aumentó el AUC0-INF de metformina en un 37% y la Cmax en un 22% en relación con la metformina sola. El abemaciclib redujo la depuración renal y la secreción renal de metformina en un 45% y un 62%, respectivamente, en relación con la metformina sola, sin ningún efecto sobre la tasa de filtración glomerular (TFG) medida por la depuración de iohexol y la cistatina C sérica.
Terapias endocrinas: En estudios clínicos en pacientes con cáncer de mama, no hubo ningún efecto clínicamente relevante de abemaciclib sobre la farmacocinética del fulvestrant, anastrozol, letrozol, exemestano o tamoxifeno.
Vías metabólicas del CYP: En un estudio clínico de interacción farmacológica en pacientes con cáncer, las dosis múltiples de abemaciclib (200 mg dos veces al día durante 7 días) no produjeron cambios clínicamente significativos en la farmacocinética de los sustratos del CYP1A2, CYP2C9, CYP2D6 y CYP3A4. El abemaciclib es un sustrato del CYP3A4, y no se observaron cambios dependientes del tiempo en la farmacocinética del abemaciclib como resultado de la autoinhibición de su metabolismo.
Estudios in vitro
Sistemas de transporte: El abemaciclib y sus principales metabolitos activos inhiben los transportadores renales OCT2, MATE1 y MATE2-K a concentraciones alcanzables con la dosis recomendada aprobada. El aumento de creatinina sérica observado en los estudios clínicos con abemaciclib probablemente se deba a la inhibición de la secreción tubular de creatinina a través de OCT2, MATE1 y MATE2-K [véase Reacciones adversas (6.1)]. El abemaciclib y sus principales metabolitos a concentraciones clínicamente relevantes no inhiben los transportadores de captación hepática OCT1, OATP1B1 y OATP1B3 ni los transportadores de captación renal OAT1 y OAT3.
El abemaciclib es un sustrato de P-gp y BCRP. El abemaciclib y sus principales metabolitos activos, M2 y M20, no son sustratos de los transportadores de captación hepática OCT1, polipéptido transportador de aniones orgánicos 1B1 (OATP1B1) ni OATP1B3.
El abemaciclib inhibe P-gp y BCRP. Se desconocen las consecuencias clínicas de este hallazgo en sustratos sensibles a P-gp y BCRP.
13 TOXICOLOGÍA NO CLÍNICA
13.1 Carcinogénesis, Mutagénesis, Deterioro de la Fertilidad
Se evaluó la carcinogenicidad de Abemaciclib en un estudio de 2 años en ratas. Abemaciclib no fue carcinogénico en ratas macho y hembra a dosis orales de hasta 3 mg/kg/día (aproximadamente 1 vez la exposición a la dosis máxima recomendada en humanos según el AUC).
Abemaciclib y sus metabolitos humanos activos M2 y M20 no fueron mutagénicos en un ensayo de mutación inversa bacteriana (Ames) ni clastogénicos en un ensayo in vitro de aberración cromosómica en células de ovario de hámster chino o linfocitos de sangre periférica humana. Abemaciclib, M2 y M20 no fueron clastogénicos en un ensayo in vivo de micronúcleos de médula ósea de rata.
Abemaciclib puede afectar la fertilidad en hombres con potencial reproductivo. En estudios de toxicidad a dosis repetidas de hasta 3 meses de duración, los hallazgos relacionados con abemaciclib en los testículos, el epidídimo, la próstata y la vesícula seminal a dosis ≥10 mg/kg/día en ratas y ≥0.3 mg/kg/día en perros incluyeron disminución del peso de los órganos, desechos celulares intratubulares, hipospermia, dilatación tubular, atrofia y degeneración/necrosis. Estas dosis en ratas y perros resultaron en aproximadamente 2 y 0.02 veces, respectivamente, la exposición (AUC) en humanos a la dosis máxima recomendada en humanos. En un estudio de fertilidad en ratas macho, abemaciclib no tuvo efectos sobre el apareamiento y la fertilidad a dosis orales de hasta 10 mg/kg/día (aproximadamente 2 veces la exposición a la dosis máxima recomendada en humanos según el AUC).
En un estudio de fertilidad femenina y desarrollo embrionario temprano en ratas, abemaciclib no afectó el apareamiento ni la fertilidad a dosis de hasta 20 mg/kg/día (aproximadamente 3 veces la exposición a la dosis máxima recomendada en humanos según el AUC).
13.2 Toxicología y/o Farmacología Animal
En estudios de toxicidad a dosis repetidas de hasta 6 meses de duración, la administración oral de abemaciclib resultó en atrofia de la retina de los ojos en ratones a una dosis de 150 mg/kg/día (aproximadamente 10 veces la exposición a la dosis máxima recomendada en humanos según el AUC) y en ratas a una dosis de 30 mg/kg/día (aproximadamente 5 veces la exposición a la dosis máxima recomendada en humanos según el AUC). En un estudio de carcinogenicidad en ratas de 2 años, la administración oral de abemaciclib resultó en atrofia de la retina en los ojos a dosis ≥0.3 mg/kg/día (aproximadamente 0.05 veces la exposición a la dosis máxima recomendada en humanos según el AUC).
14 ESTUDIOS CLÍNICOS
14.1 Cáncer de mama precoz
VERZENIO en combinación con terapia endocrina estándar (monarchE)
Pacientes con cáncer de mama precoz, HR-positivo, HER2-negativo, con ganglios positivos, con alto riesgo de recurrencia
monarchE (NCT03155997) fue un estudio multicéntrico, aleatorizado (1:1), abierto, de dos cohortes, en mujeres y hombres adultos con cáncer de mama precoz, HR-positivo, HER2-negativo, con ganglios positivos, resecado, con características clínicas y patológicas consistentes con un alto riesgo de recurrencia de la enfermedad. Para ser incluidos, los pacientes debían tener cáncer de mama precoz HR-positivo HER2-negativo con afectación tumoral en al menos 1 ganglio linfático axilar (pALN) y para ser incluidos en la cohorte 1 debían tener:
- ≥4 pALN o
- 1-3 pALN y al menos uno de:
- –
- grado tumoral 3 o
- –
- tamaño tumoral ≥50 mm
Los pacientes incluidos en la cohorte 2 no podían cumplir los criterios de inclusión de la cohorte 1. Para ser incluidos en la cohorte 2, los pacientes debían tener 1-3 pALN y una puntuación de Ki-67 ≥20 %. Las muestras de tumores de mama se analizaron en centros centrales utilizando el ensayo Ki-67 IHC MIB-1 pharmDx (Dako Omnis) para determinar si la puntuación de Ki-67 era ≥20 %.
Los pacientes fueron aleatorizados para recibir 2 años de VERZENIO más la terapia endocrina estándar a elección del médico o solo terapia endocrina estándar. La aleatorización al tratamiento se estratificó por tratamiento previo (quimioterapia neoadyuvante frente a quimioterapia adyuvante frente a ninguna quimioterapia); estado menopáusico (premenopáusico frente a posmenopáusico); y región (América del Norte/Europa frente a Asia frente a otras). Los hombres se estratificaron como posmenopáusicos. Después del final del período de tratamiento del estudio, la terapia endocrina adyuvante estándar se continuó durante un período de al menos 5 años si se consideró médicamente apropiado.
La principal medida de resultado de eficacia fue la supervivencia sin enfermedad invasiva (IDFS). La IDFS se definió como el tiempo desde la aleatorización hasta la primera aparición de: recurrencia tumoral invasiva ipsilateral, recurrencia de cáncer de mama invasivo regional, recurrencia a distancia, cáncer de mama invasivo contralateral, segundo cáncer invasivo no mamario primario o muerte atribuible a cualquier causa. La supervivencia general (SG) fue una medida de resultado adicional.
Se observó una diferencia estadísticamente significativa en la IDFS en la población por intención de tratar (ITT), que se atribuyó principalmente a los pacientes tratados en la cohorte 1. Si bien los datos de SG en la cohorte 2 siguen siendo inmaduros, se observaron más muertes entre los que recibieron VERZENIO más terapia endocrina estándar en comparación con los que recibieron solo terapia endocrina estándar (10/253 frente a 5/264).
De los 5637 pacientes aleatorizados, 5120 (91 %) fueron aleatorizados en la cohorte 1. La mediana de edad de los pacientes fue de 51 años (rango, 22-89 años), el 99 % eran mujeres, el 70 % eran blancas, el 24 % eran asiáticas, el 1,7 % eran negras o afroamericanas, el 2,1 % eran amerindias o nativas de Alaska, y el 0,1 % eran nativas de Hawái u otras isleñas del Pacífico. El cuarenta y tres por ciento de los pacientes eran premenopáusicas. La mayoría de los pacientes recibieron quimioterapia previa (37 % neoadyuvante, 59 % adyuvante) y radioterapia previa (96 %). El sesenta y cinco por ciento de los pacientes tenían 4 o más ganglios linfáticos positivos, con un 22 % que tenían ≥10 ganglios linfáticos positivos, el 41 % tenían un tumor de grado 3 y el 24 % tenían un tamaño tumoral patológico ≥50 mm. La mayoría de los pacientes (99 %) tenían enfermedad positiva para el receptor de estrógenos y el 87 % tenían enfermedad positiva para el receptor de progesterona. La terapia endocrina inicial recibida por los pacientes incluyó letrozol (39 %), tamoxifeno (31 %), anastrozol (22 %) o exemestano (8 %).
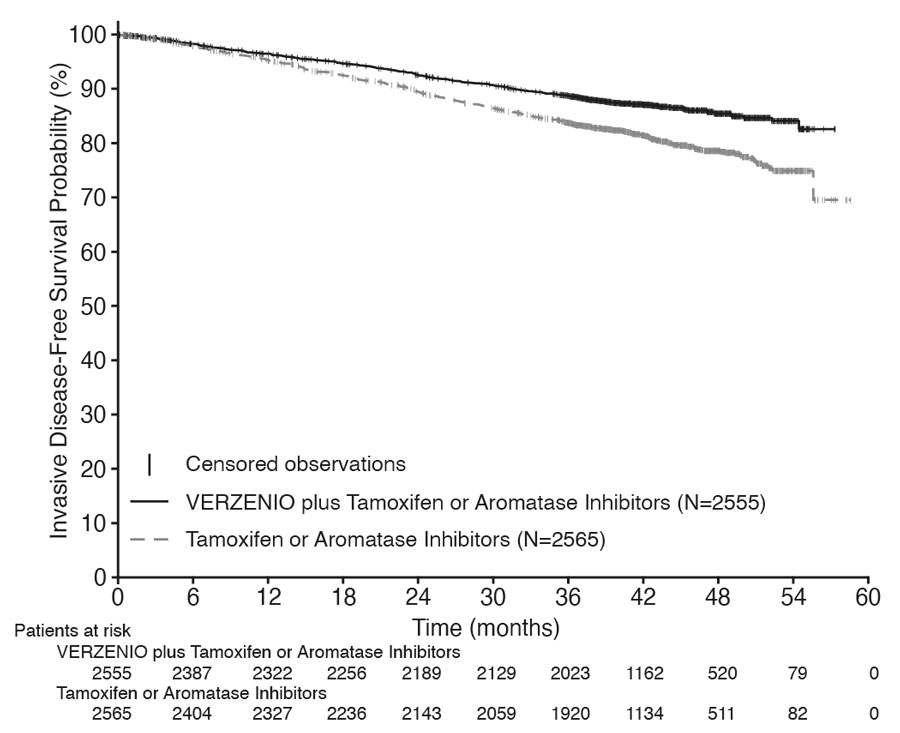
Los resultados de eficacia para la cohorte 1 se resumen en la Tabla 16 y la Figura 1. En el momento del análisis provisional 2 de la SG, la SG era inmadura y un total de 315 (6 %) de los pacientes habían fallecido en la cohorte 1.
|
Abreviatura: IC = intervalo de confianza. |
||
| VERZENIO más Tamoxifeno o un inhibidor de la aromatasa N=2555 |
Tamoxifeno o un inhibidor de la aromatasa N=2565 |
|
| Supervivencia sin enfermedad invasiva (IDFS) | ||
| Número de pacientes con un evento, n (%) | 317 (12) | 474 (18) |
| Hazard ratio (IC 95%) | 0.65 (0.57, 0.75) | |
| IDFS a los 48 meses, % (IC 95%) | 85.5 (83.8, 87.0) | 78.6 (76.7, 80.4) |
Figura 1: Curvas de Kaplan-Meier de supervivencia sin enfermedad invasiva VERZENIO más Tamoxifeno o un inhibidor de la aromatasa versus Tamoxifeno o un inhibidor de la aromatasa en la Cohorte 1 (monarchE)
14.2 Cáncer de mama avanzado o metastásico
VERZENIO en combinación con un inhibidor de la aromatasa (Anastrozol o Letrozol) (MONARCH 3)
Mujeres posmenopáusicas con cáncer de mama avanzado o metastásico HR-positivo, HER2-negativo sin terapia sistémica previa en este contexto de la enfermedad
MONARCH 3 (NCT02246621) fue un estudio multicéntrico, aleatorizado (2:1), doble ciego, controlado con placebo, en mujeres posmenopáusicas con cáncer de mama avanzado o metastásico HR-positivo, HER2-negativo en combinación con un inhibidor de la aromatasa no esteroideo como terapia inicial basada en endocrinología, incluyendo pacientes no tratadas previamente con terapia sistémica para el cáncer de mama.
La aleatorización se estratificó por localización de la enfermedad (visceral, solo hueso u otra) y por terapia endocrina (neo)adyuvante previa (inhibidor de la aromatasa versus otra versus ninguna terapia endocrina previa). Un total de 493 pacientes fueron aleatorizadas para recibir 150 mg de VERZENIO o placebo por vía oral dos veces al día, más la elección del médico de letrozol (80% de las pacientes) o anastrozol (20% de las pacientes). La mediana de edad de las pacientes fue de 63 años (rango, 32-88 años) y la mayoría eran blancas (58%) o asiáticas (30%). Un total del 51% había recibido terapia sistémica previa y el 39% de las pacientes habían recibido quimioterapia, el 53% tenía enfermedad visceral y el 22% tenía enfermedad solo ósea.
Los resultados de eficacia se resumen en la Tabla 17 y la Figura 2. La SPP se evaluó según la versión 1.1 de RECIST y la evaluación de la SPP basada en una revisión radiológica independiente ciega fue consistente con la evaluación del investigador. Se observaron resultados consistentes de SPP en todos los subgrupos de estratificación de pacientes por localización de la enfermedad y terapia endocrina (neo)adyuvante previa.
|
Abreviaturas: IC = intervalo de confianza; SG = supervivencia global; NR = no alcanzado; NS = no estadísticamente significativo. |
||
|
a Respuesta completa + respuesta parcial. |
||
|
b Basado en respuestas confirmadas. |
||
| VERZENIO más Anastrozol o Letrozol |
Placebo más Anastrozol o Letrozol |
|
| Supervivencia libre de progresión | N=328 | N=165 |
| Número de pacientes con un evento, n (%) | 138 (42) | 108 (65) |
| Mediana en meses (IC del 95%) | 28.2 (23.5, NR) | 14.8 (11.2, 19.2) |
| Razón de riesgo (IC del 95%) | 0.54 (0.42, 0.70) | |
| p-valor | <0.0001 | |
| Supervivencia global | N=328 | N=165 |
| Número de pacientes con un evento, n (%) | 198 (60) | 116 (70) |
| Mediana en meses (IC del 95%) | 66.8 (59.2, 74.8) | 53.7 (44.7, 59.3) |
| Razón de riesgo (IC del 95%) | 0.80 (0.64, 1.02) | |
| p-valor | NS | |
| Respuesta objetiva para pacientes con enfermedad mediblea | N=267 | N=132 |
| Tasa de respuesta objetiva n (%)a,b | 148 (55) | 53 (40) |
| IC del 95% | 49, 61 | 32, 49 |
Figura 2: Curvas de Kaplan-Meier de supervivencia libre de progresión: VERZENIO más Anastrozol o Letrozol versus Placebo más Anastrozol o Letrozol en la población de intención de tratar (MONARCH 3)
VERZENIO en combinación con Fulvestrant (MONARCH 2)
Pacientes con cáncer de mama avanzado o metastásico, HR-positivo y HER2-negativo con progresión de la enfermedad durante o después de la terapia endocrina adyuvante o metastásica previa
MONARCH 2 (NCT02107703) fue un estudio multicéntrico, aleatorizado y controlado con placebo en mujeres con cáncer de mama metastásico HR-positivo y HER2-negativo en combinación con fulvestrant en pacientes con progresión de la enfermedad después de la terapia endocrina que no habían recibido quimioterapia en el contexto metastásico. La aleatorización se estratificó por localización de la enfermedad (visceral, solo hueso u otra) y por la sensibilidad a la terapia endocrina previa (resistencia primaria o secundaria). La resistencia primaria a la terapia endocrina se definió como una recaída durante los primeros 2 años de terapia endocrina adyuvante o enfermedad progresiva en los primeros 6 meses de la terapia endocrina de primera línea para el cáncer de mama metastásico. Un total de 669 pacientes fueron aleatorizadas para recibir VERZENIO o placebo por vía oral dos veces al día más una inyección intramuscular de 500 mg de fulvestrant en los días 1 y 15 del ciclo 1 y luego en el día 1 del ciclo 2 y posteriores (ciclos de 28 días). Las mujeres pre/perimenopáusicas fueron incluidas en el estudio y recibieron el agonista de la hormona liberadora de gonadotropina goserelina durante al menos 4 semanas antes y durante la duración de MONARCH 2. Las pacientes permanecieron en tratamiento continuo hasta el desarrollo de enfermedad progresiva o toxicidad inmanejable.
La mediana de edad de las pacientes fue de 60 años (rango, 32-91 años), y el 37% de las pacientes tenían más de 65 años. La mayoría eran blancas (56%), y el 99% de las pacientes tenían un estado de rendimiento del Eastern Cooperative Oncology Group (ECOG) de 0 o 1. El veinte por ciento (20%) de las pacientes tenían enfermedad metastásica de novo, el 27% tenían enfermedad solo ósea y el 56% tenían enfermedad visceral. El veinticinco por ciento (25%) de las pacientes tenían resistencia primaria a la terapia endocrina. El diecisiete por ciento (17%) de las pacientes eran pre o perimenopáusicas.
Los resultados de eficacia del estudio MONARCH 2 se resumen en la Tabla 18, la Figura 3 y la Figura 4. La evaluación de la SLP basada en una revisión radiológica independiente ciega fue consistente con la evaluación del investigador. Se observaron resultados consistentes en todos los subgrupos de estratificación de pacientes de localización de la enfermedad y resistencia a la terapia endocrina para la SLP y la SG.
|
Abreviatura: IC = intervalo de confianza, SG = supervivencia global. |
||
|
a Estratificado por localización de la enfermedad (metástasis visceral vs. metástasis solo ósea vs. otra) y resistencia a la terapia endocrina (resistencia primaria vs. resistencia secundaria) |
||
|
b Datos de un análisis intermedio preespecificado (77% del número de eventos necesarios para el análisis final planificado) con el valor p comparado con la alfa asignada de 0,021. |
||
|
c Respuesta completa + respuesta parcial. |
||
| VERZENIO más Fulvestrant | Placebo más Fulvestrant | |
| Supervivencia libre de progresión (Evaluación del investigador) |
N=446 | N=223 |
| Número de pacientes con un evento n (%) | 222 (50) | 157 (70) |
| Mediana en meses (IC del 95%) | 16.4 (14.4, 19.3) | 9.3 (7.4, 12.7) |
| Razón de riesgo (IC del 95%)a | 0.55 (0.45, 0.68) | |
| Valor pa | p<.0001 | |
| Supervivencia globalb | ||
| Número de muertes n (%) | 211 (47) | 127 (57) |
| Mediana de SG en meses (IC del 95%) | 46.7 (39.2, 52.2) | 37.3 (34.4, 43.2) |
| Razón de riesgo (IC del 95%)a | 0.76 (0.61, 0.95) | |
| p-valuea | p=.0137 | |
| Respuesta Objetiva para Pacientes con Enfermedad Medible | N=318 | N=164 |
| Tasa de respuesta objetiva n (%)c | 153 (48) | 35 (21) |
| IC del 95% | 43, 54 | 15, 28 |
Figura 3: Curvas de Kaplan-Meier de Supervivencia Libre de Progresión: VERZENIO más Fulvestrant versus Placebo más Fulvestrant (MONARCH 2)
Figura 4: Curvas de Kaplan-Meier de Supervivencia Global: VERZENIO más Fulvestrant versus Placebo más Fulvestrant (MONARCH 2)
VERZENIO Administrado como Monoterapia en Cáncer de Mama Metastásico (MONARCH 1)
Pacientes con cáncer de mama HR-positivo, HER2-negativo que recibieron terapia endocrina previa y 1-2 regímenes de quimioterapia en el contexto metastásico
MONARCH 1 (NCT02102490) fue un estudio de un solo brazo, abierto, multicéntrico en mujeres con cáncer de mama metastásico HR-positivo, HER2-negativo medible cuya enfermedad progresó durante o después de la terapia endocrina, habían recibido un taxano en cualquier contexto y habían recibido 1 o 2 regímenes de quimioterapia previos en el contexto metastásico. Un total de 132 pacientes recibieron 200 mg de VERZENIO por vía oral dos veces al día con un esquema continuo hasta el desarrollo de enfermedad progresiva o toxicidad inmanejable.
La mediana de edad de las pacientes fue de 58 años (rango, 36-89 años), y la mayoría de las pacientes fueron blancas (85%). Las pacientes tenían un estado de rendimiento del Eastern Cooperative Oncology Group de 0 (55% de las pacientes) o 1 (45%). La mediana de duración de la enfermedad metastásica fue de 27,6 meses. El noventa por ciento (90%) de las pacientes presentaron metástasis viscerales, y el 51% de las pacientes presentaron 3 o más sitios de enfermedad metastásica. El cincuenta y un por ciento (51%) de las pacientes habían recibido una línea de quimioterapia en el contexto metastásico. El sesenta y nueve por ciento (69%) de las pacientes habían recibido un régimen basado en taxanos en el contexto metastásico y el 55% habían recibido capecitabina en el contexto metastásico. Tabla 19 proporciona los resultados de eficacia de MONARCH 1.
|
Abreviaturas: IC = intervalo de confianza, NR = no alcanzado. |
||
|
a Todas las respuestas fueron respuestas parciales. |
||
|
b Basado en respuestas confirmadas. |
||
| VERZENIO 200 mg N=132 |
||
| Evaluación del Investigador | Revisión Independiente | |
| Tasa de Respuesta Objetivaa,b, n (%) | 26 (20) | 23 (17) |
| IC del 95% | 13, 28 | 11, 25 |
| Duración Mediana de la Respuesta en meses | 8.6 | 7.2 |
| IC del 95% | 5.8, 10.2 | 5.6, NR |
16 SUMINISTRO/ALMACENAMIENTO Y MANIPULACIÓN
Cómo se suministra
Los comprimidos de VERZENIO 50 mg son comprimidos ovalados de color beige con “Lilly” grabado en relieve en un lado y “50” en el otro.
Los comprimidos de VERZENIO 100 mg son comprimidos ovalados de color blanco a casi blanco con “Lilly” grabado en relieve en un lado y “100” en el otro.
Los comprimidos de VERZENIO 150 mg son comprimidos ovalados de color amarillo con “Lilly” grabado en relieve en un lado y “150” en el otro.
Los comprimidos de VERZENIO 200 mg son comprimidos ovalados de color beige con “Lilly” grabado en relieve en un lado y “200” en el otro.
Los comprimidos de VERZENIO se suministran en envases de dosis para 7 días de la siguiente manera:
|
| NDC 0002-6216-54 |
|
| NDC 0002-5337-54 |
|
| NDC 0002-4815-54 |
|
| NDC 0002-4483-54 |
Almacenamiento y manipulación
Conservar a 20°C a 25°C (68°F a 77°F); se permiten excursiones a 15°C a 30°C (59°F a 86°F).
17 INFORMACIÓN DE ASESORAMIENTO AL PACIENTE
Aconseje a los pacientes que lean la información para el paciente aprobada por la FDA.
Diarrea
VERZENIO puede causar diarrea, que puede ser grave en algunos casos [ver Advertencias y precauciones (5.1)].
- La identificación e intervención temprana son cruciales para el manejo óptimo de la diarrea. Indique a los pacientes que, a la primera señal de heces blandas, deben comenzar el tratamiento antidiarreico (por ejemplo, loperamida) y notificar a su proveedor de atención médica para obtener más instrucciones y un seguimiento adecuado.
- Anime a los pacientes a aumentar la ingesta de líquidos orales.
- Si la diarrea no se resuelve con el tratamiento antidiarreico dentro de las 24 horas hasta ≤Grado 1, suspenda la administración de VERZENIO [ver Dosis y administración (2.2)].
Neutropenia
Avise a los pacientes de la posibilidad de desarrollar neutropenia y de que deben comunicarse inmediatamente con su proveedor de atención médica si desarrollan fiebre, particularmente en asociación con cualquier signo de infección [ver Advertencias y precauciones (5.2)].
Enfermedad pulmonar intersticial/Neumonitis
Avise a los pacientes que informen inmediatamente sobre cualquier síntoma respiratorio nuevo o que empeore [ver Advertencias y precauciones (5.3)].
Hepatotoxicidad
Informe a los pacientes sobre los signos y síntomas de hepatotoxicidad. Avise a los pacientes que se comuniquen inmediatamente con su proveedor de atención médica si presentan signos o síntomas de hepatotoxicidad [ver Advertencias y precauciones (5.4)].
Tromboembolismo venoso
Avise a los pacientes que informen inmediatamente sobre cualquier signo o síntoma de tromboembolismo, como dolor o hinchazón en una extremidad, dificultad para respirar, dolor en el pecho, taquipnea y taquicardia [ver Advertencias y precauciones (5.5)].
Toxicidad embriofetal
- Avise a las mujeres embarazadas y a las mujeres en edad fértil sobre el riesgo potencial para el feto. Avise a las mujeres que informen a su proveedor de atención médica sobre un embarazo conocido o sospechoso [ver Advertencias y precauciones (5.6) y Uso en poblaciones específicas (8.1)].
- Avise a las mujeres en edad fértil que usen un método anticonceptivo eficaz durante el tratamiento con VERZENIO y durante 3 semanas después de la última dosis [ver Uso en poblaciones específicas (8.1, 8.3)].
Lactancia
Avise a las mujeres lactantes que no deben amamantar durante el tratamiento con VERZENIO y durante al menos 3 semanas después de la última dosis [ver Uso en poblaciones específicas (8.2)].
Infertilidad
Informe a los hombres en edad fértil que VERZENIO puede afectar la fertilidad [ver Uso en poblaciones específicas (8.3)].
Interacciones medicamentosas
- Informe a los pacientes que eviten el uso concomitante de ketoconazol. Puede ser necesaria una reducción de la dosis para otros inhibidores potentes del CYP3A o para inhibidores moderados del CYP3A [ver Dosis y administración (2.2) e Interacciones medicamentosas (7)].
- El pomelo puede interactuar con VERZENIO. Avise a los pacientes que no consuman productos de pomelo mientras estén en tratamiento con VERZENIO.
- Avise a los pacientes que eviten el uso concomitante de inductores potentes y moderados del CYP3A y que consideren agentes alternativos [ver Dosis y administración (2.2) e Interacciones medicamentosas (7)].
- Avise a los pacientes que informen a sus proveedores de atención médica sobre todos los medicamentos concomitantes, incluidos los medicamentos recetados, los medicamentos de venta libre, las vitaminas y los productos herbales [ver Dosis y administración (2.2) e Interacciones medicamentosas (7)].
Dosis
- Indique a los pacientes que tomen las dosis de VERZENIO aproximadamente a la misma hora todos los días y que se traguen enteras (no las mastiquen, trituren ni las partan antes de tragarlas) [ver Dosis y administración (2.1)].
- Si el paciente vomita u olvida una dosis, avise al paciente que tome la siguiente dosis prescrita a la hora habitual [ver Dosis y administración (2.1)].
- Avise al paciente que VERZENIO se puede tomar con o sin alimentos [ver Dosis y administración 2.1)].
Comercializado por: Lilly USA, LLC, Indianápolis, IN 46285, EE. UU.
Copyright © 2017, 2024, Eli Lilly and Company. Todos los derechos reservados.
VER-0009-USPI-20241113
PROSPECTO PARA EL PACIENTE
|
Esta información para el paciente ha sido aprobada por la Administración de Alimentos y Medicamentos de los EE. UU. |
Revisado: marzo de 2023 |
|
| INFORMACIÓN PARA EL PACIENTE VERZENIO® (ver-ZEN-ee-oh) (abemaciclib) comprimidos |
||
|
¿Cuál es la información más importante que debo saber sobre VERZENIO?
|
||
|
|
|
|
||
|
|
|
| Consulte “¿Cuáles son los posibles efectos secundarios de VERZENIO?” para obtener más información sobre los efectos secundarios. | ||
| ¿Qué es VERZENIO? VERZENIO es un medicamento recetado que se usa:
|
||
| Cuando VERZENIO se usa en combinación con fulvestrant, tamoxifeno o un inhibidor de la aromatasa, lea también la información para el paciente del producto recetado. Consulte a su proveedor de atención médica si no está seguro. No se sabe si VERZENIO es seguro y eficaz en niños. |
||
Antes de tomar VERZENIO, informe a su proveedor de atención médica sobre todas sus afecciones médicas, incluso si:
|
||
| Informe a su proveedor de atención médica sobre todos los medicamentos que toma, incluidos los medicamentos recetados y de venta libre, las vitaminas y los suplementos herbales. VERZENIO puede afectar la forma en que funcionan otros medicamentos, y otros medicamentos pueden afectar la forma en que funciona VERZENIO, causando efectos secundarios graves. Especialmente, informe a su proveedor de atención médica si toma un medicamento que contiene ketoconazol. Conozca los medicamentos que toma. Lleve una lista de ellos para mostrársela a su proveedor de atención médica o farmacéutico cuando reciba un medicamento nuevo. |
||
¿Cómo debo tomar VERZENIO?
|
||
¿Qué debo evitar durante el tratamiento con VERZENIO?
|
||
|
¿Cuáles son los posibles efectos secundarios de VERZENIO? |
||
| Los efectos secundarios más comunes de VERZENIO incluyen: | ||
|
|
|
| VERZENIO puede causar problemas de fertilidad en los hombres. Esto puede afectar su capacidad para engendrar un hijo. Hable con su proveedor de atención médica si esto le preocupa. Estos no son todos los posibles efectos secundarios de VERZENIO. Para obtener más información, consulte a su proveedor de atención médica o farmacéutico. Llame a su proveedor de atención médica para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088. |
||
¿Cómo debo guardar VERZENIO?
|
||
| Mantenga VERZENIO y todos los medicamentos fuera del alcance de los niños. | ||
| Información general sobre el uso seguro y eficaz de VERZENIO. A veces, los medicamentos se recetan para fines distintos de los que figuran en un prospecto de información para el paciente. No use VERZENIO para una afección para la que no se lo recetaron. No le dé VERZENIO a otras personas, incluso si tienen los mismos síntomas que usted. Puede causarles daño. Puede pedirle a su farmacéutico o proveedor de atención médica más información sobre VERZENIO que esté escrita para profesionales de la salud. |
||
| ¿Cuáles son los ingredientes de VERZENIO? Ingrediente activo: abemaciclib Ingredientes inactivos: celulosa microcristalina 102, celulosa microcristalina 101, lactosa monohidrato, croscarmelosa sódica, estearil fumarato sódico, dióxido de silicio. Ingredientes de la mezcla de color: alcohol polivinílico, dióxido de titanio, polietilenglicol, talco, óxido de hierro amarillo, óxido de hierro rojo. Comercializado por: Lilly USA, LLC, Indianápolis, IN 46285, EE. UU. Copyright © 2017, 2023, Eli Lilly and Company. Todos los derechos reservados. VER-0005-PPI-20230303 Para obtener más información, visite www.verzenio.com o llame al 1-800-545-5979. |
||
PANEL DE VISUALIZACIÓN PRINCIPAL
CAJA – VERZENIO 50 mg 14 comprimidos
14 comprimidos
NDC 0002-4483-54
Rx solamente
Verzenio®
(abemaciclib) comprimidos
dosis de 50 mg
Envase para 7 días
Este envase de dosis de 50 mg contiene catorce comprimidos de 50 mg.
www.verzenio.com
LEVANTAR PARA ABRIR
Lilly
PANEL DE VISUALIZACIÓN PRINCIPAL
CAJA – VERZENIO 100 mg 14 comprimidos
14 comprimidos
NDC 0002-4815-54
Rx solamente
Verzenio®
(abemaciclib) comprimidos
dosis de 100 mg
Envase para 7 días
Este envase de dosis de 100 mg contiene catorce comprimidos de 100 mg.
www.verzenio.com
LEVANTAR PARA ABRIR
Lilly
PANEL DE VISUALIZACIÓN PRINCIPAL
CAJA DE ENVASE – VERZENIO 150 mg 14 comprimidos
14 comprimidos
NDC 0002-5337-54
Rx solamente
Verzenio®
(abemaciclib) comprimidos
dosis de 150 mg
Envase para 7 días
Este envase de dosis de 150 mg contiene catorce comprimidos de 150 mg.
www.verzenio.com
LEVANTAR PARA ABRIR
Lilly
PANEL DE VISUALIZACIÓN PRINCIPAL
CAJA – VERZENIO 200 mg 14 comprimidos
14 comprimidos
NDC 0002-6216-54
Rx solamente
Verzenio®
(abemaciclib) comprimidos
dosis de 200 mg
Envase para 7 días
Este envase de 200 mg contiene catorce comprimidos de 200 mg.
www.verzenio.com
LEVANTAR PARA ABRIR
Lilly