Fabricante de medicamentos: GlaxoSmithKline Biologicals SA (Updated: 2023-05-22)
ASPECTOS DESTACADOS DE LA INFORMACIÓN DE PRESCRIPCIÓN
SHINGRIX (vacuna recombinante contra el zóster, adyuvada), suspensión inyectable intramuscular
Aprobación inicial en EE. UU.: 2017
INDICACIONES Y USO
SHINGRIX es una vacuna indicada para la prevención del herpes zóster (HZ):
- •
- en adultos mayores de 50 años.
- •
- en adultos mayores de 18 años que corren o correrán un mayor riesgo de padecer HZ debido a una inmunodeficiencia o inmunosupresión causada por una enfermedad o terapia conocida.
Limitaciones de uso (1):
- •
- SHINGRIX no está indicado para la prevención de la infección primaria por varicela (varicela).
DOSIFICACIÓN Y ADMINISTRACIÓN
Solo para administración intramuscular.
Dos dosis (0.5 ml cada una) administradas por vía intramuscular de acuerdo con los siguientes esquemas:
- •
- Una primera dosis en el mes 0 seguida de una segunda dosis administrada de 2 a 6 meses después. (2.3)
- •
- Para las personas que son o serán inmunodeficientes o inmunodeprimidas y que se beneficiarían de un calendario de vacunación más corto: una primera dosis en el mes 0 seguida de una segunda dosis administrada de 1 a 2 meses después. (2.3)
FORMAS DE DOSIFICACIÓN Y CONCENTRACIONES
Suspensión inyectable suministrada como un vial de dosis única de componente antigénico de la glucoproteína E (gE) del virus varicela zóster liofilizado que debe reconstituirse con el vial adjunto de componente de suspensión adyuvante AS01B. Después de la reconstitución, una dosis única de SHINGRIX es de 0.5 ml. (3)
CONTRAINDICACIONES
Antecedentes de reacción alérgica grave (p. ej., anafilaxia) a cualquier componente de la vacuna o después de una dosis previa de SHINGRIX. (4)
ADVERTENCIAS Y PRECAUCIONES
- •
- En un estudio observacional posterior a la comercialización, se observó un mayor riesgo de síndrome de Guillain-Barré durante los 42 días posteriores a la vacunación con SHINGRIX. (5.2, 6.2)
- •
- El síncope (desmayo) puede estar asociado con la administración de vacunas inyectables, incluido SHINGRIX. Se deben seguir los procedimientos para evitar lesiones por caídas y restaurar la perfusión cerebral después del síncope. (5.3)
REACCIONES ADVERSAS
- •
- Las reacciones adversas locales solicitadas notificadas en personas mayores de 50 años fueron dolor (78 %), enrojecimiento (38 %) e hinchazón (26 %). (6.1)
- •
- Las reacciones adversas generales solicitadas notificadas en personas mayores de 50 años fueron mialgia (45 %), fatiga (45 %), dolor de cabeza (38 %), escalofríos (27 %), fiebre (21 %) y síntomas gastrointestinales (17 %). (6.1)
- •
- Las reacciones adversas locales solicitadas notificadas en receptores de trasplante autólogo de células madre hematopoyéticas (de 18 a 49 años y ≥50 años de edad) fueron dolor (88 % y 83 %), enrojecimiento (30 % y 35 %) e hinchazón (21 % y 18 %). (6.1)
- •
- Las reacciones adversas generales solicitadas notificadas en receptores de trasplante autólogo de células madre hematopoyéticas (de 18 a 49 años y ≥50 años de edad) fueron fatiga (64 % y 54 %), mialgia (58 % y 52 %), dolor de cabeza (44 % y 30 %), síntomas gastrointestinales (21 % y 28 %), escalofríos (31 % y 25 %) y fiebre (28 % y 18 %). (6.1)
Para informar de REACCIONES ADVERSAS SOSPECHOSAS, póngase en contacto con GlaxoSmithKline en el 1-888-825-5249 o con el VAERS en el 1-800-822-7967 o en www.vaers.hhs.gov.
Consulte la sección 17 para obtener INFORMACIÓN DE ASESORAMIENTO AL PACIENTE.
Revisado: 5/2023
Tabla de Contenido
INFORMACIÓN COMPLETA DE PRESCRIPCIÓN: CONTENIDO*
1 INDICACIONES Y USO
2 DOSIFICACIÓN Y ADMINISTRACIÓN
2.1 Reconstitución
2.2 Instrucciones de administración
2.3 Dosis y calendario
3 FORMAS DE DOSIFICACIÓN Y CONCENTRACIONES
4 CONTRAINDICACIONES
5 ADVERTENCIAS Y PRECAUCIONES
5.1 Prevención y manejo de reacciones alérgicas a las vacunas
5.2 Síndrome de Guillain-Barré (GBS)
5.3 Síncope
6 REACCIONES ADVERSAS
6.1 Experiencia en ensayos clínicos
6.2 Experiencia posterior a la comercialización
8 USO EN POBLACIONES ESPECÍFICAS
8.1 Embarazo
8.2 Lactancia
8.4 Uso pediátrico
8.5 Uso geriátrico
11 DESCRIPCIÓN
12 FARMACOLOGÍA CLÍNICA
12.1 Mecanismo de acción
13 TOXICOLOGÍA NO CLÍNICA
13.1 Carcinogénesis, mutagénesis, deterioro de la fertilidad
14 ESTUDIOS CLÍNICOS
14.1 Eficacia en sujetos de 50 años o más
14.2 Eficacia en sujetos de 70 años o más
14.3 Análisis de eficacia agrupados de los estudios 1 y 2
14.4 Evaluación inmunológica para respaldar el calendario de dosificación
14.5 Eficacia en adultos inmunocomprometidos de 18 años o más
14.6 Revacunación después de la vacunación con ZOSTAVAX (vacuna contra el zóster viva)
14.7 Administración concomitante con otras vacunas
16 CÓMO SE SUMINISTRA/ALMACENAMIENTO Y MANIPULACIÓN
16.1 Almacenamiento antes de la reconstitución
16.2 Almacenamiento después de la reconstitución
17 INFORMACIÓN DE ASESORAMIENTO AL PACIENTE
- *
- Las secciones o subsecciones omitidas de la información de prescripción completa no se enumeran.
1 INDICACIONES Y USO
SHINGRIX es una vacuna indicada para la prevención del herpes zóster (HZ):
• en adultos mayores de 50 años.
• en adultos mayores de 18 años que corren o correrán un mayor riesgo de contraer HZ debido a inmunodeficiencia o inmunosupresión causada por una enfermedad o terapia conocida.
Limitaciones de uso:
- •
- SHINGRIX no está indicado para la prevención de la infección primaria por varicela (viruela).
2 DOSIS Y ADMINISTRACIÓN
Solo para inyección intramuscular.
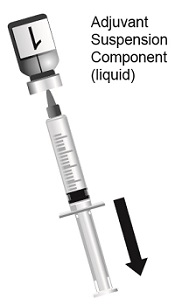
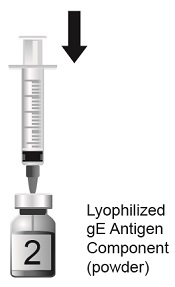
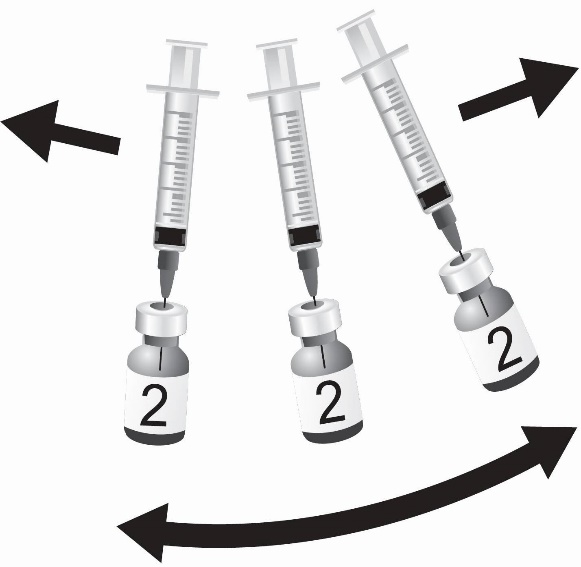
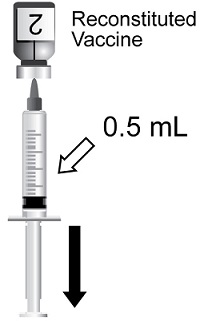
2.1 Reconstitución
SHINGRIX se suministra en 2 viales que deben combinarse antes de la administración. Prepare SHINGRIX reconstituyendo el componente de antígeno de glicoproteína E (gE) del virus varicela zóster liofilizado (polvo) con el componente de suspensión de adyuvante AS01B adjunto (líquido). Use solo el componente de suspensión de adyuvante suministrado (líquido) para la reconstitución. La vacuna reconstituida debe ser un líquido opalescente, incoloro a marrón pálido. Los productos farmacéuticos parenterales deben inspeccionarse visualmente en busca de partículas y decoloración antes de la administración, siempre que la solución y el contenedor lo permitan. Si existe alguna de estas condiciones, la vacuna no debe administrarse.
2.2 Instrucciones de administración
Solo para inyección intramuscular.
Después de la reconstitución, administre SHINGRIX inmediatamente o almacene refrigerado entre 2° y 8°C (36° y 46°F) y use dentro de las 6 horas. Deseche la vacuna reconstituida si no se usa dentro de las 6 horas.
Use una aguja estéril y una jeringa estéril separadas para cada individuo. El sitio preferido para la inyección intramuscular es la región deltoidea del brazo superior.
2.3 Dosis y programa
Dos dosis (0.5 mL cada una) administradas por vía intramuscular de acuerdo con los siguientes programas:
• Una primera dosis en el mes 0 seguida de una segunda dosis administrada de 2 a 6 meses después.
• Para las personas que son o serán inmunodeficientes o inmunosuprimidas y que se beneficiarían de un programa de vacunación más corto: una primera dosis en el mes 0 seguida de una segunda dosis administrada de 1 a 2 meses después.
3 FORMAS DE DOSIFICACIÓN Y CONCENTRACIONES
SHINGRIX es una suspensión para inyección que se suministra como un vial de dosis única de componente de antígeno gE liofilizado para reconstituirse con el vial adjunto de suspensión de adyuvante AS01B. Una dosis única después de la reconstitución es de 0,5 mL.
4 CONTRAINDICACIONES
No administre SHINGRIX a ninguna persona con antecedentes de una reacción alérgica grave (por ejemplo, anafilaxia) a cualquier componente de la vacuna o después de una dosis previa de SHINGRIX [ver Descripción (11)].
5 ADVERTENCIAS Y PRECAUCIONES
5.1 Prevención y manejo de reacciones alérgicas a las vacunas
Antes de la administración, el profesional de la salud debe revisar el historial de vacunación para detectar una posible sensibilidad a la vacuna y reacciones adversas relacionadas con la vacunación previa. Se debe contar con tratamiento médico y supervisión adecuados para manejar posibles reacciones anafilácticas después de la administración de SHINGRIX.
5.2 Síndrome de Guillain-Barré (GBS)
En un estudio observacional posterior a la comercialización, se observó un mayor riesgo de GBS durante los 42 días posteriores a la vacunación con SHINGRIX [ver Reacciones adversas (6.2)].
5.3 Síncope
El síncope (desmayo) puede estar asociado con la administración de vacunas inyectables, incluido SHINGRIX. El síncope puede estar acompañado de signos neurológicos transitorios como alteraciones visuales, parestesia y movimientos tónico-clónicos de las extremidades. Se deben implementar procedimientos para evitar lesiones por caídas y restaurar la perfusión cerebral después del síncope.
6 REACCIONES ADVERSAS
6.1 Experiencia en ensayos clínicos
Debido a que los ensayos clínicos se llevan a cabo en condiciones muy variadas, las tasas de reacciones adversas observadas en los ensayos clínicos de una vacuna no se pueden comparar directamente con las tasas en los ensayos clínicos de otra vacuna y puede que no reflejen las tasas observadas en la práctica. Existe la posibilidad de que un uso amplio de SHINGRIX pudiera revelar reacciones adversas que no se observaron en los ensayos clínicos.
Adultos de 50 años o más
En general, 17.041 adultos de 50 años o más recibieron al menos 1 dosis de SHINGRIX en 17 estudios clínicos.
La seguridad de SHINGRIX se evaluó agrupando datos de 2 estudios clínicos controlados con placebo (Estudios 1 y 2) que involucraron a 29.305 sujetos de 50 años o más que recibieron al menos 1 dosis de SHINGRIX (n = 14.645) o placebo salino (n = 14.660) administrado de acuerdo con un esquema de 0 y 2 meses. Al momento de la vacunación, la edad media de la población era de 69 años; 7.286 (25%) sujetos tenían entre 50 y 59 años, 4.488 (15%) sujetos tenían entre 60 y 69 años y 17.531 (60%) sujetos tenían 70 años o más. Ambos estudios se llevaron a cabo en América del Norte, América Latina, Europa, Asia y Australia. En la población general, la mayoría de los sujetos eran blancos (74%), seguidos por asiáticos (18%), negros (1,4%) y otros grupos raciales o étnicos (6%); el 58% eran mujeres.
Reacciones adversas solicitadas: En los Estudios 1 y 2, los datos sobre reacciones adversas locales y generales solicitadas se recopilaron utilizando tarjetas de diario estandarizadas durante 7 días después de cada dosis de la vacuna o del placebo (es decir, el día de la vacunación y los siguientes 6 días) en un subconjunto de sujetos (n = 4.886 recibiendo SHINGRIX, n = 4.881 recibiendo placebo con al menos 1 dosis documentada). A través de ambos estudios, los porcentajes de sujetos de 50 años o más que informaron cada reacción adversa local y general solicitada después de la administración de SHINGRIX (ambas dosis combinadas) fueron dolor (78%), enrojecimiento (38%) y hinchazón (26%); y mialgia (45%), fatiga (45%), dolor de cabeza (38%), escalofríos (27%), fiebre (21%) y síntomas gastrointestinales (17%).
Las frecuencias reportadas de reacciones adversas locales específicas solicitadas y reacciones adversas generales (por sujeto en general), por grupo de edad, de los 2 estudios se presentan en Tabla 1.
| La cohorte vacunada total para la seguridad incluyó todos los sujetos con al menos 1 dosis documentada (n). a 7 días incluyeron el día de la vacunación y los 6 días posteriores. b Los datos de los sujetos de 50 a 59 años y de 60 a 69 años se basan en el Estudio 1. Los datos de los sujetos de 70 años o más se basan en datos agrupados del Estudio 1: NCT01165177 y del Estudio 2: NCT01165229. c El placebo fue una solución salina. d Dolor grado 3: Se define como dolor significativo en reposo; impide las actividades diarias normales. e Mialgia grado 3, fatiga, dolor de cabeza, escalofríos y GI: Se define como impide la actividad normal. f Fiebre definida como ≥37,5°C/99,5°F por vía oral, axilar o timpánica, o ≥38°C/100,4°F por vía rectal; fiebre grado 3 definida como >39,0°C/102,2°F. g GI = Síntomas gastrointestinales que incluyen náuseas, vómitos, diarrea y/o dolor abdominal. |
||||||
|
Reacciones adversas |
50-59 años |
60-69 años |
≥70 años |
|||
|
SHINGRIX |
Placeboc |
SHINGRIX |
Placeboc |
SHINGRIX |
Placeboc |
|
|
Reacciones adversas locales |
n = 1.315 % |
n = 1.312 % |
n = 1.311 % |
n = 1.305 % |
n = 2.258 % |
n = 2.263 % |
|
Dolor |
88 |
14 |
83 |
11 |
69 |
9 |
|
Dolor, Grado 3d |
10 |
1 |
7 |
1 |
4 |
0.2 |
|
Enrojecimiento |
39 |
1 |
38 |
2 |
38 |
1 |
|
Enrojecimiento, >100 mm |
3 |
0 |
3 |
0 |
3 |
0 |
|
Hinchazón |
31 |
1 |
27 |
1 |
23 |
1 |
|
Hinchazón, >100 mm |
1 |
0 |
1 |
0 |
1 |
0 |
|
Reacciones adversas generales |
n = 1,315 % |
n = 1,312 % |
n = 1,309 % |
n = 1,305 % |
n = 2,252 % |
n = 2,264 % |
|
Mialgia |
57 |
15 |
49 |
11 |
35 |
10 |
|
Mialgia, Grado 3e |
9 |
1 |
5 |
1 |
3 |
0.4 |
|
Fatiga |
57 |
20 |
46 |
17 |
37 |
14 |
|
Fatiga, Grado 3e |
9 |
2 |
5 |
1 |
4 |
1 |
|
Dolor de cabeza |
51 |
22 |
40 |
16 |
29 |
12 |
|
Dolor de cabeza, Grado 3e |
6 |
2 |
4 |
0.2 |
2 |
0.4 |
|
Temblores |
36 |
7 |
30 |
6 |
20 |
5 |
|
Temblores, Grado 3e |
7 |
0.2 |
5 |
0.3 |
2 |
0.3 |
|
Fiebre |
28 |
3 |
24 |
3 |
14 |
3 |
|
Fiebre, Grado 3f |
0.4 |
0.2 |
1 |
0.2 |
0.1 |
0.1 |
|
GIg |
24 |
11 |
17 |
9 |
14 |
8 |
|
GI, Grado 3e |
2 |
1 |
1 |
1 |
1 |
0.4 |
La incidencia de reacciones locales y generales solicitadas fue menor en sujetos de 70 años o más en comparación con los de 50 a 69 años.
Las reacciones adversas locales y generales observadas con SHINGRIX tuvieron una mediana de duración de 2 a 3 días.
No hubo diferencias en las proporciones de sujetos que informaron cualquier reacción local solicitada o de Grado 3 entre la Dosis 1 y la Dosis 2. Los dolores de cabeza y los escalofríos fueron reportados más frecuentemente por los sujetos después de la Dosis 2 (28% y 21%, respectivamente) en comparación con la Dosis 1 (24% y 14%, respectivamente). Las reacciones adversas generales solicitadas de Grado 3 (dolores de cabeza, escalofríos, mialgia y fatiga) fueron reportadas más frecuentemente por los sujetos después de la Dosis 2 (2.3%, 3%, 4% y 4%, respectivamente) en comparación con la Dosis 1 (1.4%, 1.4%, 2.3% y 2.4%, respectivamente).
Eventos Adversos No Solicitados: Los eventos adversos no solicitados que ocurrieron dentro de los 30 días siguientes a cada vacunación (Día 0 a 29) fueron registrados en una tarjeta de diario por todos los sujetos. En los 2 estudios, eventos adversos no solicitados que ocurrieron dentro de los 30 días de la vacunación fueron reportados en el 51% y el 32% de los sujetos que recibieron SHINGRIX (n = 14.645) o placebo (n = 14.660), respectivamente (cohorte total vacunada). Eventos adversos no solicitados que ocurrieron en ≥ 1% de los receptores de SHINGRIX y a una tasa al menos 1.5 veces mayor que el placebo incluyeron escalofríos (4% versus 0.2%), prurito en el sitio de inyección (2.2% versus 0.2%), malestar (1.7% versus 0.3%), artralgia (1.7% versus 1.2%), náuseas (1.4% versus 0.5%) y mareos (1.2% versus 0.8%).
La gota (incluyendo la artritis gotosa) fue reportada por 0.18% (n = 27) versus 0.05% (n = 8) de los sujetos que recibieron SHINGRIX o placebo, respectivamente, dentro de los 30 días de la vacunación; la información disponible es insuficiente para determinar una relación causal con SHINGRIX.
Eventos Adversos Graves (EAG): En los 2 estudios, los EAG fueron reportados a tasas similares en sujetos que recibieron SHINGRIX (2.3%) o placebo (2.2%) desde la primera dosis administrada hasta 30 días después de la última vacunación. Los EAG fueron reportados en el 10.1% de los sujetos que recibieron SHINGRIX y en el 10.4% de los sujetos que recibieron placebo desde la primera dosis administrada hasta 1 año después de la última vacunación. Un sujeto (< 0.01%) reportó linfadenitis y un sujeto (< 0.01%) reportó fiebre mayor de 39 °C; existía una base para una relación causal con SHINGRIX.
La neuropatía isquémica óptica fue reportada en 3 sujetos (0.02%) que recibieron SHINGRIX (todos dentro de los 50 días posteriores a la vacunación) y 0 sujetos que recibieron placebo; la información disponible es insuficiente para determinar una relación causal con SHINGRIX.
Muertes: Desde la primera dosis administrada hasta 30 días después de la última vacunación, las muertes fueron reportadas en el 0.04% de los sujetos que recibieron SHINGRIX y en el 0.05% de los sujetos que recibieron placebo en los 2 estudios. Desde la primera dosis administrada hasta 1 año después de la última vacunación, las muertes fueron reportadas en el 0.8% de los sujetos que recibieron SHINGRIX y en el 0.9% de los sujetos que recibieron placebo. Las causas de muerte entre los sujetos fueron consistentes con las generalmente reportadas en poblaciones adultas y ancianas.
Enfermedades Potencialmente Mediadas por el Sistema Inmune: En los 2 estudios, el inicio de nuevas enfermedades potencialmente mediadas por el sistema inmune (pIMD) o la exacerbación de pIMD existentes fueron reportadas en el 0.6% de los sujetos que recibieron SHINGRIX y en el 0.7% de los sujetos que recibieron placebo desde la primera dosis administrada hasta 1 año después de la última vacunación. Las pIMD más frecuentemente reportadas ocurrieron con frecuencias comparables en el grupo que recibió SHINGRIX y el grupo de placebo.
Calendario de Dosis: En un estudio clínico de etiqueta abierta, 238 sujetos de 50 años o más recibieron SHINGRIX con un calendario de 0 y 2 meses o 0 y 6 meses. El perfil de seguridad de SHINGRIX fue similar cuando se administró de acuerdo con un calendario de 0 y 2 meses o 0 y 6 meses y fue consistente con el observado en los Estudios 1 y 2.
Adultos Inmunocomprometidos de 18 Años o Más
La seguridad de SHINGRIX fue evaluada en 6 estudios clínicos controlados con placebo que inscribieron 3.116 sujetos de 18 años o más provenientes de 5 poblaciones inmunodeficientes o inmunosuprimidas diferentes (denominadas inmunocomprometidos), en los que un total de 1.587 recibieron SHINGRIX. En todos los estudios, los sujetos recibieron las Dosis 1 y 2 de SHINGRIX con 1 a 2 meses de diferencia. La monitorización de seguridad para estos estudios fue similar a los Estudios 1 y 2. Además, los sujetos fueron monitoreados para eventos relevantes a su enfermedad o condición específica.
Al momento de la recepción de SHINGRIX o placebo, la edad media de la población era de 55 años; el 28% de los sujetos tenían entre 18 y 49 años y el 72% de los sujetos tenían 50 años o más. Cada uno de los estudios fue conducido en una o más de las siguientes regiones: América del Norte, América Latina, Europa, Asia, África y Australia/Nueva Zelanda. La mayoría de los sujetos eran blancos (77%), seguidos por asiáticos (17%), negros (2%) y otros grupos raciales (3%); el 4% eran de etnia hispana o latina americana; el 37% eran mujeres.
| a La primera dosis fue administrada dentro de los 50 a 70 días después del trasplante autólogo de células madre hematopoyéticas. b El seguimiento de seguridad fue impulsado por la acumulación de casos de herpes zoster y varió desde un mínimo de 12 meses después de la última vacunación hasta 4 años a nivel del sujeto. c Para los sujetos que fueron vacunados durante un curso de terapia contra el cáncer, cada dosis fue administrada con al menos 10 días entre la vacunación y los ciclos de terapia contra el cáncer. d Para los sujetos que recibieron la vacunación después de un curso completo de terapia contra el cáncer, la primera dosis fue administrada de 10 días a 6 meses después de que la terapia contra el cáncer había finalizado. e La primera dosis fue administrada entre 4 y 18 meses después del trasplante renal. f En el grupo PreChemo (TVC: SHINGRIX [n = 90], placebo [n = 91]), la primera dosis fue administrada un máximo de 1 mes a un mínimo de 10 días antes del inicio de un ciclo de quimioterapia, y la segunda dosis fue administrada en el primer día de un ciclo de quimioterapia. g En el grupo OnChemo (TVC: SHINGRIX [n = 27], placebo [n = 24]), cada dosis fue administrada en el primer día de un ciclo de quimioterapia. |
|||||||||||
|
Estudios Clínicos |
Número de Sujetos Vacunados |
Población del Estudio |
Período de Seguimiento de Seguridad |
||||||||
|
SHINGRIX |
Placebo |
||||||||||
|
auHSCT (NCT01610414) |
922 |
924 |
Receptores de trasplante de células madre hematopoyéticas autólogasa |
Seguimiento de seguridad mediano de 29 mesesb |
|||||||
|
Neoplasias Hematológicas (NCT01767467) |
283 |
279 |
Neoplasias hematológicasc,d |
12 meses después de la última vacunación |
|||||||
|
Trasplante Renal (NCT02058589) |
132 |
132 |
Receptores de trasplante renale |
12 meses después de la última vacunación |
|||||||
|
Tumores Sólidos |
117 |
115 |
Tumores sólidos que reciben quimioterapiaf,g |
12 meses después de la última vacunación |
|||||||
|
VIH (NCT01165203) |
74 |
49 |
Sujetos infectados por VIH |
12 meses después de la última vacunación |
|||||||
|
auHSCT (NCT00920218) |
59 |
30 |
Receptores de trasplante de células madre hematopoyéticas autólogasa |
12 meses después de la última vacunación |
|||||||
En el estudio auHSCT (NCT01610414), en el momento de la recepción de SHINGRIX o placebo, la edad media de la población era de 55 años; el 25% de los sujetos tenían entre 18 y 49 años y el 75% tenía 50 años o más. La mayoría de los sujetos eran blancos (78%), seguidos por asiáticos (16%), negros (2%) y otros grupos raciales (3%); el 3% eran de etnia hispana o latina estadounidense; el 37% eran mujeres.
Reacciones adversas solicitadas: Las reacciones adversas locales solicitadas reportadas dentro de los 7 días posteriores a la administración de SHINGRIX (ambas dosis combinadas) en los receptores auHSCT (con edades de 18 a 49 y ≥50 años) fueron dolor (88% y 83%), enrojecimiento (30% y 35%) e hinchazón (21% y 18%). Las reacciones adversas generales solicitadas reportadas dentro de los 7 días posteriores a la administración de SHINGRIX (ambas dosis combinadas) en los receptores auHSCT (con edades de 18 a 49 y ≥50 años) fueron fatiga (64% y 54%), mialgia (58% y 52%), dolor de cabeza (44% y 30%), síntomas gastrointestinales (21% y 28%), escalofríos (31% y 25%) y fiebre (28% y 18%). Los porcentajes de sujetos de 18 años o más que reportaron cada reacción adversa local y general solicitada después de la administración de cada dosis de SHINGRIX o placebo en el estudio auHSCT (NCT01610414) se presentan en Tabla 3.
| La cohorte total vacunada (TVC) para la seguridad incluyó a todos los sujetos con al menos 1 dosis documentada (n). % = Porcentaje de sujetos que reportaron el síntoma al menos una vez. a Los 7 días incluyeron el día de la vacunación y los 6 días posteriores. b El placebo era sacarosa reconstituida con solución salina. c Dolor de grado 3: definido como dolor significativo en reposo que impide las actividades cotidianas normales. d Mialgia de grado 3, fatiga, dolor de cabeza, escalofríos y GI: definidos como que impiden la actividad normal. e GI = Síntomas gastrointestinales que incluyen náuseas, vómitos, diarrea y/o dolor abdominal. |
||||||||||||||||||||
|
Reacciones adversas |
Adultos de 18-49 años |
Adultos ≥ 50 años |
||||||||||||||||||
|
SHINGRIX |
Placebob |
SHINGRIX |
Placebob |
|||||||||||||||||
|
Dosis 1 |
Dosis 2 |
Dosis 1 |
Dosis 2 |
Dosis 1 |
Dosis 2 |
Dosis 1 |
Dosis 2 |
|||||||||||||
|
Reacciones adversas locales |
n = 223 |
n = 205 |
n = 217 |
n = 207 |
n = 673 |
n = 635 |
n = 673 |
n = 627 |
||||||||||||
|
Dolor |
81 |
82 |
8 |
6 |
75 |
74 |
6 |
5 |
||||||||||||
|
Dolor, Grado 3c |
11 |
11 |
1 |
0 |
5 |
7 |
0.3 |
0 |
||||||||||||
|
Enrojecimiento |
20 |
25 |
0 |
0 |
21 |
28 |
1 |
1 |
||||||||||||
|
Enrojecimiento, >100 mm |
1 |
2 |
0 |
0 |
1 |
3 |
0 |
0 |
||||||||||||
|
Hinchazón |
14 |
17 |
0 |
0 |
10 |
15 |
1 |
1 |
||||||||||||
|
Hinchazón, >100 mm |
0 |
2 |
0 |
0 |
0.1 |
1 |
0 |
0 |
||||||||||||
|
Reacciones adversas generales |
n = 222 |
n = 203 % |
n = 218 |
n = 207 |
n = 674 |
n = 633 |
n = 674 |
n = 628 |
||||||||||||
|
Mialgia |
41 |
51 |
22 |
21 |
37 |
43 |
18 |
17 |
||||||||||||
|
Mialgia, Grado 3d |
4 |
8 |
2 |
2 |
2 |
4 |
1 |
1 |
||||||||||||
|
Fatiga |
49 |
51 |
34 |
25 |
37 |
46 |
31 |
26 |
||||||||||||
|
Fatiga, Grado 3d |
6 |
10 |
1 |
2 |
3 |
4 |
2 |
3 |
||||||||||||
|
Dolor de cabeza |
23 |
38 |
17 |
17 |
15 |
25 |
13 |
8 |
||||||||||||
|
Dolor de cabeza, Grado 3d |
1 |
5 |
0 |
2 |
0.1 |
2 |
0.4 |
1 |
||||||||||||
|
Temblores |
20 |
26 |
12 |
6 |
11 |
21 |
7 |
7 |
||||||||||||
|
Temblores, Grado 3d |
1 |
6 |
0 |
0 |
0.4 |
3 |
1 |
0.2 |
||||||||||||
|
Fiebre, ≥37.5°C/99.5°F |
9 |
28 |
4 |
2 |
6 |
15 |
3 |
4 |
||||||||||||
|
Fiebre, Grado 3 >39.5°C/103.1°F |
0 |
1 |
0 |
0 |
0.1 |
0.2 |
0 |
0.2 |
||||||||||||
|
GIe |
14 |
13 |
13 |
12 |
18 |
18 |
16 |
12 |
||||||||||||
|
GI, Grado 3d |
1 |
1 |
0 |
1 |
1 |
2 |
1 |
2 |
||||||||||||
En general, las frecuencias informadas de reacciones adversas locales y generales solicitadas en los otros estudios en poblaciones inmunocomprometidas fueron similares a las del estudio auHSCT (NCT01610414). Las reacciones adversas locales y generales observadas con SHINGRIX tuvieron una duración mediana de 1 a 3 días en todos los estudios que reclutaron sujetos inmunocomprometidos.
Eventos adversos no solicitados: En los 6 estudios que reclutaron sujetos inmunocomprometidos, se informaron eventos adversos no solicitados, incluidos eventos graves y no graves, que ocurrieron dentro de los 30 días posteriores a cada vacunación en el 46% y el 44% de los sujetos que recibieron SHINGRIX o placebo. Los eventos adversos de artralgia, neumonía infecciosa e infección similar a la gripe ocurrieron en ≥1% de los receptores de SHINGRIX y a una tasa al menos 1,5 veces mayor que el placebo (1,5% versus 1,0%, 1,5% versus 0,9% y 1,3% versus 0,6%, respectivamente).
Eventos adversos graves: En los 6 estudios que reclutaron sujetos inmunocomprometidos, se informaron SAE a tasas similares en los sujetos que recibieron SHINGRIX (7%) o placebo (8%) desde la primera dosis administrada hasta 30 días después de la última vacunación. Se informaron SAE para el 26% de los sujetos que recibieron SHINGRIX y para el 27% de los sujetos que recibieron placebo desde la primera dosis administrada hasta 1 año después de la última vacunación. Se informaron SAE de neumonía infecciosa para 21 sujetos (1,3%) que recibieron SHINGRIX y para 11 sujetos (0,7%) que recibieron placebo hasta 30 días después de la última vacunación. La información disponible es insuficiente para determinar una relación causal con la vacunación.
Muertes: En los 6 estudios que reclutaron sujetos inmunocomprometidos, desde la primera dosis administrada hasta 30 días después de la última vacunación, se informaron muertes para 2 sujetos (0,1%) que recibieron SHINGRIX y 7 sujetos (0,5%) que recibieron placebo. Desde la primera dosis administrada hasta 1 año después de la última vacunación, se informaron muertes para el 6% de los sujetos que recibieron SHINGRIX y para el 6% de los sujetos que recibieron placebo. Las causas de muerte entre los sujetos fueron consistentes con las esperadas en las poblaciones evaluadas.
Posibles enfermedades inmunomediadas: En los 6 estudios que reclutaron sujetos inmunocomprometidos, se informaron nuevos casos de pIMD o exacerbación de pIMD existentes para el 1,3% de los sujetos que recibieron SHINGRIX y el 1,0% de los sujetos que recibieron placebo desde la primera dosis administrada hasta 1 año después de la última vacunación. No hubo desequilibrios notables en pIMD específicos entre los grupos de tratamiento.
Otros eventos médicamente relevantes: En el estudio auHSCT (NCT01610414), se informó de recaída o progresión en 315 de 922 sujetos (34%) que recibieron al menos una dosis de SHINGRIX y 331 de 924 sujetos (36%) que recibieron placebo desde la primera vacunación hasta el final del estudio.
En el estudio auHSCT (NCT00920218), se informó de recaída o progresión en 17 de 59 sujetos (29%) que recibieron al menos una dosis de SHINGRIX y 8 de 30 sujetos (27%) que recibieron placebo desde la primera vacunación hasta el final del estudio.
En el estudio de malignidad hematológica, se informó de recaída o progresión en 45 de 283 sujetos (16%) que recibieron al menos una dosis de SHINGRIX y 58 de 279 sujetos (21%) que recibieron placebo desde la primera vacunación hasta el final del estudio.
En el estudio de trasplante renal, se informó de rechazo de aloinjerto confirmado por biopsia en 4 de 132 (3%) de los sujetos que recibieron SHINGRIX y en 7 de 132 (5%) de los sujetos que recibieron placebo desde la primera vacunación hasta el final del estudio (aproximadamente 13 meses después). La creatinina como medida de la función del injerto y los cambios en la aloinmunidad después de la vacunación no se evaluaron sistemáticamente.
En el estudio del VIH, se informó al menos 1 evento de empeoramiento de la condición del VIH en 9 de 74 (12%) de los sujetos que recibieron SHINGRIX y en 5 de 49 (10%) de los sujetos que recibieron placebo desde la primera vacunación hasta el final del estudio.
Administración concomitante con la vacuna neumocócica polisacárida 23-valente
En un estudio clínico abierto (NCT02045836) en sujetos de 50 años o más, se recopiló información sobre reacciones adversas locales y sistémicas solicitadas utilizando tarjetas de diario durante 7 días (es decir, el día de la vacunación y los 6 días siguientes). Cuando PNEUMOVAX 23 se administró conjuntamente con la primera dosis de SHINGRIX en comparación con cuando se administró la primera dosis de SHINGRIX sola, un mayor porcentaje de sujetos informó fiebre, definida como ≥37,5 °C/99,5 °F (16% frente a 7%, respectivamente) y escalofríos (21% frente a 7%, respectivamente) [ver Estudios clínicos (14.7)].
6.2 Experiencia postcomercialización
Las siguientes reacciones adversas se han identificado durante el uso posterior a la aprobación de SHINGRIX. Debido a que estas reacciones se informan voluntariamente de una población de tamaño incierto, no siempre es posible estimar su frecuencia de manera confiable o establecer una relación causal con la vacuna.
Trastornos generales y condiciones del sitio de administración
Disminución de la movilidad del brazo inyectado que puede persistir durante 1 o más semanas.
Trastornos del sistema inmunitario
Reacciones de hipersensibilidad, incluido angioedema, erupción cutánea y urticaria.
Trastornos del sistema nervioso
Síndrome de Guillain-Barré.
Estudio observacional postcomercialización del riesgo de síndrome de Guillain-Barré después de la vacunación con SHINGRIX
Se evaluó la asociación entre la vacunación con SHINGRIX y el SGB entre los beneficiarios de Medicare de 65 años o más. Utilizando datos de reclamos de Medicare, desde octubre de 2017 hasta febrero de 2020, se identificaron las vacunaciones con SHINGRIX entre los beneficiarios a través de los Códigos Nacionales de Medicamentos, y se identificaron posibles casos de SGB hospitalizado entre los receptores de SHINGRIX a través de los códigos de la Clasificación Internacional de Enfermedades.
El riesgo de SGB después de la vacunación con SHINGRIX se evaluó en análisis de series de casos autocontrolados utilizando una ventana de riesgo de 1 a 42 días después de la vacunación y una ventana de control de 43 a 183 días después de la vacunación. El análisis principal (basado en reclamos, todas las dosis) encontró un mayor riesgo de SGB durante los 42 días posteriores a la vacunación con SHINGRIX, con un estimado de 3 casos adicionales de SGB por millón de dosis administradas a adultos de 65 años o más. En análisis secundarios, se observó un mayor riesgo de SGB durante los 42 días posteriores a la primera dosis de SHINGRIX, con un estimado de 6 casos adicionales de SGB por millón de dosis administradas a adultos de 65 años o más, y no se observó un mayor riesgo de SGB después de la segunda dosis de SHINGRIX. Estos análisis de diagnósticos de SGB en datos de reclamos fueron respaldados por análisis de casos de SGB confirmados por revisión de registros médicos. Si bien los resultados de este estudio observacional sugieren una asociación causal del SGB con SHINGRIX, la evidencia disponible es insuficiente para establecer una relación causal.
8 USO EN POBLACIONES ESPECÍFICAS
8.1 Embarazo
Resumen de Riesgos
Todos los embarazos tienen un riesgo de defectos de nacimiento, pérdida u otros resultados adversos. En la población general de los EE. UU., el riesgo de fondo estimado de defectos de nacimiento mayores y aborto espontáneo en embarazos clínicamente reconocidos es del 2% al 4% y del 15% al 20%, respectivamente. Los datos son insuficientes para establecer si existe un riesgo asociado a la vacuna con SHINGRIX en mujeres embarazadas.
Se realizó un estudio de toxicidad del desarrollo en ratas hembras a las que se administró SHINGRIX o el adyuvante AS01B solo antes del apareamiento, durante la gestación y durante la lactancia. La dosis total fue de 0,2 mL en cada ocasión (una dosis humana única de SHINGRIX es de 0,5 mL). Este estudio no reveló efectos adversos en el desarrollo fetal o pre-destete debido a SHINGRIX (ver Datos).
Datos
Datos de animales: En un estudio de toxicidad del desarrollo, se administraron a ratas hembras SHINGRIX o el adyuvante AS01B solo por inyección intramuscular 28 y 14 días antes del apareamiento, en los días de gestación 3, 8, 11 y 15, y en el día de lactancia 7. La dosis total fue de 0,2 mL en cada ocasión (una dosis humana única de SHINGRIX es de 0,5 mL). No se observaron efectos adversos en el desarrollo pre-destete hasta el día 25 postnatal. No hubo malformaciones o variaciones fetales relacionadas con la vacuna.
8.2 Lactancia
Resumen de Riesgos
Se desconoce si SHINGRIX se excreta en la leche materna. No hay datos disponibles para evaluar los efectos de SHINGRIX en el lactante amamantado o en la producción/excreción de leche.
Los beneficios para el desarrollo y la salud de la lactancia materna deben considerarse junto con la necesidad clínica de la madre de SHINGRIX y cualquier posible efecto adverso en el niño amamantado por SHINGRIX o por la condición materna subyacente. Para las vacunas preventivas, la condición materna subyacente es la susceptibilidad a la enfermedad que previene la vacuna.
8.4 Uso Pediátrico
No se ha establecido la seguridad y eficacia en individuos menores de 18 años. SHINGRIX no está indicado para la prevención de la infección primaria por varicela (varicela).
8.5 Uso Geriátrico
Adultos de 60 años o más
Del total de sujetos que recibieron al menos 1 dosis de SHINGRIX en los Estudios 1 y 2 (n = 14.645), 2.243 (15%) tenían entre 60 y 69 años, 6.837 (47%) tenían entre 70 y 79 años y 1.921 (13%) tenían 80 años o más. No hubo diferencias clínicamente significativas en la eficacia entre los grupos de edad. [Ver Estudios Clínicos (14.1, 14.2, 14.3).]
Las frecuencias de reacciones adversas locales y generales solicitadas en sujetos de 70 años o más fueron más bajas que en adultos más jóvenes (de 50 a 69 años). [Ver Reacciones Adversas (6.1).]
Adultos inmunocomprometidos de 65 años o más
Del total de sujetos que recibieron al menos 1 dosis de SHINGRIX en el estudio auHSCT (n = 922), 172 (18,7%) tenían 65 años o más [ver Estudios Clínicos (14.5)]. No hubo diferencias clínicamente significativas en la eficacia entre estos sujetos y los adultos más jóvenes (de 18 a 64 años).
Del total de sujetos que recibieron al menos 1 dosis de SHINGRIX en los 6 estudios en sujetos inmunocomprometidos (n = 1.587), 337 (21,2%) tenían 65 años o más. Las frecuencias de reacciones adversas locales y generales solicitadas en sujetos de 65 años o más fueron generalmente similares o más bajas que las reportadas por adultos más jóvenes (de 18 a 64 años).
11 DESCRIPCIÓN
SHINGRIX (Vacuna recombinante contra el zoster, adyuvada) es una suspensión estéril para inyección intramuscular. La vacuna se presenta como un frasco de componente antigénico recombinante de la glicoproteína E de superficie del virus del zoster varicela (gE) liofilizado, que debe reconstitucionarse en el momento de su uso con el frasco adjunto de componente de suspensión adyuvante AS01B. El componente antigénico gE liofilizado se presenta en forma de un polvo blanco estéril. El componente de suspensión adyuvante AS01B es un líquido opalescente, incoloro a ligeramente marrón pálido suministrado en frascos.
El antígeno gE se obtiene mediante el cultivo de células de ovario de hámster chino genéticamente modificadas, que llevan un gen de gE truncado, en medios que contienen aminoácidos, sin albúmina, antibióticos o proteínas de origen animal. La proteína gE se purifica mediante varios pasos cromatográficos, se formula con excipientes, se llena en frascos y se liofiliza.
El componente de suspensión adyuvante es AS01B, que está compuesto por 3-O-desacil-4’-monofosforil lípido A (MPL) de Salmonella minnesota y QS-21, una saponina purificada a partir de extracto vegetal Quillaja saponaria Molina, combinados en una formulación liposomal. Los liposomas están compuestos de dioleoil fosfatidilcolina (DOPC) y colesterol en solución salina tamponada con fosfato que contiene fosfato disódico anhidro, fosfato monopotásico dihidrogeno, cloruro sódico y agua para inyección.
Después de la reconstitución, cada dosis de 0,5 ml está formulada para contener 50 mcg del antígeno gE recombinante, 50 mcg de MPL y 50 mcg de QS-21. Cada dosis también contiene 20 mg de sacarosa (como estabilizante), 4,385 mg de cloruro sódico, 1 mg de DOPC, 0,54 mg de fosfato monopotásico dihidrogeno, 0,25 mg de colesterol, 0,160 mg de fosfato monosódico dihidrato, 0,15 mg de fosfato disódico anhidro, 0,116 mg de fosfato dipotásico y 0,08 mg de polisorbato 80. Después de la reconstitución, SHINGRIX es un líquido estéril, opalescente, incoloro a ligeramente marrón pálido.
SHINGRIX no contiene conservantes. Cada dosis también puede contener cantidades residuales de proteínas de células hospedadoras (≤3,0%) y ADN (≤2,1 picogramos) procedentes del proceso de fabricación.
Los tapones de los frascos no están hechos con látex de caucho natural.
12 FARMACOLOGÍA CLÍNICA
12.1 Mecanismo de acción
El riesgo de desarrollar HZ, que aumenta con la edad y con la inmunosupresión debido a la enfermedad y/o la terapia, parece estar relacionado con una disminución de la inmunidad específica al virus varicela zóster (VZV). Se demostró que SHINGRIX aumenta la respuesta inmunitaria específica al VZV, que se cree que es el mecanismo por el cual protege contra la enfermedad del zóster [ver Estudios clínicos (14)].
13 TOXICOLOGÍA NO CLÍNICA
13.1 Carcinogénesis, Mutagénesis, Deterioro de la Fertilidad
SHINGRIX no se ha evaluado para su potencial carcinogénico o mutagénico. La vacunación de ratas hembras con SHINGRIX no tuvo ningún efecto sobre la fertilidad [ver Uso en Poblaciones Específicas (8.1)]. En un estudio de fertilidad masculina, las ratas fueron vacunadas con 0.1 mL de SHINGRIX (una dosis humana única es de 0.5 mL) 42, 28 y 14 días antes del apareamiento. No hubo efectos sobre la fertilidad masculina.
14 ESTUDIOS CLÍNICOS
14.1 Eficacia en sujetos de 50 años o más
El estudio 1 fue un estudio clínico aleatorizado, controlado con placebo, ciegoobservador realizado en 18 países. La aleatorización se estratificó (8:5:3:1) por edad: 50 a 59 años, 60 a 69 años, 70 a 79 años y ≥80 años. Entre otros, el estudio excluyó a sujetos inmunocomprometidos, que tuvieran antecedentes de HZ anteriores, que hubieran sido vacunados contra la varicela o la HZ, y a pacientes cuya supervivencia no se esperaba que fuera al menos de 4 años o que tuvieran condiciones que pudieran interferir con las evaluaciones del estudio. Los sujetos fueron seguidos para el desarrollo de HZ y neuralgia postherpética (PHN) durante una mediana de 3.1 años (rango: 0 a 3.7 años). Los casos sospechosos de HZ se siguieron prospectivamente para el desarrollo de PHN, una complicación relacionada con la HZ definida como dolor asociado a la HZ (calificado como 3 o más en una escala de 0 a 10 por el sujeto del estudio) que ocurra o persista al menos 90 días después del inicio del sarpullido en casos confirmados de HZ.
La población de análisis de eficacia primaria (denominada cohorte total vacunada modificada [mTVC]) incluyó 14 759 sujetos de 50 años o más que recibieron 2 dosis (0 y 2 meses) de SHINGRIX (n = 7 344) o placebo (n = 7 415) y no desarrollaron un caso confirmado de HZ dentro de 1 mes después de la segunda dosis. En la población mTVC, el 61 % eran mujeres; el 72 % eran blancas, el 19 % eran asiáticas, el 1,7 % eran negras y el 7 % pertenecían a otros grupos raciales/étnicos. La edad media de los sujetos era de 62,3 años.
Los casos confirmados de HZ se determinaron mediante reacción en cadena de la polimerasa (PCR) (89,4 %) o un comité de evaluación clínica (10,6%).
Eficacia contra el Herpes Zoster
En comparación con el placebo, SHINGRIX redujo significativamente el riesgo de desarrollar HZ en un 97,2 % (95 % IC: 93,7, 99,0) en sujetos de 50 años o más (Tabla 4).
| N = Número de sujetos incluidos en cada grupo; n = Número de sujetos que tuvieron al menos 1 episodio confirmado de HZ; HZ = Herpes zoster; IC = Intervalo de confianza. a Estudio 1: NCT01165177. b mTVC = Cohorte total vacunada modificada definida como sujetos que recibieron 2 dosis (0 y 2 meses) de SHINGRIX o placebo y no desarrollaron un caso confirmado de HZ dentro de 1 mes después de la segunda dosis. c El punto final de estudio primario se basó en casos confirmados de HZ en sujetos de 50 años o más. |
|||||||
|
Grupo de edad (Años) |
SHINGRIX |
Placebo |
% Eficacia (95 % IC) |
||||
|
N |
n |
Tasa de incidencia de HZ por 1.000 personas-años |
N |
n |
Tasa de incidencia de HZ por 1.000 personas-años |
||
|
Total (≥50)c |
7.344 |
6 |
0,3 |
7.415 |
210 |
9,1 |
97,2 (93,7, 99,0) |
|
50-59 |
3.492 |
3 |
0,3 |
3.525 |
87 |
7,8 |
96,6 (89,6, 99,3) |
|
60-69 |
2.141 |
2 |
0,3 |
2.166 |
75 |
10,8 |
97,4 (90,1, 99,7) |
|
≥70 |
1,711 |
1 |
0.2 |
1,724 |
48 |
9.4 |
97.9 (87.9, 100.0) |
En un análisis descriptivo, la eficacia de la vacuna contra la HZ en sujetos de 50 años y mayores fue del 93,1 % (95% IC: 81,3, 98,2) en el cuarto año posterior a la vacunación.
Ocurrencia de neuralgia posherpética
Entre todos los sujetos de 50 años o mayores en la mTVC, no se informaron casos de PHN en el grupo de la vacuna en comparación con 18 casos informados en el grupo placebo.
14.2 Eficacia en sujetos de 70 años y mayores
El Estudio 2 fue un estudio clínico aleatorizado, controlado con placebo, ciego observador realizado en 18 países. La aleatorización se estratificó (3:1) por edad: 70 a 79 años y ≥80 años. Con la excepción de la edad, los criterios de exclusión del estudio fueron los mismos que para el Estudio 1. Los sujetos fueron seguidos para el desarrollo de HZ y PHN durante una mediana de 3,9 años (rango: 0 a 4,5 años). Los casos sospechosos de HZ se siguieron prospectivamente para el desarrollo de PHN como en el Estudio 1.
La población de análisis de eficacia primaria (mTVC) incluyó a 13 163 sujetos de 70 años y mayores que recibieron 2 dosis (0 y 2 meses) de SHINGRIX (n = 6541) o placebo (n = 6622) y no desarrollaron un caso confirmado de HZ en un mes después de la segunda dosis. En la población mTVC, el 55% eran mujeres; el 78% eran blancos, el 17% eran asiáticos, el 1% eran negros y el 4% eran de otros grupos raciales/étnicos. La edad media de los sujetos fue de 75,5 años.
Los casos confirmados de HZ se determinaron ya sea por PCR (92,3%) o por un Comité de Evaluación Clínica (7,7%).
Eficacia contra el herpes zóster
Los resultados de la eficacia de la vacuna contra la HZ en sujetos de 70 años y mayores se muestran en Tabla 5.
| N = Número de sujetos incluidos en cada grupo; n = Número de sujetos que tuvieron al menos 1 episodio confirmado de HZ; HZ = Herpes zóster; CI = Intervalo de confianza. a Estudio 2: NCT01165229. b mTVC = Cohorte vacunada total modificada definida como sujetos que recibieron 2 dosis (0 y 2 meses) de SHINGRIX o placebo y no desarrollaron un caso confirmado de HZ en un mes después de la segunda dosis. c El punto final primario del estudio se basó en los casos confirmados de HZ en sujetos de 70 años y mayores. |
|||||||
|
Grupo de edad (años) |
SHINGRIX |
Placebo |
% Eficacia (95% CI) |
||||
|
N |
n |
Tasa de incidencia de HZ por 1000 personas-años |
N |
n |
Tasa de incidencia de HZ por 1000 personas-años |
||
|
En general (≥70)c |
6541 |
23 |
0,9 |
6622 |
223 |
9,2 |
89,8 (84,3, 93,7) |
|
70 – 79 |
5114 |
17 |
0,9 |
5189 |
169 |
8,8 |
90,0 (83,5, 94,3) |
|
≥80 |
1427 |
6 |
1,2 |
1433 |
54 |
11,0 |
89,1 (74,7, 96,2) |
En un análisis descriptivo, la eficacia de la vacuna contra el HZ en sujetos de 70 años o más fue del 85,1% (IC del 95%: 64,5, 94,8) en el cuarto año después de la vacunación.
Eficacia contra la neuralgia posherpética
Entre todos los sujetos de 70 años o más en el mTVC, se informaron 4 casos de PHN en el grupo de la vacuna en comparación con 28 casos informados en el grupo placebo. La eficacia de la vacuna contra la PHN fue del 85,5% (IC del 95%: [58,5; 96,3]). El beneficio de SHINGRIX en la prevención de la PHN se puede atribuir al efecto de la vacuna en la prevención del HZ.
Reducción del uso de medicamentos para el dolor
Entre los sujetos con HZ confirmado, se informó el uso de medicamentos para el dolor asociados con el HZ para 10 de 23 sujetos (43,5%) que recibieron SHINGRIX y para 160 de 223 sujetos (71,7%) que recibieron placebo.
14.3 Análisis de eficacia agrupados en los estudios 1 y 2
La eficacia de SHINGRIX para prevenir el HZ y la PHN en sujetos de 70 años o más se evaluó combinando los resultados de los estudios 1 y 2 mediante un análisis agrupado preespecificado en el mTVC. Se incluyeron un total de 8.250 y 8.346 sujetos que recibieron SHINGRIX y placebo, respectivamente, en el análisis agrupado de mTVC.
Eficacia contra el herpes zóster
En comparación con el placebo, SHINGRIX redujo significativamente el riesgo de desarrollar HZ en un 91,3% (IC del 95%: 86,9, 94,5) en sujetos de 70 años o más (Tabla 6).
| N = Número de sujetos incluidos en cada grupo; n = Número de sujetos que tienen al menos 1 episodio confirmado de HZ; HZ = Herpes zóster; IC = Intervalo de confianza. a Datos agrupados del estudio 1: NCT01165177 (sujetos ≥50 años) y estudio 2: NCT01165229 (sujetos ≥70 años). b mTVC = Cohorte total vacunada modificada definida como sujetos que recibieron 2 dosis (0 y 2 meses) de SHINGRIX o placebo y no desarrollaron un caso confirmado de HZ dentro de 1 mes después de la segunda dosis. c El criterio de valoración principal del análisis agrupado se basó en casos confirmados de HZ en sujetos de 70 años o más. |
|||||||
|
Grupo de edad (años) |
SHINGRIX |
Placebo |
% Eficacia (IC del 95%) |
||||
|
N |
n |
Tasa de incidencia de HZ por 1.000 personas-año |
N |
n |
Tasa de incidencia de HZ por 1.000 personas-año |
||
|
General (≥70)c |
8.250 |
25 |
0,8 |
8.346 |
284 |
9,3 |
91,3 (86,9, 94,5) |
|
70-79 |
6.468 |
19 |
0,8 |
6.554 |
216 |
8,9 |
91,3 (86,0, 94,9) |
|
≥80 |
1.782 |
6 |
1,0 |
1.792 |
68 |
11,1 |
91,4 (80,2, 96,9) |
Eficacia contra la neuralgia postherpética
Tabla 7 compara las tasas generales de PHN en los grupos de vacuna y placebo en ambos estudios.
| N = Número de sujetos incluidos en cada grupo; n = Número de sujetos que tienen al menos 1 PHN; CI = Intervalo de confianza. a Datos agrupados del estudio 1: NCT01165177 (sujetos ≥50 años) y estudio 2: NCT01165229 (sujetos ≥70 años). b mTVC = Cohorte total vacunada modificada definida como sujetos que recibieron 2 dosis (0 y 2 meses) de SHINGRIX o placebo y no desarrollaron un caso confirmado de HZ dentro de 1 mes después de la segunda dosis. c PHN = Neuralgia postherpética definida como dolor asociado a HZ calificado como 3 o mayor (en una escala de 0 a 10 puntos) que ocurre o persiste al menos 90 días después del inicio de la erupción utilizando el cuestionario Zoster Brief Pain Inventory. |
|||||||||||||||
|
Grupo de edad (Años) |
SHINGRIX |
Placebo |
% Eficacia (95% CI) |
||||||||||||
|
N |
n |
Tasa de incidencia de PHNc por 1.000 personas-año |
N |
n |
Tasa de incidencia de PHN por 1.000 personas-año |
||||||||||
|
General (≥70) |
8.250 |
4 |
0,1 |
8.346 |
36 |
1,2 |
88,8 (68,7, 97,1) |
||||||||
|
70-79 |
6.468 |
2 |
0,1 |
6.554 |
29 |
1,2 |
93,0 (72,5, 99,2) |
||||||||
|
≥80 |
1.782 |
2 |
0,3 |
1.792 |
7 |
1,1 |
71,2 (-51,5, 97,1) |
||||||||
El beneficio de SHINGRIX en la prevención de la NPH se puede atribuir al efecto de la vacuna en la prevención de la HZ. No se pudo demostrar la eficacia de SHINGRIX en la prevención de la NPH en sujetos con HZ confirmado.
14.4 Evaluación inmunológica para respaldar el régimen de dosificación
Se desconoce una medida de la respuesta inmunitaria que confiere protección contra la HZ. Los niveles de anticuerpos anti-gE se midieron mediante un ensayo inmunoabsorbente ligado a enzimas anti-gE (ELISA gE) y se utilizaron para respaldar el régimen de dosificación.
En un estudio clínico abierto, 238 sujetos de 50 años o más recibieron SHINGRIX en un régimen de 0 y 2 meses o de 0 y 6 meses. Se demostró la no inferioridad del régimen de 0 y 6 meses en comparación con el régimen de 0 y 2 meses en función de las GMC de ELISA gE 1 mes después de la segunda dosis.
14.5 Eficacia en adultos inmunocomprometidos de 18 años o más
La eficacia de SHINGRIX se evaluó en un estudio clínico de fase 3 aleatorizado, controlado con placebo y ciego para el observador en adultos inmunocomprometidos de ≥18 años que recibieron un auHSCT de 50 a 70 días antes de la dosis 1 y que se esperaba que recibieran terapia antiviral profiláctica durante ≤6 meses después del trasplante. La eficacia de SHINGRIX se calculó post hoc en otro estudio aleatorizado, controlado con placebo y ciego para el observador en sujetos con neoplasias hematológicas que recibieron la dosis 1 de SHINGRIX o placebo durante o dentro de los 6 meses posteriores a la finalización de la quimioterapia inmunosupresora. Cada uno de estos estudios se llevó a cabo en las siguientes regiones: América del Norte, América Latina, Europa, Asia, África (solo estudio auHSCT) y Australia/Nueva Zelanda.
Eficacia en sujetos de 18 años o más: receptores de auHSCT
En el estudio auHSCT, los sujetos fueron seguidos para el desarrollo de HZ y NPH durante una mediana de 21 meses (rango: 0 a 49,4 meses). Los casos sospechosos de HZ se siguieron prospectivamente para el desarrollo de NPH como en los estudios 1 y 2.
La población de análisis de eficacia primaria (mTVC) para el estudio auHSCT incluyó 1.721 sujetos que recibieron 2 dosis de SHINGRIX o placebo y no desarrollaron un caso confirmado de HZ dentro del mes posterior a la segunda dosis. Los casos confirmados de HZ se determinaron mediante PCR (83,7%) o mediante un Comité de Evaluación Clínica (16,3%).
Eficacia contra el herpes zóster: En comparación con el placebo, SHINGRIX redujo significativamente el riesgo de desarrollar HZ en receptores de auHSCT de 18 años o más (Tabla 8).
| auHSCT = Trasplante autólogo de células madre hematopoyéticas. N = Número de sujetos incluidos en cada grupo; n = Número de sujetos que tienen al menos 1 episodio confirmado de HZ; HZ = Herpes zóster; IC = Intervalo de confianza. a mTVC = Cohorte total vacunada modificada, definida como los sujetos que recibieron 2 dosis (0 y 1 a 2 meses) de SHINGRIX o placebo y no desarrollaron un caso confirmado de HZ dentro del mes posterior a la segunda dosis. El seguimiento se censuró en el momento del tratamiento para la recaída. b NCT01610414. c El criterio de valoración principal del estudio se basó en casos confirmados de HZ en sujetos de ≥18 años. |
||||||||
|
Estudios clínicos |
Grupo de edad (Años) |
SHINGRIX |
Placebo |
% Eficacia (IC del 95%) |
||||
|
N |
n |
Tasa de incidencia de HZ por 1.000 personas-año |
N |
n |
Tasa de incidencia de HZ por 1.000 personas-año |
|||
|
auHSCTb |
General (≥18)c |
870 |
49 |
30.0 |
851 |
135 |
94.3 |
68.2 (55.5, 77.6) |
|
18-49 |
213 |
9 |
21.5 |
212 |
29 |
76.0 |
71.8 (38.7, 88.3) |
|
|
≥50 |
657 |
40 |
33.0 |
639 |
106 |
100.9 |
67.3 (52.6, 77.9) |
|
Eficacia en sujetos de 18 años o más con enfermedades malignas hematológicas
En el estudio de enfermedades malignas hematológicas, la edad media fue de 57 años. La mayoría de los sujetos eran blancos (71%), seguidos de asiáticos (25%), negros (0,4%) y otros grupos raciales (4%); 5% eran de etnia hispana o latina estadounidense; y 41% eran mujeres. Los sujetos fueron seguidos para el desarrollo de HZ durante una mediana de 11,1 meses (rango: 0 a 15,6 meses). PHN no fue evaluado como un punto final del estudio.
En el estudio de malignidad hematológica, la población para el análisis de eficacia post hoc incluyó 515 sujetos que recibieron 2 dosis de SHINGRIX o placebo y no desarrollaron un caso confirmado de HZ dentro de 1 mes después de la segunda dosis. Los casos confirmados de HZ se determinaron ya sea por PCR (81,3%) o por un Comité de Evaluación Clínica (18,7%). El análisis post hoc mostró que SHINGRIX fue 87,2% (95% IC [44,2; 98,6]) efectiva contra el desarrollo de HZ. La tasa de incidencia de HZ por 1.000 personas-años fue de 8,5 frente a 66,2 en los grupos SHINGRIX y placebo, respectivamente.
Puntos finales de eficacia adicionales evaluados en el estudio auHSCT
Eficacia contra la neuralgia postherpética: En un análisis descriptivo, incluyendo todos los sujetos de 18 años o más en el mTVC, se informó 1 caso de PHN en el grupo de vacuna en comparación con 9 casos informados en el grupo de placebo. La eficacia de la vacuna contra PHN fue de 89,3% (95% IC: [22,5; 99,8]). El beneficio de SHINGRIX en la prevención de PHN puede atribuirse al efecto de la vacuna en la prevención de HZ.
Dolor asociado al herpes zoster: Los sujetos con sospecha de HZ calificaron su dolor asociado a HZ “más grave” en una escala de 10 puntos. Entre los sujetos con HZ confirmada, 37 de 49 sujetos (75,5%) que recibieron SHINGRIX y 120 de 135 sujetos (88,9%) que recibieron placebo calificaron su dolor asociado a HZ “más grave” como 3 o más. En este subconjunto de sujetos, la mediana de la duración del dolor asociado a HZ “más grave” fue de 14 y 24 días, entre los receptores de SHINGRIX y placebo, respectivamente.
14.6 Revacunación después de la vacunación con ZOSTAVAX (Vacuna viva contra el herpes zoster)
En un estudio clínico abierto (NCT02581410), sujetos de 65 años o más, que habían sido previamente vacunados con ZOSTAVAX más de 5 años antes del inicio del estudio (n = 215) o que nunca habían sido vacunados con ZOSTAVAX (n = 215), recibieron 1 dosis de SHINGRIX en los meses 0 y 2. Los sujetos que nunca habían sido vacunados con ZOSTAVAX fueron emparejados con aquellos que habían sido previamente vacunados con ZOSTAVAX de acuerdo con las variables predefinidas de edad (65 a 69, 70 a 79 y ≥80 años), sexo, raza / etnia y condición médica (enfermedades inmune-mediadas, diabetes mellitus, depresión, afecciones pulmonares o afecciones cardíacas). La edad media fue de 71 años; 51% eran mujeres. Todos los sujetos eran blancos y no eran hispanos o latinos.
La concentración de anticuerpos (Ab) anti-gE medida por ELISA 1 mes después de 2 dosis de SHINGRIX en sujetos que habían sido previamente vacunados con ZOSTAVAX no fue inferior a la de sujetos que nunca habían sido vacunados con ZOSTAVAX. El límite superior (UL) del intervalo de confianza (IC) del 95% fue 1.17 (criterio de éxito <1.5) para la razón de la concentración geométrica media (GMC) ajustada de Ab anti-gE entre sujetos que nunca habían sido vacunados con ZOSTAVAX y sujetos que habían sido previamente vacunados con ZOSTAVAX. No hubo evidencia de interferencia en la respuesta inmune a SHINGRIX en sujetos previamente vacunados con ZOSTAVAX.
14.7 Administración concomitante con otras vacunas
Administración concomitante con la vacuna contra la influenza
En un estudio clínico abierto (NCT01954251), sujetos de 50 años o más recibieron 1 dosis cada una de SHINGRIX y la vacuna cuadrivalente contra la influenza (FLUARIX QUADRIVALENT) en el mes 0 y 1 dosis de SHINGRIX en el mes 2 (n = 413), o 1 dosis de FLUARIX QUADRIVALENT en el mes 0 y 1 dosis de SHINGRIX en los meses 2 y 4 (n = 415). La edad media de la población fue de 63 años; 52% eran mujeres. La mayoría de los sujetos eran blancos (92%), seguidos de asiáticos (6%) y negros (2%); 0,4% eran de etnia hispana o latina estadounidense. No hubo evidencia de interferencia en la respuesta inmune a ninguno de los antígenos contenidos en SHINGRIX o la vacuna coadministrada.
Administración concomitante con PNEUMOVAX 23 (Vacuna polisacarídica neumocócica)
En un estudio clínico abierto (NCT02045836), sujetos de 50 años o más recibieron 1 dosis cada una de SHINGRIX y PNEUMOVAX 23 en el mes 0 y 1 dosis de SHINGRIX en el mes 2 (n = 432), o 1 dosis de PNEUMOVAX 23 en el mes 0 y 1 dosis de SHINGRIX en los meses 2 y 4 (n = 433). La edad media de la población fue de 63 años; 60% eran mujeres. La mayoría de los sujetos eran blancos (94%), seguidos de negros (2%), asiáticos (2%) y otros grupos raciales (2%); 1% era de etnia hispana o latina estadounidense.
La respuesta inmune a SHINGRIX, basada en Ab anti-gE, se midió por ELISA 1 mes después de la administración de la segunda dosis de SHINGRIX. Las respuestas inmunes a 12 de los 23 serotipos neumocócicos contenidos en PNEUMOVAX 23 se midieron por ensayo multiplex de opsonofagocitosis (MOPA) 1 mes después de la administración de la única dosis de PNEUMOVAX 23. No hubo evidencia de interferencia en la respuesta inmune al antígeno contenido en SHINGRIX o a los 12 antígenos evaluados contenidos en PNEUMOVAX 23 cuando las dos vacunas se administraron concomitantemente.
Administración concomitante con PREVNAR 13 (Vacuna conjugada neumocócica de 13 valentes [Proteína CRM197 del difteria])
En un estudio clínico abierto (NCT03439657), sujetos de 50 años o más recibieron 1 dosis cada una de SHINGRIX y PREVNAR 13 en el mes 0 y 1 dosis de SHINGRIX en el mes 2 (n = 449), o 1 dosis de PREVNAR 13 en el mes 0 y 1 dosis de SHINGRIX en los meses 2 y 4 (n = 463). La edad media de la población fue de 63 años; 60% eran mujeres. La mayoría de los sujetos eran blancos (98%), seguidos de negros (2%); 0,4% eran de etnia hispana o latina estadounidense.
La respuesta inmune a SHINGRIX, basada en Ab anti-gE, se midió por ELISA 1 mes después de la administración de la segunda dosis de SHINGRIX. Las respuestas inmunes a los serotipos neumocócicos contenidos en PREVNAR 13 se midieron por MOPA 1 mes después de la administración de la única dosis de PREVNAR 13. No hubo evidencia de interferencia en la respuesta inmune a los antígenos contenidos en SHINGRIX o PREVNAR 13 cuando las dos vacunas se administraron concomitantemente.
Administración concomitante con BOOSTRIX (Vacuna de toxoide tetánico, toxoide diftérico reducido y pertusis acelular, adsorbida)
En un estudio clínico de etiqueta abierta (NCT02052596), los sujetos de 50 años o más recibieron 1 dosis cada una de SHINGRIX y BOOSTRIX en el Mes 0 y 1 dosis de SHINGRIX en el Mes 2 (n = 412; grupo de administración concomitante), o 1 dosis de BOOSTRIX en el Mes 0 y 1 dosis de SHINGRIX en los Meses 2 y 4 (n = 418; grupo de administración secuencial). La edad media de la población fue de 63 años; el 54% eran mujeres. La mayoría de los sujetos eran blancos (87%), seguidos por negros (11%) y otros grupos raciales; el 2% eran de etnia hispanoamericana o latina.
La respuesta inmune a SHINGRIX, basada en el Ab anti-gE, se midió por ELISA 1 mes después de la administración de la segunda dosis de SHINGRIX. La respuesta inmune a BOOSTRIX (anti-D, anti-T y anticuerpos contra antígenos de la tos ferina) se midió 1 mes después de la administración de la dosis única de BOOSTRIX. La administración concomitante no mostró evidencia de interferencia en la respuesta inmune al antígeno contenido en SHINGRIX o los antígenos contenidos en BOOSTRIX, con la excepción de uno de los antígenos de la tos ferina (pertactina), que no cumplió el criterio de no inferioridad: el límite superior (UL) del 95% del CI para la relación GMC ajustada (grupo de administración secuencial/grupo de administración concomitante) para el anticuerpo antipertactina fue de 1.58 (criterio de no inferioridad <1.5). El significado clínico de la respuesta inmune reducida a la pertactina se desconoce.
16 FORMA DE SUMINISTRO/ALMACENAMIENTO Y MANIPULACIÓN
SHINGRIX se suministra como 2 componentes: un vial de dosis única de componente de antígeno gE liofilizado (polvo) y un vial de dosis única de componente de suspensión de adyuvante (líquido) (envasado sin jeringas ni agujas).
|
Presentación |
Número de NDC del cartón |
Componentes |
|
|
Componente de suspensión de adyuvante (líquido) |
Componente de antígeno gE liofilizado (polvo) |
||
|
Un cartón exterior de 1 dosis |
58160-819-12 |
Vial 1 de 2 NDC 58160-829-01 |
Vial 2 de 2 NDC 58160-828-01 |
|
Un cartón exterior de 10 dosis |
58160-823-11 |
10 viales NDC 58160-829-03 |
10 viales NDC 58160-828-03 |
16.1 Almacenamiento antes de la reconstitución
Viales de componente de suspensión de adyuvante: Almacenar refrigerado entre 2° y 8°C (36° y 46°F). Proteger los viales de la luz. No congelar. Desechar si la suspensión de adyuvante se ha congelado.
Viales de componente de antígeno gE liofilizado: Almacenar refrigerado entre 2° y 8°C (36° y 46°F). Proteger los viales de la luz. No congelar. Desechar si el componente de antígeno se ha congelado.
16.2 Almacenamiento después de la reconstitución
- •
- Administrar inmediatamente o almacenar refrigerado entre 2° y 8°C (36° y 46°F) hasta por 6 horas antes de su uso.
- •
- Desechar la vacuna reconstituida si no se usa dentro de las 6 horas.
- •
- No congelar. Desechar si la vacuna se ha congelado.
17 INFORMACIÓN PARA EL PACIENTE
- •
- Informe a los pacientes sobre los posibles beneficios y riesgos de la inmunización con SHINGRIX y sobre la importancia de completar la serie de inmunización de 2 dosis según el calendario.
- •
- Informe a los pacientes sobre la posibilidad de reacciones adversas que se han asociado temporalmente con la administración de SHINGRIX.
- •
- Proporcione las Declaraciones de información sobre vacunas, que están disponibles de forma gratuita en el sitio web de los Centros para el Control y la Prevención de Enfermedades (CDC) (www.cdc.gov/vaccines).
SECCIÓN NO CLASIFICADA SPL
BOOSTRIX y FLUARIX QUADRIVALENT son marcas comerciales propiedad de o con licencia del grupo de empresas GSK. Las otras marcas enumeradas son marcas comerciales propiedad de o con licencia de sus propietarios y no son propiedad de o con licencia del grupo de empresas GSK. Los fabricantes de estas marcas no están afiliados a ni respaldan al grupo de empresas GSK o sus productos.
Fabricado por GlaxoSmithKline Biologicals
Rixensart, Bélgica, Licencia de EE. UU. 1617, y
Distribuido por GlaxoSmithKline
Durham, NC 27701
©2023 Grupo de empresas GSK o su licenciante.
SHX:7PI
PANEL DE VISUALIZACIÓN PRINCIPAL
PANEL PRINCIPAL DE VISUALIZACIÓN
NDC 58160-819-12
SHINGRIX
Vacuna Recombinante contra el Herpes Zóster, Adyuvada
Rx solamente
AVISO: Un vial de polvo liofilizado y un vial de suspensión líquida DEBEN COMBINARSE ANTES DE USAR
Para personas de 50 años o más y para personas de 18 años o más que están inmunocomprometidas y tienen un riesgo aumentado de Herpes Zóster
Contenido (una dosis única de SHINGRIX):
1 Vial que contiene el componente de antígeno gE liofilizado
1 Vial que contiene el componente de suspensión adyuvante
Después de la reconstitución, una dosis única de SHINGRIX es de 0.5 mL
GSK
SHINGRIX
Antígeno y Adyuvante Fabricado en Bélgica
©2021 GSK group of companies or its licensor.
- Rev. 7/23
- 515720
PANEL DE VISUALIZACIÓN PRINCIPAL
Etiqueta de vial de adyuvante de un cuenta
NDC 58160-829-01
- 496837 Rev. 2/19
PANEL DE VISUALIZACIÓN PRINCIPAL
Etiqueta del Vial de Antígeno de una Dosis
NDC 58160-828-01
- 496835 Rev. 2/19
PANEL DE VISUALIZACIÓN PRINCIPAL
PANEL PRINCIPAL DE VISUALIZACIÓN
NDC 58160-823-11
SHINGRIX
Vacuna Recombinante contra el Herpes Zoster, Adyuvada
Rx solamente
AVISO: Un vial de polvo liofilizado y un vial de suspensión líquida DEBEN COMBINARSE ANTES DE USAR
Para personas de 50 años o más y para personas de 18 años o más que están inmunocomprometidas y tienen un mayor riesgo de Herpes Zoster
Contenido (10 dosis de SHINGRIX):
10 Viales que contienen el componente de antígeno gE liofilizado
10 Viales que contienen el componente de suspensión adyuvante
Después de la reconstitución, una sola dosis de SHINGRIX es de 0.5 mL
GSK
SHINGRIX
Antígeno y Adyuvante Fabricado en Bélgica
©2023 GSK group of companies or its licensor.
- Rev. 8/23
- 515300
PANEL DE VISUALIZACIÓN PRINCIPAL
Etiqueta del frasco de adyuvante de 10 dosis
NDC 58160-829-03
- 490658 Rev. 10/17
PANEL DE VISUALIZACIÓN PRINCIPAL
Etiqueta del vial de antígeno de 10 unidades
NDC 58160-828-03
- 490735 Rev. 10/17