Fabricante de medicamentos: Waylis Therapeutics LLC (Updated: 2025-01-08)
ADVERTENCIA EN EL RECUADRO
ADVERTENCIA
LEUKERAN (clorambucilo) puede suprimir severamente la función de la médula ósea. El clorambucilo es un carcinógeno en humanos. El clorambucilo es probablemente mutágeno y teratógeno en humanos. El clorambucilo produce infertilidad humana (ver ADVERTENCIAS y PRECAUCIONES).
DESCRIPCIÓN
LEUKERAN (clorambucil) fue sintetizado por primera vez por Everett et al. Es un agente alquilante bifuncional del tipo mostaza nitrogenada que ha demostrado actividad contra enfermedades neoplásicas humanas seleccionadas.
El clorambucil se conoce químicamente como ácido 4-[bis(2-cloroetil)amino]bencenobutanoico y tiene la siguiente fórmula estructural:
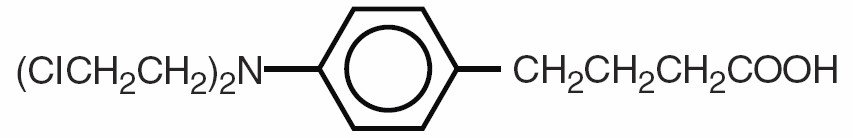
El clorambucil se hidroliza en agua y tiene un pKa de 5.8.
LEUKERAN (clorambucil) está disponible en forma de comprimidos para administración oral. Cada comprimido recubierto con película contiene 2 mg de clorambucil y los excipientes dióxido de silicio coloidal, hipromelosa, lactosa (anhidra), macrogol/PEG 400, celulosa microcristalina, óxido de hierro rojo, ácido esteárico, dióxido de titanio y óxido de hierro amarillo.
Farmacología Clínica
Mecanismo de acción
Chlorambucil, un derivado de la mostaza nitrogenada aromática, es un agente alquilante. El Chlorambucil interfiere con la replicación del ADN e induce la apoptosis celular a través de la acumulación de p53 citosólica y la posterior activación de Bax, un promotor de la apoptosis.
FARMACOCINÉTICA
En un estudio de 12 pacientes que recibieron dosis orales únicas de 0.2 mg/kg de LEUKERAN, la Cmáx plasmática media de chlorambucil ajustada a la dosis (±DE) fue de 492 ± 160 ng/mL, el AUC fue de 883 ± 329 ng.h/mL, la vida media de eliminación media (t½) fue de 1.3 ± 0.5 horas y la Tmáx fue de 0.83 ± 0.53 horas. Para el metabolito principal, mostaza del ácido fenilacético (PAAM), la Cmáx plasmática media ajustada a la dosis (± DE) fue de 306 ± 73 ng/mL, el AUC fue de 1204 ± 285 ng.h/mL, la t½ media fue de 1.8 ± 0.4 horas y la Tmáx fue de 1.9 ± 0.7 horas.
Después de dosis orales únicas de 0.6 a 1.2 mg/kg, los niveles plasmáticos máximos de chlorambucil (Cmáx) se alcanzan en 1 hora y la vida media de eliminación terminal (t½) del fármaco original se estima en 1.5 horas.
Absorción: El Chlorambucil se absorbe rápida y completamente (>70%) del tracto gastrointestinal. De acuerdo con la absorción rápida y predecible de chlorambucil, se ha demostrado que la variabilidad interindividual en la farmacocinética plasmática de chlorambucil es relativamente pequeña después de dosis orales de entre 15 y 70 mg (variabilidad intrapaciente de 2 veces y una variabilidad interpaciente de 2 a 4 veces en el AUC). La absorción de chlorambucil se reduce cuando se toma después de los alimentos. En un estudio de diez pacientes, la ingesta de alimentos aumentó la Tmáx media en 2 veces y redujo los valores de Cmáx y AUC ajustados a la dosis en un 55% y un 20%, respectivamente.
Distribución: El volumen aparente de distribución promedio fue de 0.31 L/kg después de una dosis oral única de 0.2 mg/kg de chlorambucil en 11 pacientes con cáncer con leucemia linfocítica crónica. El Chlorambucil y sus metabolitos se unen ampliamente a las proteínas plasmáticas y tisulares. In vitro, el chlorambucil se une en un 99% a las proteínas plasmáticas, específicamente a la albúmina. No se han determinado los niveles de chlorambucil en el líquido cefalorraquídeo.
Metabolismo: El Chlorambucil se metaboliza ampliamente en el hígado, principalmente a mostaza del ácido fenilacético, que tiene actividad antineoplásica. El Chlorambucil y su principal metabolito sufren degradación oxidativa a derivados monohidroxi y dihidroxi.
Excreción: Después de una dosis única de chlorambucil radiomarcado (14C), aproximadamente del 20% al 60% de la radiactividad aparece en la orina después de 24 horas. Nuevamente, menos del 1% de la radiactividad urinaria está en forma de chlorambucil o mostaza del ácido fenilacético.
INDICACIONES Y USO
LEUKERAN (clorambucilo) está indicado en el tratamiento de la leucemia linfática crónica (linfocítica), linfomas malignos incluyendo el linfosarcoma, linfoma folicular gigante y la enfermedad de Hodgkin. No es curativo en ninguno de estos trastornos, pero puede producir una paliación clínicamente útil.
CONTRAINDICACIONES
Chlorambucil no debe usarse en pacientes cuya enfermedad ha demostrado una resistencia previa al agente. Los pacientes que han demostrado hipersensibilidad a chlorambucil no deben recibir el medicamento.
Puede haber hipersensibilidad cruzada (erupción cutánea) entre chlorambucil y otros agentes alquilantes.
ADVERTENCIAS
Debido a sus propiedades carcinogénicas, el clorambucil no debe administrarse a pacientes con afecciones distintas a la leucemia linfática crónica o los linfomas malignos. Se han observado convulsiones, infertilidad, leucemia y neoplasias malignas secundarias cuando se empleó clorambucil en el tratamiento de enfermedades malignas y no malignas.
Existen numerosos informes de leucemia aguda que surge en pacientes con enfermedades malignas y no malignas después del tratamiento con clorambucil. En muchos casos, estos pacientes también recibieron otros agentes quimioterapéuticos o alguna forma de radioterapia. No es posible cuantificar el riesgo de inducción de leucemia o carcinoma por clorambucil en humanos. La evaluación de los informes publicados sobre la aparición de leucemia en pacientes que han recibido clorambucil (y otros agentes alquilantes) sugiere que el riesgo de leucemogénesis aumenta con la cronicidad del tratamiento y las dosis acumulativas elevadas. Sin embargo, ha resultado imposible definir una dosis acumulativa por debajo de la cual no exista riesgo de inducción de neoplasia maligna secundaria. Los beneficios potenciales de la terapia con clorambucil deben sopesarse individualmente frente al posible riesgo de inducción de una neoplasia maligna secundaria.
Se ha demostrado que el clorambucil causa daño cromosómico o cromátide en humanos. Se ha observado esterilidad tanto reversible como permanente en ambos sexos que recibieron clorambucil.
Se ha documentado una alta incidencia de esterilidad cuando se administra clorambucil a varones prepuberales y puberales. También se ha observado azoospermia prolongada o permanente en varones adultos. Si bien la mayoría de los informes de disfunción gonadal secundaria al clorambucil se han relacionado con varones, la inducción de amenorrea en mujeres con agentes alquilantes está bien documentada y el clorambucil puede producir amenorrea. Los estudios de autopsia de los ovarios de mujeres con linfoma maligno tratadas con quimioterapia combinada que incluye clorambucil han mostrado diversos grados de fibrosis, vasculitis y depleción de folículos primordiales.
Se han notificado casos raros de erupción cutánea que progresa a eritema multiforme, necrolisis epidérmica tóxica o síndrome de Stevens-Johnson. El clorambucil debe suspenderse inmediatamente en pacientes que desarrollan reacciones cutáneas.
Embarazo
El clorambucil puede causar daño fetal cuando se administra a una mujer embarazada. Se ha observado agenesia renal unilateral en 2 descendientes cuyas madres recibieron clorambucil durante el primer trimestre. Se encontraron malformaciones urogenitales, incluida la ausencia de un riñón, en fetos de ratas a las que se administró clorambucil. No hay estudios adecuados y bien controlados en mujeres embarazadas. Si se utiliza este medicamento durante el embarazo, o si la paciente queda embarazada mientras toma este medicamento, se debe informar a la paciente sobre el posible peligro para el feto. Se debe aconsejar a las mujeres en edad fértil que eviten quedar embarazadas.
Precauciones
Generalidades
Muchos pacientes desarrollan una linfopenia de progresión lenta durante el tratamiento. El recuento de linfocitos generalmente vuelve rápidamente a los niveles normales al finalizar la terapia con fármacos. La mayoría de los pacientes presentan algo de neutropenia después de la tercera semana de tratamiento y esto puede continuar hasta 10 días después de la última dosis. Posteriormente, el recuento de neutrófilos generalmente vuelve rápidamente a la normalidad. La neutropenia severa parece estar relacionada con la dosis y generalmente ocurre solo en pacientes que han recibido una dosis total de 6,5 mg/kg o más en un curso de terapia con dosificación continua. Se puede esperar que alrededor de un cuarto de todos los pacientes que reciben el esquema de dosis continua y un tercio de aquellos que reciben esta dosis en 8 semanas o menos desarrollen neutropenia severa.
Aunque no es necesario suspender el clorambucilo al primer indicio de una disminución en el recuento de neutrófilos, se debe recordar que la disminución puede continuar durante 10 días después de la última dosis y que a medida que la dosis total se acerca a 6,5 mg/kg, existe el riesgo de causar daño irreversible en la médula ósea. La dosis de clorambucilo debe disminuirse si los recuentos de leucocitos o plaquetas caen por debajo de los valores normales y debe suspenderse en caso de depresión más severa.
El clorambucilo no debe administrarse a dosis completas antes de 4 semanas después de un curso completo de radioterapia o quimioterapia debido a la vulnerabilidad de la médula ósea al daño en estas condiciones. Si los recuentos de leucocitos o plaquetas antes del tratamiento están deprimidos debido a un proceso de enfermedad de la médula ósea antes de iniciar el tratamiento, el tratamiento debe iniciarse con una dosis reducida.
RecuentosPersistentemente bajos de neutrófilos y plaquetas o linfocitosis periférica sugieren infiltración de la médula ósea. Si se confirma mediante examen de la médula ósea, la dosis diaria de clorambucilo no debe exceder 0,1 mg/kg. El clorambucilo parece estar relativamente libre de efectos secundarios gastrointestinales u otra evidencia de toxicidad aparte de la acción depresora de la médula ósea. En humanos, dosis orales únicas de 20 mg o más pueden producir náuseas y vómitos.
Los niños con síndrome nefrótico y los pacientes que reciben dosis altas en pulsos de clorambucilo pueden tener un mayor riesgo de convulsiones. Al igual que con cualquier fármaco potencialmente epileptógeno, se debe tener precaución al administrar clorambucilo a pacientes con antecedentes de trastorno convulsivo o trauma craneal, o que están recibiendo otros fármacos potencialmente epileptógenos.
Se debe evitar la administración de vacunas vivas a pacientes inmunocomprometidos.
INFORMACIÓN PARA PACIENTES
Los pacientes deben ser informados de que las toxicidades principales del clorambucilo están relacionadas con hipersensibilidad, fiebre por medicamento, mielosupresión, hepatotoxicidad, infertilidad, convulsiones, toxicidad gastrointestinal y neoplasias secundarias. Los pacientes nunca deben tomar el fármaco sin supervisión médica y deben consultar a su médico si experimentan erupción cutánea, sangrado, fiebre, ictericia, tos persistente, convulsiones, náuseas, vómitos, amenorrea o bultos/masas inusuales. Las mujeres en edad fértil deben ser aconsejadas para evitar quedar embarazadas.
Pruebas de Laboratorio
Los pacientes deben ser seguidos cuidadosamente para evitar daños peligrosos para la vida en la médula ósea durante el tratamiento. Se debe realizar un examen semanal de la sangre para determinar los niveles de hemoglobina, el recuento total y diferencial de leucocitos y el recuento cuantitativo de plaquetas. Además, durante las primeras 3 a 6 semanas de tratamiento, se recomienda que se realicen recuentos de glóbulos blancos 3 o 4 días después de cada recuento completo de sangre semanal. Galton et al han sugerido que al seguir a los pacientes es útil trazar los recuentos de sangre en un gráfico al mismo tiempo que se registra el peso corporal, la temperatura, el tamaño del bazo, etc. Se considera peligroso permitir que un paciente pase más de 2 semanas sin examen hematológico y clínico durante el tratamiento.
Carcinogénesis, Mutagénesis, Disminución de la Fertilidad
Consulte la sección ADVERTENCIAS para obtener información sobre carcinogénesis, mutagénesis y disminución de la fertilidad.
Lactancia
No se sabe si este fármaco se excreta en la leche humana. Debido a que muchos fármacos se excretan en la leche humana y debido al potencial de reacciones adversas graves en los lactantes amamantados por el clorambucilo, se debe decidir si suspender la lactancia o el fármaco, teniendo en cuenta la importancia del fármaco para la madre.
Uso en Ancianos
Los estudios clínicos de clorambucilo no incluyeron un número suficiente de sujetos de 65 años o más para determinar si responden de manera diferente a los sujetos más jóvenes. Otra experiencia clínica reportada no ha identificado diferencias en las respuestas entre los pacientes ancianos y los más jóvenes. En general, la selección de la dosis para un paciente anciano debe ser cautelosa, generalmente comenzando en el extremo inferior del rango de dosificación, reflejando la mayor frecuencia de disminución de la función hepática, renal o cardíaca, y de enfermedades concomitantes u otra terapia farmacológica.
Uso en Pacientes con Insuficiencia Renal: No se ha estudiado formalmente el impacto de la insuficiencia renal en la eliminación de clorambucilo. La eliminación renal de clorambucilo sin cambios y sus metabolitos activos principales, el ácido fenilacético mostaza, representa menos del 1% de la dosis administrada. Además, no se requirió un ajuste de dosis en 2 pacientes en diálisis que recibían clorambucilo. Por lo tanto, no se espera que la insuficiencia renal tenga un impacto significativo en la eliminación de clorambucilo.
Uso en Pacientes con Insuficiencia Hepática: No se han realizado estudios formales en pacientes con insuficiencia hepática. Como el clorambucilo se metaboliza principalmente en el hígado, los pacientes con insuficiencia hepática deben ser monitoreados estrechamente por toxicidad y se puede considerar una reducción de la dosis en pacientes con insuficiencia hepática cuando se tratan con LEUKERAN (consulte DOSIFICACIÓN Y ADMINISTRACIÓN).
REACCIONES ADVERSAS
Para notificar REACCIONES ADVERSAS SOSPECHOSAS, comuníquese con Waylis Therapeutics LLC sin cargo al 1-888-514-4727 o con la FDA al 1-800-FDA-1088 o www.fda.gov/medwatch.
Hematologías
El efecto secundario más común es la supresión de la médula ósea, anemia, leucopenia, neutropenia, trombocitopenia o pancitopenia. Aunque la supresión de la médula ósea ocurre con frecuencia, generalmente es reversible si el clorambucil se retira lo suficientemente temprano. Sin embargo, se ha informado de insuficiencia irreversible de la médula ósea.
Gastrointestinales
Los trastornos gastrointestinales como náuseas y vómitos, diarrea y ulceración oral ocurren con poca frecuencia.
SNC
Temblores, contracciones musculares, mioclonía, confusión, agitación, ataxia, paresia flácida y alucinaciones se han reportado como experiencias adversas raras al clorambucil que se resuelven al suspender el medicamento. Se ha informado que ocurren convulsiones focales y/o generalizadas raras tanto en niños como en adultos con dosis diarias terapéuticas y regímenes de dosificación en pulsos, y en sobredosis aguda (ver PRECAUCIONES: Generales).
Dermatológicas
Se han reportado reacciones alérgicas como urticaria y edema angioneurótico después de la dosis inicial o subsecuente. Se ha reportado hipersensibilidad cutánea (incluidos informes raros de erupción cutánea que progresa a eritema multiforme, necrolisis epidérmica tóxica y síndrome de Stevens-Johnson) (ver ADVERTENCIAS).
Misceláneas
Otras reacciones adversas reportadas incluyen: fibrosis pulmonar, hepatotoxicidad e ictericia, fiebre medicamentosa, neuropatía periférica, neumonía intersticial, cistitis estéril, infertilidad, leucemia y neoplasias secundarias (ver ADVERTENCIAS).
Sobredosis
La pancitopenia reversible fue el principal hallazgo en sobredosis involuntarias de clorambucil.
También se ha producido toxicidad neurológica que va desde comportamiento agitado y ataxia hasta convulsiones múltiples de gran mal. Como no existe antídoto conocido, se debe controlar estrechamente el hemograma y deben instituirse medidas de apoyo generales, junto con transfusiones sanguíneas apropiadas, si es necesario. El clorambucil no es dializable.
Las dosis únicas orales LD50 en ratones son de 123 mg/kg. En ratas, una dosis intraperitoneal única de 12,5 mg/kg de clorambucil produce efectos típicos de mostaza nitrogenada; estos incluyen atrofia de la membrana mucosa intestinal y los tejidos linfoides, linfopenia grave que alcanza su máximo en 4 días, anemia y trombocitopenia. Después de esta dosis, los animales comienzan a recuperarse en 3 días y parecen normales en aproximadamente una semana, aunque la médula ósea puede no volverse completamente normal durante aproximadamente 3 semanas. Una dosis intraperitoneal de 18,5 mg/kg mata aproximadamente al 50% de las ratas con desarrollo de convulsiones. Se han administrado hasta 50 mg/kg por vía oral a ratas como dosis única, con recuperación. Tal dosis causa bradicardia, salivación excesiva, hematuria, convulsiones y disfunción respiratoria.
DOSIFICACIÓN Y ADMINISTRACIÓN
La dosis oral habitual es de 0,1 a 0,2 mg/kg de peso corporal al día durante 3 a 6 semanas según sea necesario. Esto suele equivaler a 4 a 10 mg por día para el paciente promedio. Toda la dosis diaria puede administrarse de una sola vez. Estas dosis son para iniciar el tratamiento o para tratamientos cortos. La dosis debe ajustarse cuidadosamente según la respuesta del paciente y debe reducirse tan pronto como haya una caída brusca en el recuento de glóbulos blancos. Los pacientes con enfermedad de Hodgkin suelen requerir 0,2 mg/kg al día, mientras que los pacientes con otros linfomas o leucemia linfocítica crónica suelen requerir solo 0,1 mg/kg al día. Cuando hay infiltración linfocítica de la médula ósea, o cuando la médula ósea es hipoplásica, la dosis diaria no debe exceder de 0,1 mg/kg (aproximadamente 6 mg para el paciente promedio). Se han notificado programas alternativos para el tratamiento de la leucemia linfocítica crónica que emplean dosis pulsátiles intermitentes, bisemanales o mensuales de clorambucilo. Los programas intermitentes de clorambucilo comienzan con una dosis única inicial de 0,4 mg/kg. Las dosis generalmente aumentan en 0,1 mg/kg hasta que se observa el control de la linfocitosis o la toxicidad. Las dosis posteriores se modifican para producir una toxicidad hematológica leve. Se considera que la tasa de respuesta de la leucemia linfocítica crónica al programa bisemanal o mensual de administración de clorambucilo es similar o mejor a la notificada previamente con la administración diaria y que la toxicidad hematológica fue menor o igual a la encontrada en estudios que utilizaron clorambucilo diario.
La radiación y los fármacos citotóxicos hacen que la médula ósea sea más vulnerable al daño, y el clorambucilo debe usarse con especial precaución dentro de las 4 semanas posteriores a un tratamiento completo de radioterapia o quimioterapia. Sin embargo, las dosis pequeñas de radiación paliativa sobre focos aislados alejados de la médula ósea generalmente no deprimirán el recuento de neutrófilos y plaquetas. En estos casos, el clorambucilo puede administrarse en la dosis habitual.
Actualmente se considera que los tratamientos cortos son más seguros que la terapia de mantenimiento continuo, aunque ambos métodos han sido efectivos. Debe reconocerse que la terapia continua puede dar la apariencia de “mantenimiento” en pacientes que están en realidad en remisión y no tienen necesidad inmediata de más fármacos. Si se utiliza una dosis de mantenimiento, no debe exceder de 0,1 mg/kg al día y bien puede ser tan baja como 0,03 mg/kg al día. Una dosis de mantenimiento típica es de 2 mg a 4 mg al día, o menos, dependiendo del estado de los recuentos sanguíneos. Por lo tanto, puede ser deseable retirar el fármaco después de haber logrado el control máximo, ya que la terapia intermitente reinstaurada en el momento de la recaída puede ser tan eficaz como el tratamiento continuo.
Deben utilizarse los procedimientos adecuados para la manipulación y eliminación de fármacos anticancerígenos. Se han publicado varias directrices sobre este tema.1-4 No existe un acuerdo general sobre si todos los procedimientos recomendados en las directrices son necesarios o apropiados.
POBLACIONES ESPECIALES
Insuficiencia hepática: Los pacientes con insuficiencia hepática deben ser controlados estrechamente para detectar toxicidad. Dado que el clorambucilo se metaboliza principalmente en el hígado, puede considerarse una reducción de la dosis en pacientes con insuficiencia hepática cuando se trata con LEUKERAN. Sin embargo, no hay datos suficientes en pacientes con insuficiencia hepática para proporcionar una recomendación de dosificación específica.
Presentación
LEUKERAN se suministra como comprimidos redondos, biconvexos, recubiertos con película marrón, que contienen 2 mg de clorambucil en frascos de vidrio ámbar con cierre a prueba de niños. Un lado está grabado con “GX EG3” y el otro lado con una “L.”
Frasco de 25 (NDC 80725-610-25)
Conservar en nevera, entre 2° y 8°C.
REFERENCIAS
1. Alerta del NIOSH: Prevención de exposiciones ocupacionales a fármacos antineoplásicos y otros fármacos peligrosos en entornos de atención médica. 2004. Departamento de Salud y Servicios Humanos de EE. UU., Servicio de Salud Pública, Centros para el Control y la Prevención de Enfermedades, Instituto Nacional de Seguridad y Salud Ocupacional, Publicación DHHS (NIOSH) No. 2004-165.
2. Manual técnico de OSHA, TED 1-0.15A, Sección VI: Capítulo 2. Control de la exposición ocupacional a fármacos peligrosos. OSHA, 1999. http://www.osha.gov/dts/osta/otm/otm_vi/otm_vi_2.html
3. Sociedad Estadounidense de Farmacéuticos de Sistemas de Salud. Pautas de la ASHP sobre el manejo de fármacos peligrosos. Am J Health-Syst Pharm. (2006) 63:1172-1193.
4. Polovich, M., White, J. M., & Kelleher, L.O. (eds.) 2005. Pautas y recomendaciones de quimioterapia y bioterapia para la práctica (2.ª ed.) Pittsburgh, PA: Oncology Nursing Society.
SECCIÓN NO CLASIFICADA SPL

Distribuido por: Waylis Therapeutics LLC
Wixom, MI 48393
Hecho en Alemania
Rev. 02/2023
ETIQUETA PRINCIPAL DEL ENVASE
Panel principal de visualización
NDC 80725-610-25
LEUKERAN®
(clorambucil) Comprimidos
2 mg
25 Comprimidos
Cada comprimido contiene 2 mg de clorambucil.
Receta médica únicamente.

Caja de Leukeran 2 mg, 25 unidades.

Etiqueta de Leukeran 2 mg, 25 unidades.

