Fabricante de medicamentos: Pfizer Laboratories Div Pfizer Inc (Updated: 2024-12-27)
ASPECTOS DESTACADOS DE LA INFORMACIÓN DE PRESCRIPCIÓN
IBRANCE® (palbociclib) cápsulas, para administración oral
Aprobación inicial en EE. UU.: 2015
INDICACIONES Y USO
IBRANCE es un inhibidor de cinasa indicado para el tratamiento de pacientes adultas con cáncer de mama avanzado o metastásico, receptor de hormonas (RH)-positivo y receptor 2 del factor de crecimiento epidérmico humano (HER2)-negativo, en combinación con:
POSOLOGÍA Y ADMINISTRACIÓN
Las cápsulas de IBRANCE se toman por vía oral con alimentos en combinación con un inhibidor de la aromatasa o fulvestrant. (2)
PRESENTACIONES Y CONCENTRACIONES
Cápsulas: 125 mg, 100 mg y 75 mg. (3)
CONTRAINDICACIONES
Ninguna. (4)
ADVERTENCIAS Y PRECAUCIONES
- •
- Neutropenia: Controle el hemograma completo antes de comenzar el tratamiento con IBRANCE y al comienzo de cada ciclo, así como el día 15 de los dos primeros ciclos, y según esté clínicamente indicado. (2.2, 5.1)
- •
- Enfermedad pulmonar intersticial (EPI)/Neumonitis: Se han notificado casos graves y mortales de EPI/neumonitis. Controle los síntomas pulmonares de EPI/neumonitis. Interrumpa inmediatamente IBRANCE en pacientes con sospecha de EPI/neumonitis. Suspenda permanentemente IBRANCE si se produce una EPI/neumonitis grave. (5.2)
- •
- Toxicidad embriofetal: IBRANCE puede causar daño fetal. Avise a las pacientes del riesgo potencial para un feto y del uso de métodos anticonceptivos eficaces. (5.3, 8.1, 8.3)
REACCIONES ADVERSAS
Las reacciones adversas más frecuentes (incidencia ≥10%) fueron neutropenia, infecciones, leucopenia, fatiga, náuseas, estomatitis, anemia, alopecia, diarrea, trombocitopenia, erupción cutánea, vómitos, disminución del apetito, astenia y pirexia. (6)
Para notificar SOSPECHAS DE REACCIONES ADVERSAS, póngase en contacto con Pfizer Inc. al 1-800-438-1985 o con la FDA al 1-800-FDA-1088 o www.fda.gov/medwatch.
INTERACCIONES MEDICAMENTOSAS
- •
- Inhibidores de CYP3A: Evite el uso concomitante de IBRANCE con inhibidores potentes de CYP3A. Si no se puede evitar el inhibidor potente, reduzca la dosis de IBRANCE. (2.2, 7.1)
- •
- Inductores de CYP3A: Evite el uso concomitante de IBRANCE con inductores potentes de CYP3A. (7.2)
- •
- Sustratos de CYP3A: Puede ser necesario reducir la dosis de sustratos sensibles de CYP3A4 con índices terapéuticos estrechos cuando se administran de forma concomitante con IBRANCE. (7.3)
Ver 17 para obtener INFORMACIÓN PARA EL PACIENTE y el etiquetado del paciente aprobado por la FDA.
Revisado: 12/2024
Tabla de contenido
INFORMACIÓN COMPLETA DE PRESCRIPCIÓN: CONTENIDO*
1 INDICACIONES Y USO
2 DOSIFICACIÓN Y ADMINISTRACIÓN
2.1 Dosis y régimen recomendados
2.2 Modificación de la dosis
3 FORMAS Y CONCENTRACIONES FARMACÉUTICAS
4 CONTRAINDICACIONES
5 ADVERTENCIAS Y PRECAUCIONES
5.1 Neutropenia
5.2 Enfermedad pulmonar intersticial (EPI)/Neumonitis
5.3 Toxicidad embriofetal
6 REACCIONES ADVERSAS
6.1 Experiencia en estudios clínicos
6.2 Experiencia postcomercialización
7 INTERACCIONES MEDICAMENTOSAS
7.1 Agentes que pueden aumentar las concentraciones plasmáticas de palbociclib
7.2 Agentes que pueden disminuir las concentraciones plasmáticas de palbociclib
7.3 Fármacos cuyas concentraciones plasmáticas pueden verse alteradas por palbociclib
8 USO EN POBLACIONES ESPECÍFICAS
8.1 Embarazo
8.2 Lactancia
8.3 Mujeres y hombres en edad fértil
8.4 Uso pediátrico
8.5 Uso geriátrico
8.6 Insuficiencia hepática
8.7 Insuficiencia renal
10 SOBREDOSIFICACIÓN
11 DESCRIPCIÓN
12 FARMACOLOGÍA CLÍNICA
12.1 Mecanismo de acción
12.2 Farmacodinamia
12.3 Farmacocinética
13 TOXICOLOGÍA NO CLÍNICA
13.1 Carcinogénesis, mutagénesis, deterioro de la fertilidad
14 ESTUDIOS CLÍNICOS
16 PRESENTACIÓN/ALMACENAMIENTO Y MANIPULACIÓN
17 INFORMACIÓN PARA EL PACIENTE
- *
- Las secciones o subsecciones omitidas de la información completa de prescripción no se enumeran.
1 INDICACIONES Y USO
IBRANCE está indicado para el tratamiento de pacientes adultas con cáncer de mama avanzado o metastásico, receptor hormonal (RH)-positivo y receptor 2 del factor de crecimiento epidérmico humano (HER2)-negativo, en combinación con:
- •
- un inhibidor de la aromatasa como terapia endocrina inicial; o
- •
- fulvestrant en pacientes con progresión de la enfermedad tras terapia endocrina.
2 DOSIS Y ADMINISTRACIÓN
2.1 Dosis y régimen recomendados
La dosis recomendada de IBRANCE es un comprimido de 125 mg administrado por vía oral una vez al día durante 21 días consecutivos, seguidos de 7 días sin tratamiento para completar un ciclo de 28 días. IBRANCE debe tomarse con alimentos [véase Farmacología clínica (12.3)].
Administrar la dosis recomendada de un inhibidor de la aromatasa cuando se administra con IBRANCE. Consulte la información completa de prescripción para el inhibidor de la aromatasa que se esté utilizando.
Cuando se administra con IBRANCE, la dosis recomendada de fulvestrant es de 500 mg administrada los días 1, 15, 29 y una vez al mes a partir de entonces. Consulte la información completa de prescripción de fulvestrant.
Se debe animar a los pacientes a tomar su dosis de IBRANCE aproximadamente a la misma hora cada día.
Si el paciente vomita u olvida una dosis, no debe tomar una dosis adicional. La siguiente dosis prescrita debe tomarse a la hora habitual. Los comprimidos de IBRANCE deben tragarse enteros (no deben masticarse, triturarse ni abrirse antes de tragarlos). Los comprimidos no deben ingerirse si están rotos, agrietados o no están intactos.
Las mujeres pre/perimenopáusicas tratadas con la combinación de IBRANCE más un inhibidor de la aromatasa o terapia con fulvestrant también deben ser tratadas con agonistas de la hormona liberadora de hormona luteinizante (LHRH) de acuerdo con los estándares actuales de la práctica clínica.
Para los hombres tratados con la combinación de IBRANCE más terapia con inhibidor de la aromatasa, considere el tratamiento con un agonista de la LHRH de acuerdo con los estándares actuales de la práctica clínica.
2.2 Modificación de la dosis
Las modificaciones de la dosis recomendadas para las reacciones adversas se enumeran en las Tablas 1, 2 y 3.
| Nivel de dosis | Dosis |
|---|---|
|
|
|
Dosis inicial recomendada |
125 mg/día |
|
Primera reducción de la dosis |
100 mg/día |
|
Segunda reducción de la dosis |
75 mg/día* |
| Grados según CTCAE 4.0. CTCAE=Criterios terminológicos comunes para eventos adversos; LLN=límite inferior de la normalidad. |
|
|
|
|
Controlar los hemogramas completos antes de comenzar el tratamiento con IBRANCE y al comienzo de cada ciclo, así como el día 15 de los dos primeros ciclos, y según esté clínicamente indicado. |
|
|
Grado CTCAE |
Modificaciones de la dosis |
|
Grado 1 o 2 |
No se requiere ajuste de la dosis. |
|
Grado 3 |
Día 1 del ciclo: |
|
Neutropenia de grado 3† con fiebre ≥38.5 ºC o infección |
En cualquier momento: |
|
En cualquier momento: |
|
| Grado CTCAE | Modificaciones de la dosis |
|---|---|
| Grados según CTCAE 4.0. CTCAE=Criterios terminológicos comunes para eventos adversos. |
|
|
Grado 1 o 2 |
No se requiere ajuste de la dosis. |
|
Toxicidad no hematológica de grado ≥3 (si persiste a pesar del tratamiento médico óptimo) |
Suspender hasta que los síntomas se resuelvan a:
Reanudar con la dosis inmediatamente inferior. |
Suspenda permanentemente IBRANCE en pacientes con enfermedad pulmonar intersticial (ILD)/neumonitis grave.
Consulte la información completa de prescripción para obtener pautas de ajuste de la dosis de la terapia endocrina coadministrada en caso de toxicidad y otra información de seguridad o contraindicaciones relevantes.
Modificaciones de la dosis para su uso con inhibidores potentes del CYP3A
Evite el uso concomitante de inhibidores potentes del CYP3A y considere un medicamento concomitante alternativo sin o con mínima inhibición del CYP3A. Si los pacientes deben recibir un inhibidor potente del CYP3A de forma concomitante, reduzca la dosis de IBRANCE a 75 mg una vez al día. Si se suspende el inhibidor potente, aumente la dosis de IBRANCE (después de 3 a 5 semividas del inhibidor) a la dosis utilizada antes del inicio del inhibidor potente del CYP3A [véase Interacciones medicamentosas (7.1) y Farmacología clínica (12.3)].
Modificaciones de la dosis para insuficiencia hepática
No se requiere ajuste de la dosis para pacientes con insuficiencia hepática leve o moderada (clases A y B de Child-Pugh). Para pacientes con insuficiencia hepática grave (clase C de Child-Pugh), la dosis recomendada de IBRANCE es de 75 mg una vez al día durante 21 días consecutivos seguidos de 7 días sin tratamiento para completar un ciclo de 28 días [véase Uso en poblaciones específicas (8.6) y Farmacología clínica (12.3)].
3 FORMAS DE DOSIFICACIÓN Y CONCENTRACIONES
Cápsulas de 125 mg: cápsulas de gelatina dura, opacas, tamaño 0, con tapa y cuerpo color caramelo, impresas con tinta blanca “Pfizer” en la tapa y “PBC 125” en el cuerpo.
Cápsulas de 100 mg: cápsulas de gelatina dura, opacas, tamaño 1, con tapa color caramelo y cuerpo color naranja claro, impresas con tinta blanca “Pfizer” en la tapa y “PBC 100” en el cuerpo.
Cápsulas de 75 mg: cápsulas de gelatina dura, opacas, tamaño 2, con tapa y cuerpo color naranja claro, impresas con tinta blanca “Pfizer” en la tapa y “PBC 75” en el cuerpo.
4 CONTRAINDICACIONES
Ninguna.
5 ADVERTENCIAS Y PRECAUCIONES
5.1 Neutropenia
La neutropenia fue la reacción adversa notificada con mayor frecuencia en PALOMA-2, con una incidencia del 80 %, y en PALOMA-3, con una incidencia del 83 %. Se notificó una disminución de Grado ≥3 en el recuento de neutrófilos en el 66 % de las pacientes que recibieron IBRANCE más letrozol en PALOMA-2 y en el 66 % de las pacientes que recibieron IBRANCE más fulvestrant en PALOMA-3. En PALOMA-2 y PALOMA-3, la mediana del tiempo hasta el primer episodio de neutropenia de cualquier grado fue de 15 días y la mediana de la duración de la neutropenia de Grado ≥3 fue de 7 días [see Adverse Reactions (6.1)].
Controle los hemogramas completos antes de iniciar el tratamiento con IBRANCE y al comienzo de cada ciclo, así como en el día 15 de los 2 primeros ciclos, y según esté clínicamente indicado. Se recomienda la interrupción de la dosis, la reducción de la dosis o el retraso en el inicio de los ciclos de tratamiento para las pacientes que desarrollen neutropenia de Grado 3 o 4 [see Dosage and Administration (2.2)].
Se ha notificado neutropenia febril en el 1.8 % de las pacientes expuestas a IBRANCE en PALOMA-2 y PALOMA-3. Se observó una muerte por sepsis neutropénica en PALOMA-3. Los médicos deben informar a las pacientes que notifiquen inmediatamente cualquier episodio de fiebre [see Patient Counseling Information (17)].
5.2 Enfermedad Pulmonar Intersticial (EPI)/Neumonitis
En pacientes tratadas con inhibidores de la quinasa 4/6 dependiente de ciclina (CDK4/6), incluido IBRANCE cuando se toma en combinación con terapia endocrina, puede producirse enfermedad pulmonar intersticial (EPI) y/o neumonitis grave, potencialmente mortal o mortal.
En los ensayos clínicos (PALOMA-1, PALOMA-2, PALOMA-3), el 1.0 % de las pacientes tratadas con IBRANCE presentaron EPI/neumonitis de cualquier grado, el 0.1 % presentaron Grado 3 o 4 y no se notificaron casos mortales. Se han observado casos adicionales de EPI/neumonitis en la fase posterior a la comercialización, con notificaciones de muertes [see Adverse Reactions (6.2)].
Controle a las pacientes para detectar síntomas pulmonares indicativos de EPI/neumonitis (p. ej., hipoxia, tos, disnea). En pacientes que presenten síntomas respiratorios nuevos o que empeoren y se sospeche que han desarrollado neumonitis, interrumpa IBRANCE inmediatamente y evalúe a la paciente. Interrumpa permanentemente IBRANCE en pacientes con EPI o neumonitis grave [see Dosage and Administration (2.2)].
5.3 Toxicidad Embrio-Fetal
Según los hallazgos de estudios en animales y su mecanismo de acción, IBRANCE puede causar daño fetal cuando se administra a una mujer embarazada. En estudios de reproducción animal, la administración de palbociclib a ratas y conejas preñadas durante la organogénesis resultó en toxicidad embriofetal a exposiciones maternas que fueron ≥4 veces la exposición clínica humana según el área bajo la curva (AUC). Informe a las mujeres embarazadas sobre el riesgo potencial para el feto. Aconseje a las mujeres en edad fértil que utilicen métodos anticonceptivos eficaces durante el tratamiento con IBRANCE y durante al menos 3 semanas después de la última dosis [see Use in Specific Populations (8.1 and 8.3) and Clinical Pharmacology (12.1)].
6 REACCIONES ADVERSAS
Las siguientes reacciones adversas clínicamente significativas se describen en otras partes del etiquetado:
- •
- Neutropenia [ver Advertencias y precauciones (5.1)]
- •
- ILD/Neumonitis [ver Advertencias y precauciones (5.2)]
6.1 Experiencia en estudios clínicos
Debido a que los ensayos clínicos se realizan en diversas condiciones, las tasas de reacciones adversas observadas no pueden compararse directamente con las tasas en otros ensayos y pueden no reflejar las tasas observadas en la práctica clínica.
PALOMA-2: IBRANCE más Letrozol
Pacientes con cáncer de mama avanzado o metastásico, receptor de estrógenos (ER)-positivo, HER2-negativo para terapia inicial basada en endocrinología
La seguridad de IBRANCE (125 mg/día) más letrozol (2,5 mg/día) versus placebo más letrozol se evaluó en PALOMA-2. Los datos que se describen a continuación reflejan la exposición a IBRANCE en 444 de 666 pacientes con cáncer de mama avanzado ER-positivo, HER2-negativo que recibieron al menos 1 dosis de IBRANCE más letrozol en PALOMA-2. La duración mediana del tratamiento con IBRANCE más letrozol fue de 19,8 meses, mientras que la duración mediana del tratamiento con placebo más letrozol fue de 13,8 meses.
Las reducciones de dosis debido a una reacción adversa de cualquier grado ocurrieron en el 36% de los pacientes que recibieron IBRANCE más letrozol. No se permitió ninguna reducción de dosis para letrozol en PALOMA-2.
La interrupción permanente asociada con una reacción adversa ocurrió en 43 de 444 (9,7%) pacientes que recibieron IBRANCE más letrozol y en 13 de 222 (5,9%) pacientes que recibieron placebo más letrozol. Las reacciones adversas que llevaron a la interrupción permanente para los pacientes que recibieron IBRANCE más letrozol incluyeron neutropenia (1,1%) y aumento de la alanina aminotransferasa (0,7%).
Las reacciones adversas más comunes (≥10%) de cualquier grado notificadas en pacientes en el brazo de IBRANCE más letrozol por frecuencia descendente fueron neutropenia, infecciones, leucopenia, fatiga, náuseas, alopecia, estomatitis, diarrea, anemia, erupción cutánea, astenia, trombocitopenia, vómitos, disminución del apetito, piel seca, pirexia y disgeusia.
Las reacciones adversas de Grado ≥3 más frecuentemente notificadas (≥5%) en pacientes que recibieron IBRANCE más letrozol por frecuencia descendente fueron neutropenia, leucopenia, infecciones y anemia.
Las reacciones adversas (≥10%) notificadas en pacientes que recibieron IBRANCE más letrozol o placebo más letrozol en PALOMA-2 se enumeran en la Tabla 4.
| IBRANCE más Letrozol (N=444) |
Placebo más Letrozol (N=222) |
|||||
|---|---|---|---|---|---|---|
| Reacción adversa | Todos los grados % |
Grado 3 % |
Grado 4 % |
Todos los grados % |
Grado 3 % |
Grado 4 % |
| Grados según CTCAE 4.0. CTCAE=Criterios de terminología común para eventos adversos; N=número de pacientes; N/A=no aplicable; |
||||||
|
||||||
|
Infecciones e infestaciones |
||||||
|
Infecciones* |
60† |
6 |
1 |
42 |
3 |
0 |
|
Trastornos de la sangre y del sistema linfático |
||||||
|
Neutropenia |
80 |
56 |
10 |
6 |
1 |
1 |
|
Leucopenia |
39 |
24 |
1 |
2 |
0 |
0 |
|
Anemia |
24 |
5 |
<1 |
9 |
2 |
0 |
|
Trombocitopenia |
16 |
1 |
<1 |
1 |
0 |
0 |
|
Trastornos del metabolismo y de la nutrición |
||||||
|
Disminución del apetito |
15 |
1 |
0 |
9 |
0 |
0 |
|
Trastornos del sistema nervioso |
||||||
|
Disgeusia |
10 |
0 |
0 |
5 |
0 |
0 |
|
Trastornos gastrointestinales |
||||||
|
Estomatitis‡ |
30 |
1 |
0 |
14 |
0 |
0 |
|
Náuseas |
35 |
<1 |
0 |
26 |
2 |
0 |
|
Diarrea |
26 |
1 |
0 |
19 |
1 |
0 |
|
Vómitos |
16 |
1 |
0 |
17 |
1 |
0 |
|
Trastornos de la piel y del tejido subcutáneo |
||||||
|
Alopecia |
33§ |
N/A |
N/A |
16¶ |
N/A |
N/A |
|
Erupción# |
18 |
1 |
0 |
12 |
1 |
0 |
|
Piel seca |
12 |
0 |
0 |
6 |
0 |
0 |
|
Trastornos generales y afecciones en el lugar de administración |
||||||
|
Fatiga |
37 |
2 |
0 |
28 |
1 |
0 |
|
Astenia |
17 |
2 |
0 |
12 |
0 |
0 |
|
Pirexia |
12 |
0 |
0 |
9 |
0 |
0 |
Otras reacciones adversas que ocurrieron con una incidencia general de <10.0% en pacientes que recibieron IBRANCE más letrozol en PALOMA-2 incluyeron aumento de la alanina aminotransferasa (9.9%), aumento de la aspartato aminotransferasa (9.7%), epistaxis (9.2%), aumento de la lagrimación (5.6%), ojo seco (4.1%), visión borrosa (3.6%) y neutropenia febril (2.5%).
| IBRANCE más Letrozol (N=444) |
Placebo más Letrozol (N=222) |
|||||
|---|---|---|---|---|---|---|
| Anormalidad de laboratorio | Todos los grados % |
Grado 3 % |
Grado 4 % |
Todos los grados % |
Grado 3 % |
Grado 4 % |
| N=número de pacientes; WBC=glóbulos blancos. | ||||||
|
Disminución de los glóbulos blancos |
97 |
35 |
1 |
25 |
1 |
0 |
|
Disminución de neutrófilos |
95 |
56 |
12 |
20 |
1 |
1 |
|
Anemia |
78 |
6 |
0 |
42 |
2 |
0 |
|
Disminución de plaquetas |
63 |
1 |
1 |
14 |
0 |
0 |
|
Aumento de la aspartato aminotransferasa |
52 |
3 |
0 |
34 |
1 |
0 |
|
Aumento de la alanina aminotransferasa |
43 |
2 |
<1 |
30 |
0 |
0 |
PALOMA-3: IBRANCE plus Fulvestrant
Pacientes con cáncer de mama avanzado o metastásico, HR-positivo y HER2-negativo que han presentado progresión de la enfermedad durante o después de una terapia endocrina adyuvante o metastásica previa
La seguridad de IBRANCE (125 mg/día) más fulvestrant (500 mg) frente a placebo más fulvestrant se evaluó en PALOMA-3. Los datos que se describen a continuación reflejan la exposición a IBRANCE en 345 de 517 pacientes con cáncer de mama avanzado o metastásico, HR-positivo y HER2-negativo que recibieron al menos 1 dosis de IBRANCE más fulvestrant en PALOMA-3. La duración media del tratamiento con IBRANCE más fulvestrant fue de 10,8 meses, mientras que la duración media del tratamiento con placebo más fulvestrant fue de 4,8 meses.
Se produjeron reducciones de dosis debido a una reacción adversa de cualquier grado en el 36 % de los pacientes que recibieron IBRANCE más fulvestrant. No se permitió ninguna reducción de la dosis de fulvestrant en PALOMA-3.
La interrupción permanente asociada con una reacción adversa se produjo en 19 de 345 (6 %) pacientes que recibieron IBRANCE más fulvestrant y en 6 de 172 (3 %) pacientes que recibieron placebo más fulvestrant. Las reacciones adversas que llevaron a la interrupción en los pacientes que recibieron IBRANCE más fulvestrant incluyeron fatiga (0,6 %), infecciones (0,6 %) y trombocitopenia (0,6 %).
Las reacciones adversas más frecuentes (≥10 %) de cualquier grado notificadas en pacientes del brazo de IBRANCE más fulvestrant por frecuencia descendente fueron neutropenia, leucopenia, infecciones, fatiga, náuseas, anemia, estomatitis, diarrea, trombocitopenia, vómitos, alopecia, erupción cutánea, disminución del apetito y pirexia.
Las reacciones adversas de grado ≥3 más frecuentes (≥5 %) en pacientes que recibieron IBRANCE más fulvestrant por frecuencia descendente fueron neutropenia y leucopenia.
Las reacciones adversas (≥10 %) notificadas en pacientes que recibieron IBRANCE más fulvestrant o placebo más fulvestrant en PALOMA-3 se enumeran en la Tabla 6.
| Reacción adversa | IBRANCE plus Fulvestrant (N=345) |
Placebo plus Fulvestrant (N=172) |
||||
|---|---|---|---|---|---|---|
| Todos los grados | Grado 3 | Grado 4 | Todos los grados | Grado 3 | Grado 4 | |
| % | % | % | % | % | % | |
| Grados según CTCAE 4.0. CTCAE=Criterios terminológicos comunes para eventos adversos; N=número de pacientes; N/A=no aplicable. |
||||||
|
||||||
|
Infecciones e infestaciones |
||||||
|
Infecciones* |
47† |
3 |
1 |
31 |
3 |
0 |
|
Trastornos de la sangre y del sistema linfático |
||||||
|
Neutropenia |
83 |
55 |
11 |
4 |
1 |
0 |
|
Leucopenia |
53 |
30 |
1 |
5 |
1 |
1 |
|
Anemia |
30 |
4 |
0 |
13 |
2 |
0 |
|
Trombocitopenia |
23 |
2 |
1 |
0 |
0 |
0 |
|
Trastornos del metabolismo y la nutrición |
||||||
|
Disminución del apetito |
16 |
1 |
0 |
8 |
1 |
0 |
|
Trastornos gastrointestinales |
||||||
|
Náuseas |
34 |
0 |
0 |
28 |
1 |
0 |
|
Estomatitis‡ |
28 |
1 |
0 |
13 |
0 |
0 |
|
Diarrea |
24 |
0 |
0 |
19 |
1 |
0 |
|
Vómitos |
19 |
1 |
0 |
15 |
1 |
0 |
|
Trastornos de la piel y del tejido subcutáneo |
||||||
|
Alopecia |
18§ |
N/A |
N/A |
6¶ |
N/A |
N/A |
|
Rash# |
17 |
1 |
0 |
6 |
0 |
0 |
|
Trastornos generales y alteraciones en el lugar de administración |
||||||
|
Fatiga |
41 |
2 |
0 |
29 |
1 |
0 |
|
Pirexia |
13 |
<1 |
0 |
5 |
0 |
0 |
Otras reacciones adversas que ocurrieron con una incidencia general de <10.0% en pacientes que recibieron IBRANCE más fulvestrant en PALOMA-3 incluyeron astenia (7.5%), aumento de la aspartato aminotransferasa (7.5%), disgeusia (6.7%), epistaxis (6.7%), aumento de la lagrimación (6.4%), piel seca (6.1%), aumento de la alanina aminotransferasa (5.8%), visión borrosa (5.8%), ojo seco (3.8%) y neutropenia febril (0.9%).
| Anormalidad de laboratorio | IBRANCE más Fulvestrant (N=345) |
Placebo más Fulvestrant (N=172) |
||||
|---|---|---|---|---|---|---|
| Todos los grados % |
Grado 3 % |
Grado 4 % |
Todos los grados % |
Grado 3 % |
Grado 4 % |
|
| N=número de pacientes; WBC=glóbulos blancos. | ||||||
|
Disminución de los glóbulos blancos |
99 |
45 |
1 |
26 |
0 |
1 |
|
Disminución de neutrófilos |
96 |
56 |
11 |
14 |
0 |
1 |
|
Anemia |
78 |
3 |
0 |
40 |
2 |
0 |
|
Disminución de plaquetas |
62 |
2 |
1 |
10 |
0 |
0 |
|
Aumento de la aspartato aminotransferasa |
43 |
4 |
0 |
48 |
4 |
0 |
|
Aumento de la alanina aminotransferasa |
36 |
2 |
0 |
34 |
0 |
0 |
Experiencia en otros ensayos clínicos
Se ha notificado la siguiente reacción adversa tras la administración de IBRANCE: tromboembolismo venoso.
6.2 Experiencia post-comercialización
Las siguientes reacciones adversas se han identificado durante el uso post-aprobación de IBRANCE. Debido a que estas reacciones se notifican voluntariamente a partir de una población de tamaño incierto, no siempre es posible estimar de forma fiable su frecuencia o establecer una relación causal con la exposición al fármaco.
Trastornos respiratorios: Enfermedad pulmonar intersticial (ILD)/neumonitis no infecciosa
Trastornos de la piel y del tejido subcutáneo: Síndrome de eritrodisestesia palmar-plantar (PPES)
Pacientes varones con cáncer de mama avanzado o metastásico HR-positivo, HER2-negativo
Basándose en datos limitados de informes post-comercialización y registros electrónicos de salud, el perfil de seguridad para los hombres tratados con IBRANCE es consistente con el perfil de seguridad en las mujeres tratadas con IBRANCE.
7 INTERACCIONES MEDICAMENTOSAS
El palbociclib se metaboliza principalmente mediante el CYP3A y la sulfotransferasa (SULT), enzima SULT2A1. In vivo, el palbociclib es un inhibidor dependiente del tiempo del CYP3A.
7.1 Agentes que pueden aumentar las concentraciones plasmáticas de palbociclib
Efecto de los inhibidores del CYP3A
La administración conjunta de un inhibidor potente del CYP3A (itraconazol) aumentó la exposición plasmática al palbociclib en sujetos sanos en un 87 %. Evite el uso concomitante de inhibidores potentes del CYP3A (p. ej., claritromicina, indinavir, itraconazol, ketoconazol, lopinavir/ritonavir, nefazodona, nelfinavir, posaconazol, ritonavir, saquinavir, telaprevir, telithromicina y voriconazol). Evite el pomelo o el zumo de pomelo durante el tratamiento con IBRANCE. Si no se puede evitar la administración conjunta de IBRANCE con un inhibidor potente del CYP3A, reduzca la dosis de IBRANCE [véase Posología y administración (2.2) y Farmacología clínica (12.3)].
7.2 Agentes que pueden disminuir las concentraciones plasmáticas de palbociclib
Efecto de los inductores del CYP3A
La administración conjunta de un inductor potente del CYP3A (rifampicina) disminuyó la exposición plasmática al palbociclib en sujetos sanos en un 85 %. Evite el uso concomitante de inductores potentes del CYP3A (p. ej., fenitoína, rifampicina, carbamazepina, enzalutamida y hierba de San Juan) [véase Farmacología clínica (12.3)].
7.3 Fármacos cuyas concentraciones plasmáticas pueden verse alteradas por el palbociclib
La administración conjunta de midazolam con dosis múltiples de IBRANCE aumentó la exposición plasmática al midazolam en un 61 % en sujetos sanos, en comparación con la administración de midazolam solo. Puede ser necesario reducir la dosis del sustrato sensible del CYP3A con un índice terapéutico estrecho (p. ej., alfentanilo, ciclosporina, dihidroergotamina, ergotamina, everolimus, fentanilo, pimozida, quinidina, sirolimus y tacrolimus), ya que IBRANCE puede aumentar su exposición [véase Farmacología clínica (12.3)].
8 USO EN POBLACIONES ESPECÍFICAS
8.1 Embarazo
Resumen de riesgos
Con base en los hallazgos de estudios en animales y su mecanismo de acción, IBRANCE puede causar daño fetal cuando se administra a una mujer embarazada [ver Farmacología clínica (12.1)]. No hay datos disponibles en mujeres embarazadas para informar el riesgo asociado con el medicamento. En estudios de reproducción animal, la administración de palbociclib a ratas y conejas preñadas durante la organogénesis resultó en toxicidad embriofetal a exposiciones maternas que fueron ≥4 veces la exposición clínica humana según el AUC [ver Datos]. Informe a las mujeres embarazadas sobre el riesgo potencial para el feto.
Se desconoce el riesgo subyacente estimado de defectos congénitos importantes y aborto espontáneo para la población indicada. En la población general de EE. UU., el riesgo subyacente estimado de defectos congénitos importantes y aborto espontáneo en embarazos clínicamente reconocidos es del 2 % al 4 % y del 15 % al 20 %, respectivamente.
Datos
Datos en animales
En un estudio de fertilidad y desarrollo embrionario temprano en ratas hembra, se administró palbociclib por vía oral durante 15 días antes del apareamiento hasta el día 7 de embarazo, lo que no causó toxicidad embrionaria en dosis de hasta 300 mg/kg/día con exposiciones sistémicas maternas de aproximadamente 4 veces la exposición humana (AUC) a la dosis recomendada.
En estudios de desarrollo embriofetal en ratas y conejas, los animales preñados recibieron dosis orales de palbociclib de hasta 300 mg/kg/día y 20 mg/kg/día, respectivamente, durante el período de organogénesis. La dosis maternalmente tóxica de 300 mg/kg/día fue fetotóxica en ratas, lo que resultó en una reducción del peso corporal fetal. En dosis ≥100 mg/kg/día en ratas, hubo una mayor incidencia de una variación esquelética (mayor incidencia de una costilla presente en la séptima vértebra cervical). A la dosis maternalmente tóxica de 20 mg/kg/día en conejas, hubo una mayor incidencia de variaciones esqueléticas, incluidas falanges pequeñas en la extremidad anterior. A 300 mg/kg/día en ratas y 20 mg/kg/día en conejas, las exposiciones sistémicas maternas fueron aproximadamente 4 y 9 veces la exposición humana (AUC) a la dosis recomendada, respectivamente.
Se ha informado que los ratones con doble nocaut de CDK4/6 mueren en las últimas etapas del desarrollo fetal (día 14.5 de gestación hasta el nacimiento) debido a anemia grave. Sin embargo, los datos de ratones con nocaut pueden no ser predictivos de los efectos en humanos debido a las diferencias en el grado de inhibición del objetivo.
8.2 Lactancia
Resumen de riesgos
No hay información sobre la presencia de palbociclib en la leche humana, sus efectos sobre la producción de leche o el lactante. Debido al potencial de reacciones adversas graves en lactantes por IBRANCE, aconseje a la mujer que está amamantando que no lo haga durante el tratamiento con IBRANCE y durante 3 semanas después de la última dosis.
8.3 Mujeres y hombres con potencial reproductivo
Prueba de embarazo
Según estudios en animales, IBRANCE puede causar daño fetal cuando se administra a una mujer embarazada [ver Uso en poblaciones específicas (8.1)]. Las mujeres con potencial reproductivo deben someterse a una prueba de embarazo antes de comenzar el tratamiento con IBRANCE.
Anticoncepción
Mujeres
IBRANCE puede causar daño fetal cuando se administra a una mujer embarazada [ver Uso en poblaciones específicas (8.1)]. Aconseje a las mujeres con potencial reproductivo que utilicen métodos anticonceptivos eficaces durante el tratamiento con IBRANCE y durante al menos 3 semanas después de la última dosis.
Hombres
Debido al potencial de genotoxicidad, aconseje a los pacientes masculinos con parejas femeninas con potencial reproductivo que utilicen métodos anticonceptivos eficaces durante el tratamiento con IBRANCE y durante 3 meses después de la última dosis [ver Toxicología no clínica (13.1)].
Infertilidad
Hombres
Según estudios en animales, IBRANCE puede afectar la fertilidad en hombres con potencial reproductivo [ver Toxicología no clínica (13.1)].
8.4 Uso pediátrico
No se ha estudiado la seguridad y eficacia de IBRANCE en pacientes pediátricos.
Se identificaron alteraciones del metabolismo de la glucosa (glucosuria, hiperglucemia, disminución de la insulina) asociadas con cambios en el páncreas (vacuolización de las células de los islotes), ojos (cataratas, degeneración del cristalino), riñones (vacuolización tubular, nefropatía crónica progresiva) y tejido adiposo (atrofia) en un estudio toxicológico de dosis repetidas de 27 semanas en ratas que eran inmaduras al comienzo de los estudios y fueron más frecuentes en machos con dosis orales de palbociclib ≥30 mg/kg/día (aproximadamente 11 veces la exposición humana adulta [AUC] a la dosis recomendada). Algunos de estos hallazgos (glucosuria/hiperglucemia, vacuolización de las células de los islotes pancreáticos y vacuolización de los túbulos renales) estuvieron presentes con menor incidencia y gravedad en un estudio toxicológico de dosis repetidas de 15 semanas en ratas inmaduras. No se identificaron alteraciones del metabolismo de la glucosa ni cambios asociados en el páncreas, los ojos, los riñones y el tejido adiposo en un estudio toxicológico de dosis repetidas de 27 semanas en ratas que eran maduras al comienzo del estudio y en perros en estudios toxicológicos de dosis repetidas de hasta 39 semanas de duración.
Se observaron toxicidades en los dientes independientes de la alteración del metabolismo de la glucosa en ratas. La administración de 100 mg/kg de palbociclib durante 27 semanas (aproximadamente 15 veces la exposición humana adulta [AUC] a la dosis recomendada) resultó en anomalías en los dientes incisivos en crecimiento (decoloración, degeneración/necrosis de ameloblastos, infiltrado de células mononucleares). Otras toxicidades de posible interés para pacientes pediátricos no se han evaluado en animales juveniles.
8.5 Uso Geriátrico
De los 444 pacientes que recibieron IBRANCE en PALOMA-2, 181 pacientes (41%) tenían ≥65 años de edad y 48 pacientes (11%) tenían ≥75 años de edad. De los 347 pacientes que recibieron IBRANCE en PALOMA-3, 86 pacientes (25%) tenían ≥65 años de edad y 27 pacientes (8%) tenían ≥75 años de edad. No se observaron diferencias generales en la seguridad o la eficacia de IBRANCE entre estos pacientes y los pacientes más jóvenes.
8.6 Insuficiencia Hepática
No se requiere ajuste de dosis en pacientes con insuficiencia hepática leve o moderada (clases A y B de Child-Pugh). Para pacientes con insuficiencia hepática grave (clase C de Child-Pugh), la dosis recomendada de IBRANCE es de 75 mg una vez al día durante 21 días consecutivos seguidos de 7 días sin tratamiento para completar un ciclo completo de 28 días [see Dosage and Administration (2.2)]. Según un ensayo farmacocinético en sujetos con diversos grados de función hepática, la exposición a palbociclib libre (AUCINF libre) disminuyó en un 17% en sujetos con insuficiencia hepática leve (clase A de Child-Pugh) y aumentó en un 34% y un 77% en sujetos con insuficiencia hepática moderada (clase B de Child-Pugh) y grave (clase C de Child-Pugh), respectivamente, en relación con los sujetos con función hepática normal. La exposición máxima a palbociclib libre (Cmax libre) aumentó en un 7%, 38% y 72% para la insuficiencia hepática leve, moderada y grave, respectivamente, en relación con los sujetos con función hepática normal [see Clinical Pharmacology (12.3)].
Revise la información de prescripción completa del inhibidor de la aromatasa o fulvestrant para las modificaciones de dosis relacionadas con la insuficiencia hepática.
8.7 Insuficiencia Renal
No se requiere ajuste de dosis en pacientes con insuficiencia renal leve, moderada o grave (CrCl >15 mL/min). Según un ensayo farmacocinético en sujetos con diversos grados de función renal, la exposición total a palbociclib (AUCINF) aumentó en un 39%, 42% y 31% con insuficiencia renal leve (60 mL/min ≤ CrCl <90 mL/min), moderada (30 mL/min ≤ CrCl <60 mL/min) y grave (CrCl <30 mL/min), respectivamente, en relación con los sujetos con función renal normal. La exposición máxima a palbociclib (Cmax) aumentó en un 17%, 12% y 15% para la insuficiencia renal leve, moderada y grave, respectivamente, en relación con los sujetos con función renal normal. La farmacocinética de palbociclib no se ha estudiado en pacientes que requieren hemodiálisis [see Clinical Pharmacology (12.3)].
10 SOBREDOSIS
No se conoce ningún antídoto para IBRANCE. El tratamiento de la sobredosis de IBRANCE debe consistir en medidas de apoyo generales.
11 DESCRIPCIÓN
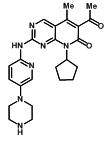
Las cápsulas de IBRANCE para administración oral contienen 125 mg, 100 mg o 75 mg de palbociclib, un inhibidor de la quinasa. La fórmula molecular del palbociclib es C24H29N7O2. El peso molecular es de 447.54 daltons. El nombre químico es 6-acetil-8-ciclopentil-5-metil-2-{[5-(piperazin-1-il)piridin-2-il]amino}pirido[2,3-d]pirimidin-7(8H)-ona, y su fórmula estructural es:
Palbociclib es un polvo de color amarillo a naranja con un pKa de 7.4 (el nitrógeno secundario de la piperazina) y 3.9 (el nitrógeno de la piridina). A un pH de 4 o inferior, palbociclib se comporta como un compuesto de alta solubilidad. Por encima de un pH de 4, la solubilidad del fármaco se reduce significativamente.
Ingredientes inactivos: Celulosa microcristalina, lactosa monohidrato, glicolato sódico de almidón, dióxido de silicio coloidal, estearato de magnesio y cápsulas de gelatina dura. Las cápsulas opacas de color naranja claro, naranja claro/caramelo y caramelo contienen gelatina, óxido de hierro rojo, óxido de hierro amarillo y dióxido de titanio; la tinta de impresión contiene goma laca, dióxido de titanio, hidróxido de amonio, propilenglicol y simeticona.
12 FARMACOLOGÍA CLÍNICA
12.1 Mecanismo de acción
Palbociclib es un inhibidor de las cinasas dependientes de ciclina (CDK) 4 y 6. La ciclina D1 y CDK4/6 se encuentran aguas abajo de las vías de señalización que conducen a la proliferación celular. In vitro, palbociclib redujo la proliferación celular de líneas celulares de cáncer de mama con receptor de estrógenos (ER) positivo al bloquear la progresión de la célula de la fase G1 a la fase S del ciclo celular. El tratamiento de líneas celulares de cáncer de mama con la combinación de palbociclib y antiestrógenos conduce a una disminución de la fosforilación de la proteína retinoblastoma (Rb), lo que resulta en una reducción de la expresión y señalización de E2F y un aumento del arresto del crecimiento en comparación con el tratamiento con cada fármaco por separado. El tratamiento in vitro de líneas celulares de cáncer de mama con receptor de estrógenos positivo con la combinación de palbociclib y antiestrógenos provocó un aumento de la senescencia celular en comparación con cada fármaco por separado, que se mantuvo hasta 6 días después de la retirada de palbociclib y fue mayor si se continuó el tratamiento con antiestrógenos. Los estudios in vivo con un modelo de xenotrasplante de cáncer de mama con receptor de estrógenos positivo derivado de pacientes demostraron que la combinación de palbociclib y letrozol aumentó la inhibición de la fosforilación de Rb, la señalización aguas abajo y el crecimiento tumoral en comparación con cada fármaco por separado.
Las células mononucleares de médula ósea humana tratadas con palbociclib en presencia o ausencia de un anti-estrógeno in vitro no se volvieron senescentes y reanudaron la proliferación después de la retirada de palbociclib.
12.2 Farmacodinamia
Electrofisiología cardíaca
El efecto de palbociclib en el intervalo QT corregido para la frecuencia cardíaca (QTc) se evaluó utilizando electrocardiogramas (ECG) coincidentes en el tiempo que evaluaron el cambio con respecto a la línea de base y los datos farmacocinéticos correspondientes en 77 pacientes con cáncer de mama. Palbociclib no tuvo un gran efecto en el QTc (es decir, >20 ms) a 125 mg una vez al día durante 21 días consecutivos seguidos de 7 días sin tratamiento para completar un ciclo de 28 días.
12.3 Farmacocinética
La farmacocinética (PK) de palbociclib se caracterizó en pacientes con tumores sólidos, incluido el cáncer de mama avanzado, y en sujetos sanos.
Absorción
La concentración máxima observada media (Cmax) de palbociclib generalmente se observa entre 6 y 12 horas (tiempo para alcanzar la concentración máxima, Tmax) después de la administración oral. La biodisponibilidad absoluta media de IBRANCE después de una dosis oral de 125 mg es del 46 %. En el rango de dosificación de 25 mg a 225 mg, el AUC y la Cmax aumentaron proporcionalmente con la dosis en general. El estado estacionario se logró dentro de los 8 días posteriores a la administración repetida una vez al día. Con la administración repetida una vez al día, palbociclib se acumuló con una relación de acumulación mediana de 2,4 (rango de 1,5 a 4,2).
Efecto de los alimentos: La absorción y la exposición a palbociclib fueron muy bajas en aproximadamente el 13 % de la población en condiciones de ayuno. La ingesta de alimentos aumentó la exposición a palbociclib en este pequeño subconjunto de la población, pero no alteró la exposición a palbociclib en el resto de la población en una medida clínicamente relevante. Por lo tanto, la ingesta de alimentos redujo la variabilidad interindividual de la exposición a palbociclib, lo que respalda la administración de IBRANCE con alimentos. En comparación con IBRANCE administrado en ayunas durante la noche, el promedio poblacional del área bajo la curva de concentración-tiempo desde cero hasta el infinito (AUCINF) y la Cmax de palbociclib aumentaron en un 21 % y un 38 %, respectivamente, cuando se administró con alimentos ricos en grasas y calorías (aproximadamente 800 a 1000 calorías con 150, 250 y 500 a 600 calorías de proteínas, carbohidratos y grasas, respectivamente), en un 12 % y un 27 %, respectivamente, cuando se administró con alimentos bajos en grasas y calorías (aproximadamente 400 a 500 calorías con 120, 250 y 28 a 35 calorías de proteínas, carbohidratos y grasas, respectivamente), y en un 13 % y un 24 %, respectivamente, cuando se administró alimentos con contenido moderado de grasa y calorías estándar (aproximadamente 500 a 700 calorías con 75 a 105, 250 a 350 y 175 a 245 calorías de proteínas, carbohidratos y grasas, respectivamente) 1 hora antes y 2 horas después de la administración de IBRANCE.
Distribución
La unión de palbociclib a las proteínas plasmáticas humanas in vitro fue de aproximadamente el 85 %, sin dependencia de la concentración en el rango de concentración de 500 ng/ml a 5000 ng/ml. La fracción libre media (fu) de palbociclib en plasma humano in vivo aumentó incrementalmente con el empeoramiento de la función hepática. No hubo una tendencia obvia en la fu media de palbociclib en plasma humano in vivo con el empeoramiento de la función renal. La media geométrica del volumen aparente de distribución (Vz/F) fue de 2583 L con un coeficiente de variación (CV) del 26 %.
Metabolismo
Estudios in vitro e in vivo indicaron que el palbociclib se somete a metabolismo hepático en humanos. Después de la administración oral de una dosis única de 125 mg de [14C]palbociclib a humanos, las vías metabólicas principales para el palbociclib incluyeron la oxidación y la sulfonación, con la acilación y la glucuronidación contribuyendo como vías menores. El palbociclib fue la principal entidad derivada del fármaco circulante en plasma (23%). El principal metabolito circulante fue un conjugado glucurónido de palbociclib, aunque solo representó el 1,5% de la dosis administrada en los excrementos. El palbociclib se metabolizó extensamente, con el fármaco sin cambios representando el 2,3% y el 6,9% de la radiactividad en las heces y la orina, respectivamente. En las heces, el conjugado de ácido sulfámico de palbociclib fue el principal componente relacionado con el fármaco, representando el 26% de la dosis administrada. Los estudios in vitro con hepatocitos humanos, fracciones citosólicas y S9 del hígado y enzimas SULT recombinantes indicaron que CYP3A y SULT2A1 participan principalmente en el metabolismo del palbociclib.
Eliminación
La media geométrica del aclaramiento oral aparente (CL/F) del palbociclib fue de 63,1 L/h (29% CV), y la vida media de eliminación plasmática media (± desviación estándar) fue de 29 (±5) horas en pacientes con cáncer de mama avanzado. En 6 sujetos masculinos sanos a los que se administró una dosis oral única de [14C]palbociclib, se recuperó una mediana del 91,6% de la dosis radiactiva total administrada en 15 días; las heces (74,1% de la dosis) fueron la principal vía de excreción, con el 17,5% de la dosis recuperada en la orina. La mayor parte del material se excretó como metabolitos.
Edad, sexo y peso corporal
Según un análisis farmacocinético poblacional en 183 pacientes con cáncer (50 pacientes masculinos y 133 pacientes femeninos, rango de edad de 22 a 89 años y rango de peso corporal de 37,9 a 123 kg), el sexo no tuvo ningún efecto en la exposición al palbociclib, y la edad y el peso corporal no tuvieron ningún efecto clínicamente importante en la exposición al palbociclib.
Insuficiencia hepática
Los datos de un ensayo farmacocinético en sujetos con diferentes grados de insuficiencia hepática indican que el AUCINF no unido al palbociclib disminuyó un 17% en sujetos con insuficiencia hepática leve (clase A de Child-Pugh) y aumentó en un 34% y un 77% en sujetos con insuficiencia hepática moderada (clase B de Child-Pugh) y grave (clase C de Child-Pugh), respectivamente, en relación con los sujetos con función hepática normal. La Cmax no unida al palbociclib aumentó en un 7%, 38% y 72% para la insuficiencia hepática leve, moderada y grave, respectivamente, en relación con los sujetos con función hepática normal. Además, según un análisis farmacocinético poblacional que incluyó 183 pacientes, donde 40 pacientes tuvieron insuficiencia hepática leve según la clasificación del Instituto Nacional del Cáncer (NCI) (bilirrubina total ≤ ULN y AST > ULN, o bilirrubina total >1,0 a 1,5 × ULN y cualquier AST), la insuficiencia hepática leve no tuvo ningún efecto en la exposición al palbociclib, lo que respalda aún más los hallazgos del estudio dedicado a la insuficiencia hepática.
Insuficiencia renal
Los datos de un ensayo farmacocinético en sujetos con diferentes grados de insuficiencia renal indican que el AUCINF del palbociclib aumentó en un 39%, 42% y 31% con insuficiencia renal leve (60 mL/min ≤ CrCl < 90 mL/min), moderada (30 mL/min ≤ CrCl <60 mL/min) y grave (CrCl <30 mL/min), respectivamente, en relación con los sujetos con función renal normal. La exposición máxima al palbociclib (Cmax) aumentó en un 17%, 12% y 15% para la insuficiencia renal leve, moderada y grave, respectivamente, en relación con los sujetos con función renal normal. Además, según un análisis farmacocinético poblacional que incluyó 183 pacientes, donde 73 pacientes tuvieron insuficiencia renal leve y 29 pacientes tuvieron insuficiencia renal moderada, la insuficiencia renal leve y moderada no tuvo ningún efecto en la exposición al palbociclib. La farmacocinética del palbociclib no se ha estudiado en pacientes que requieren hemodiálisis.
Interacciones medicamentosas
Los datos in vitro indican que la enzima CYP3A y la enzima SULT SULT2A1 participan principalmente en el metabolismo del palbociclib. El palbociclib es un inhibidor débil dependiente del tiempo de CYP3A después de la administración diaria de 125 mg hasta alcanzar el estado estacionario en humanos. In vitro, el palbociclib no es un inhibidor de CYP1A2, 2A6, 2B6, 2C8, 2C9, 2C19 y 2D6, y no es un inductor de CYP1A2, 2B6, 2C8 y 3A4 a concentraciones clínicamente relevantes.
Inhibidores de CYP3A: Los datos de un ensayo de interacción farmacológica en sujetos sanos (N=12) indican que la administración conjunta de múltiples dosis diarias de 200 mg de itraconazol con una dosis única de 125 mg de IBRANCE aumentó el AUCINF y la Cmax del palbociclib en aproximadamente un 87% y un 34%, respectivamente, en relación con una dosis única de 125 mg de IBRANCE administrada sola [ver Interacciones medicamentosas (7.1)].
Inductores del CYP3A: Los datos de un ensayo de interacción farmacológica en sujetos sanos (N=15) indican que la administración conjunta de múltiples dosis diarias de 600 mg de rifampicina, un inductor potente del CYP3A, con una dosis única de 125 mg de IBRANCE redujo el AUCINF y la Cmax de palbociclib en un 85% y un 70%, respectivamente, en relación con una dosis única de 125 mg de IBRANCE administrada sola. Los datos de un ensayo de interacción farmacológica en sujetos sanos (N=14) indican que la administración conjunta de múltiples dosis diarias de 400 mg de modafinilo, un inductor moderado del CYP3A, con una dosis única de 125 mg de IBRANCE redujo el AUCINF y la Cmax de palbociclib en un 32% y un 11%, respectivamente, en relación con una dosis única de 125 mg de IBRANCE administrada sola [ver Interacciones farmacológicas (7.2)].
Sustratos del CYP3A: Palbociclib es un inhibidor débil dependiente del tiempo del CYP3A después de la administración diaria de 125 mg hasta alcanzar el estado estacionario en humanos. En un ensayo de interacción farmacológica en sujetos sanos (N=26), la administración conjunta de midazolam con múltiples dosis de IBRANCE aumentó los valores de AUCINF y Cmax de midazolam en un 61% y un 37%, respectivamente, en comparación con la administración de midazolam solo [ver Interacciones farmacológicas (7.3)].
Medicamentos que aumentan el pH gástrico: En un ensayo de interacción farmacológica en sujetos sanos, la administración conjunta de una dosis única de 125 mg de IBRANCE con múltiples dosis del inhibidor de la bomba de protones (IBP) rabeprazol en condiciones de alimentación redujo la Cmax de palbociclib en un 41%, pero tuvo un impacto limitado en el AUCINF (disminución del 13%), en comparación con una dosis única de IBRANCE administrada sola. Dado el efecto reducido en el pH gástrico de los antagonistas de los receptores H2 y los antiácidos locales en comparación con los IBP, se espera que el efecto de estas clases de agentes reductores de ácido en la exposición a palbociclib en condiciones de alimentación sea mínimo. En condiciones de alimentación, no hay un efecto clínicamente relevante de los IBP, los antagonistas de los receptores H2 o los antiácidos locales en la exposición a palbociclib. En otro estudio en sujetos sanos, la administración conjunta de una dosis única de IBRANCE con múltiples dosis del IBP rabeprazol en ayunas redujo el AUCINF y la Cmax de palbociclib en un 62% y un 80%, respectivamente, en comparación con una dosis única de IBRANCE administrada sola.
Letrozol: Los datos de un ensayo clínico en pacientes con cáncer de mama mostraron que no hubo interacción farmacológica entre palbociclib y letrozol cuando se administraron conjuntamente los 2 fármacos.
Fulvestrant: Los datos de un ensayo clínico en pacientes con cáncer de mama mostraron que no hubo interacción farmacológica clínicamente relevante entre palbociclib y fulvestrant cuando se administraron conjuntamente los 2 fármacos.
Goserelina: Los datos de un ensayo clínico en pacientes con cáncer de mama mostraron que no hubo interacción farmacológica clínicamente relevante entre palbociclib y goserelina cuando se administraron conjuntamente los 2 fármacos.
Anastrozol o Exemestano: No hay datos clínicos disponibles para evaluar las interacciones farmacológicas entre anastrozol o exemestano y palbociclib. No se espera una interacción farmacológica clínicamente significativa entre anastrozol o exemestano y palbociclib basándose en análisis de los efectos de anastrozol, exemestano y palbociclib sobre o por vías metabólicas o sistemas de transporte.
Efecto de Palbociclib sobre los transportadores: Las evaluaciones in vitro indicaron que palbociclib tiene un bajo potencial para inhibir las actividades de los transportadores de fármacos transportador de aniones orgánicos (OAT)1, OAT3, transportador de cationes orgánicos (OCT)2 y polipéptido transportador de aniones orgánicos (OATP)1B1, OATP1B3 a concentraciones clínicamente relevantes. In vitro, palbociclib tiene el potencial de inhibir OCT1 a concentraciones clínicamente relevantes, así como el potencial de inhibir la glicoproteína P (P-gp) o la proteína de resistencia al cáncer de mama (BCRP) en el tracto gastrointestinal a la dosis propuesta.
13 TOXICOLOGÍA NO CLÍNICA
13.1 Carcinogenicidad, Mutagénesis, Deterioro de la Fertilidad
Se evaluó la carcinogenicidad de palbociclib en un estudio de 6 meses en ratones transgénicos y en un estudio de 2 años en ratas. La administración oral de palbociclib durante 2 años provocó un aumento en la incidencia de tumores de células microgliales en el sistema nervioso central de ratas macho a una dosis de 30 mg/kg/día (aproximadamente 8 veces la exposición clínica humana basada en el AUC). No hubo hallazgos neoplásicos en ratas hembra a dosis de hasta 200 mg/kg/día (aproximadamente 5 veces la exposición clínica humana basada en el AUC). La administración oral de palbociclib a ratones transgénicos rasH2 machos y hembras durante 6 meses no provocó un aumento en la incidencia de neoplasias a dosis de hasta 60 mg/kg/día.
Palbociclib fue aneugénico en células de ovario de hámster chino in vitro y en la médula ósea de ratas macho a dosis ≥100 mg/kg/día durante 3 semanas. Palbociclib no fue mutagénico en una prueba in vitro de mutación inversa bacteriana (Ames) y no fue clastogénico en la prueba in vitro de aberración cromosómica en linfocitos humanos.
En un estudio de fertilidad en ratas hembra, palbociclib no afectó el apareamiento ni la fertilidad a ninguna dosis de hasta 300 mg/kg/día (aproximadamente 4 veces la exposición clínica humana basada en el AUC) y no se observaron efectos adversos en los tejidos reproductivos femeninos en estudios de toxicidad con dosis repetidas de hasta 300 mg/kg/día en ratas y 3 mg/kg/día en perros (aproximadamente 6 veces y similar a la exposición humana [AUC], a la dosis recomendada, respectivamente).
Los efectos adversos de palbociclib sobre la función y la fertilidad reproductivas masculinas se observaron en los estudios de toxicología con dosis repetidas en ratas y perros y en un estudio de fertilidad masculina en ratas. En los estudios de toxicología con dosis repetidas, los hallazgos relacionados con palbociclib en el testículo, el epidídimo, la próstata y la vesícula seminal a ≥30 mg/kg/día en ratas y ≥0,2 mg/kg/día en perros incluyeron disminución del peso orgánico, atrofia o degeneración, hipospermia, desechos celulares intratubulares y disminución de la secreción. Se observó una reversibilidad parcial de los efectos en los órganos reproductivos masculinos en ratas y perros después de un período de 4 y 12 semanas sin dosificación, respectivamente. Estas dosis en ratas y perros dieron como resultado aproximadamente ≥10 y 0,1 veces, respectivamente, la exposición [AUC] en humanos a la dosis recomendada. En el estudio de fertilidad y desarrollo embrionario temprano en ratas macho, palbociclib no causó efectos en el apareamiento, pero provocó una ligera disminución de la fertilidad asociada con una menor motilidad y densidad de espermatozoides a 100 mg/kg/día con niveles de exposición proyectados [AUC] de 20 veces la exposición en humanos a la dosis recomendada.
14 ESTUDIOS CLÍNICOS
PALOMA-2: IBRANCE más Letrozole
Pacientes con cáncer de mama avanzado o metastásico, ER-positivo y HER2-negativo para terapia endocrina inicial
PALOMA-2 fue un estudio internacional, aleatorizado, doble ciego, de grupos paralelos y multicéntrico de IBRANCE más letrozole versus placebo más letrozole realizado en mujeres posmenopáusicas con cáncer de mama avanzado ER-positivo y HER2-negativo que no habían recibido tratamiento sistémico previo para su enfermedad avanzada. Se aleatorizó un total de 666 pacientes en una proporción de 2:1 a IBRANCE más letrozole o placebo más letrozole. La aleatorización se estratificó por localización de la enfermedad (visceral versus no visceral), intervalo libre de enfermedad (metástasis de novo versus ≤12 meses desde el final del tratamiento adyuvante hasta la recurrencia de la enfermedad versus >12 meses desde el final del tratamiento adyuvante hasta la recurrencia de la enfermedad), y naturaleza de las terapias anticancerosas (neo)adyuvantes previas (terapias hormonales previas versus ninguna terapia hormonal previa). IBRANCE se administró por vía oral a una dosis de 125 mg diarios durante 21 días consecutivos seguidos de 7 días sin tratamiento. Los pacientes recibieron el tratamiento del estudio hasta la progresión objetiva de la enfermedad, el deterioro sintomático, la toxicidad inaceptable, la muerte o la retirada del consentimiento, lo que ocurriera primero. El principal resultado de eficacia del estudio fue la supervivencia libre de progresión (SLP) evaluada por el investigador según los Criterios de Evaluación de la Respuesta en Tumores Sólidos versión 1.1 (RECIST). Las medidas adicionales de resultado de eficacia fueron la tasa de respuesta global (TRG) confirmada, según la evaluación del investigador de acuerdo con RECIST versión 1.1 y la supervivencia global (SG).
Las pacientes incluidas en este estudio tenían una mediana de edad de 62 años (rango de 28 a 89). La mayoría de las pacientes eran blancas (78%), y la mayoría de las pacientes tenían un estado de rendimiento (EP) del Eastern Cooperative Oncology Group (ECOG) de 0 o 1 (98%). El cuarenta y ocho por ciento de las pacientes habían recibido quimioterapia y el 56% habían recibido terapia antihormonal en el contexto neoadyuvante o adyuvante antes del diagnóstico de cáncer de mama avanzado. El treinta y siete por ciento de las pacientes no habían recibido terapia sistémica previa en el contexto neoadyuvante o adyuvante. La mayoría de las pacientes (97%) tenían enfermedad metastásica. El veintitrés por ciento de las pacientes tenían enfermedad únicamente ósea, y el 49% de las pacientes tenían enfermedad visceral.
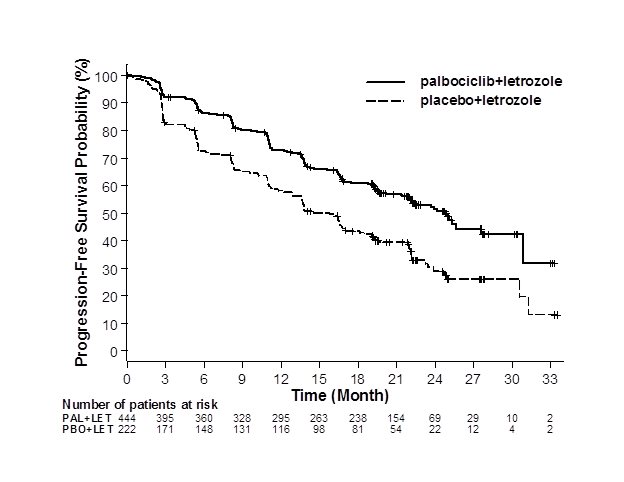
Los principales resultados de eficacia de PALOMA-2 se resumen en la Tabla 8 y la Figura 1. Se observaron resultados consistentes en los subgrupos de pacientes de intervalo libre de enfermedad (ILE), localización de la enfermedad y terapia previa. El efecto del tratamiento de la combinación sobre la SLP también fue apoyado por una revisión independiente de las radiografías. Basándose en el análisis de SG final preespecificado realizado después de 435 eventos, la SG no fue estadísticamente significativa.
| IBRANCE más Letrozole | Placebo más Letrozole | |
|---|---|---|
| IC=intervalo de confianza; ITT=Intención de tratar; N=número de pacientes; NE=no estimable; SG=supervivencia global; SLP=supervivencia libre de progresión. | ||
|
Supervivencia libre de progresión para ITT (evaluación del investigador) |
N=444 |
N=222 |
|
Número de eventos de SLP (%) |
194 (43,7) |
137 (61,7) |
|
Mediana de supervivencia libre de progresión (meses, IC del 95%) |
24,8 (22,1, NE) |
14,5 (12,9, 17,1) |
|
Razón de riesgo (IC del 95%) y valor p |
||
|
Respuesta objetiva para pacientes con enfermedad medible (evaluación del investigador) |
N=338 |
N=171 |
|
Tasa de respuesta objetiva‡ (%, IC del 95%) |
55,3 (49,9, 60,7) |
44,4 (36,9, 52,2) |
|
Supervivencia general para ITT |
N=444 |
N=222 |
|
Número de eventos de SG (%) |
287 (64.6) |
148 (66.7) |
|
SG mediana (meses, IC del 95%) |
53.8 (49.8, 59.2) |
49.8 (42.3, 56.4) |
|
Razón de riesgo (IC del 95%) y valor p |
||
PALOMA-3: IBRANCE más Fulvestrant
Pacientes con cáncer de mama avanzado o metastásico, HR-positivo y HER2-negativo que han presentado progresión de la enfermedad durante o después de una terapia endocrina adyuvante o metastásica previa
PALOMA-3 fue un estudio internacional, aleatorizado, doble ciego, de grupos paralelos y multicéntrico de IBRANCE más fulvestrant versus placebo más fulvestrant realizado en mujeres con cáncer de mama avanzado HR-positivo y HER2-negativo, independientemente de su estado menopáusico, cuya enfermedad progresó durante o después de una terapia endocrina previa. Un total de 521 mujeres pre/posmenopáusicas fueron aleatorizadas en una proporción de 2:1 a IBRANCE más fulvestrant o placebo más fulvestrant y estratificadas por sensibilidad documentada a la terapia hormonal previa, estado menopáusico al inicio del estudio (pre/perimenopáusica versus posmenopáusica) y presencia de metástasis visceral. IBRANCE se administró por vía oral a una dosis de 125 mg diarios durante 21 días consecutivos seguidos de 7 días sin tratamiento. Las mujeres pre/perimenopáusicas fueron incluidas en el estudio y recibieron el agonista de LHRH goserelina durante al menos 4 semanas antes y durante la duración de PALOMA-3. Las pacientes continuaron recibiendo el tratamiento asignado hasta la progresión objetiva de la enfermedad, el deterioro sintomático, la toxicidad inaceptable, la muerte o la retirada del consentimiento, lo que ocurriera primero. El principal resultado de eficacia del estudio fue la supervivencia libre de progresión (SLP) evaluada por el investigador según RECIST 1.1.
Las pacientes incluidas en este estudio tenían una mediana de edad de 57 años (rango de 29 a 88). La mayoría de las pacientes del estudio eran de raza blanca (74%), todas las pacientes tenían una puntuación de PS ECOG de 0 o 1, y el 80% eran posmenopáusicas. Todas las pacientes habían recibido terapia sistémica previa, y el 75% de las pacientes habían recibido un régimen de quimioterapia previo. El veinticinco por ciento de las pacientes no habían recibido terapia previa en el contexto de enfermedad metastásica, el 60% tenían metástasis visceral y el 23% tenían enfermedad únicamente ósea.
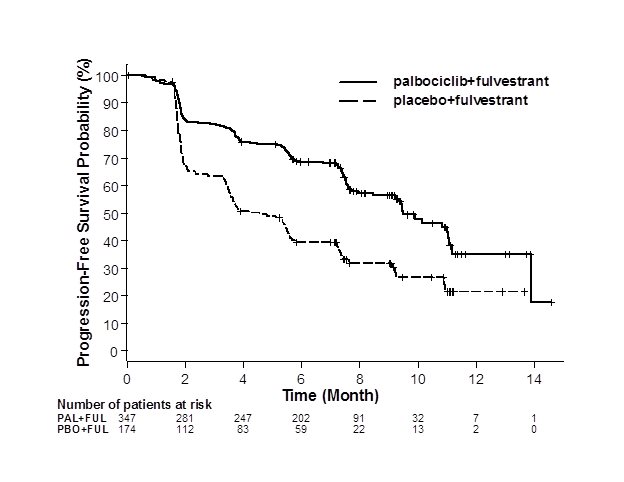
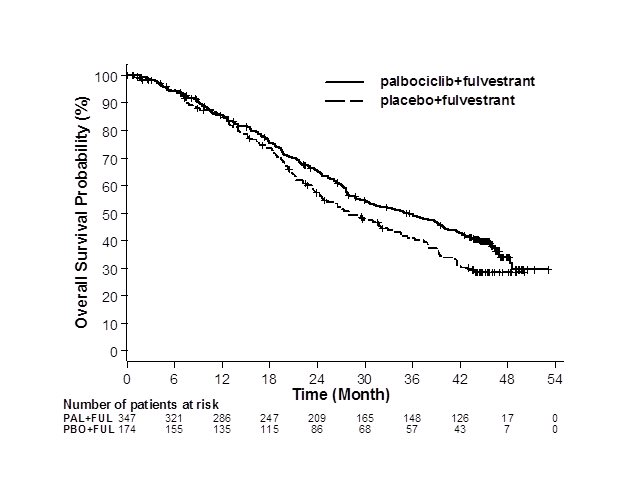
Los resultados de la SLP evaluada por el investigador y la supervivencia general (SG) final de PALOMA-3 se resumen en la Tabla 9. Las gráficas de Kaplan-Meier correspondientes se muestran en las Figuras 2 y 3, respectivamente. Se observaron resultados de SLP consistentes en los subgrupos de pacientes según el sitio de la enfermedad, la sensibilidad a la terapia hormonal previa y el estado menopáusico. Después de un tiempo de seguimiento mediano de 45 meses, los resultados de SG finales no fueron estadísticamente significativos.
| IBRANCE más Fulvestrant | Placebo más Fulvestrant | |
|---|---|---|
| IC=intervalo de confianza; ITT=Intención de tratar; N=número de pacientes; SG=supervivencia general; SLP=supervivencia libre de progresión. | ||
|
||
|
Supervivencia libre de progresión para ITT |
N=347 |
N=174 |
|
Número de eventos de SLP (%) |
145 (41.8) |
114 (65.5) |
|
SLP mediana (meses, IC del 95%) |
9.5 (9.2, 11.0) |
4.6 (3.5, 5.6) |
|
Razón de riesgo (IC del 95%) y valor p |
0.461 (0.360, 0.591), p<0.0001 |
|
|
Respuesta objetiva para pacientes con enfermedad medible |
N=267 |
N=138 |
|
Tasa de respuesta objetiva* (%, IC del 95%) |
24.6 (19.6, 30.2) |
10.9 (6.2, 17.3) |
|
Supervivencia general para ITT |
N=347 |
N=174 |
|
Número de eventos de SG (%) |
201 (57.9) |
109 (62.6) |
|
Supervivencia mediana (meses, IC del 95%) |
34.9 (28.8, 40.0) |
28.0 (23.6, 34.6) |
|
Hazard ratio (IC del 95%) y valor p |
||
16 SUMINISTRO/ALMACENAMIENTO Y MANIPULACIÓN
IBRANCE se suministra en las siguientes concentraciones y configuraciones de envases:
| Cápsulas de IBRANCE | |||
|---|---|---|---|
| Configuración del envase | Concentración de la cápsula (mg) | NDC | Descripción de la cápsula |
|
Frascos de 21 cápsulas |
125 |
NDC 0069-0189-21 |
cápsulas de gelatina dura, opacas, tamaño 0, con tapa y cuerpo color caramelo, impresas con tinta blanca “Pfizer” en la tapa, “PBC 125” en el cuerpo |
|
Frascos de 21 cápsulas |
100 |
NDC 0069-0188-21 |
cápsulas de gelatina dura, opacas, tamaño 1, con tapa color caramelo y cuerpo color naranja claro, impresas con tinta blanca “Pfizer” en la tapa, “PBC 100” en el cuerpo |
|
Frascos de 21 cápsulas |
75 |
NDC 0069-0187-21 |
cápsulas de gelatina dura, opacas, tamaño 2, con tapa y cuerpo color naranja claro, impresas con tinta blanca “Pfizer” en la tapa, “PBC 75” en el cuerpo |
Consérvese a 20 °C a 25 °C (68 °F a 77 °F); se permiten excursiones entre 15 °C a 30 °C (59 °F a 86 °F) [véase Temperatura ambiente controlada USP].
17 INFORMACIÓN DE ASESORAMIENTO AL PACIENTE
Aconseje al paciente que lea el etiquetado del paciente aprobado por la FDA (Información para el paciente).
Mielosupresión/Infección
- •
- Aconseje a los pacientes que informen inmediatamente cualquier signo o síntoma de mielosupresión o infección, como fiebre, escalofríos, mareos, dificultad para respirar, debilidad o cualquier aumento de la tendencia a sangrar y/o a formar hematomas [ver Advertencias y precauciones (5.1)].
Enfermedad pulmonar intersticial/Neumonitis
- •
- Aconseje a los pacientes que informen inmediatamente sobre cualquier síntoma respiratorio nuevo o que empeore [ver Advertencias y precauciones (5.2)].
Interacciones medicamentosas
- •
- El pomelo puede interactuar con IBRANCE. Los pacientes no deben consumir productos de pomelo mientras estén en tratamiento con IBRANCE.
- •
- Informe a los pacientes que eviten los inhibidores potentes del CYP3A y los inductores potentes del CYP3A.
- •
- Aconseje a los pacientes que informen a sus proveedores de atención médica sobre todos los medicamentos concomitantes, incluidos los medicamentos recetados, los medicamentos de venta libre, las vitaminas y los productos herbales [ver Interacciones medicamentosas (7)].
Dosis y administración
- •
- Aconseje a los pacientes que tomen IBRANCE con alimentos.
- •
- Si el paciente vomita u olvida una dosis, no debe tomar una dosis adicional. La siguiente dosis prescrita debe tomarse a la hora habitual. Las cápsulas de IBRANCE deben tragarse enteras (no las mastique, triture ni abra antes de tragarlas). No se debe ingerir ninguna cápsula si está rota, agrietada o de alguna manera no intacta.
- •
- Las mujeres pre/perimenopáusicas tratadas con IBRANCE también deben ser tratadas con agonistas de LHRH [ver Dosis y administración (2.1)].
Embarazo, lactancia e infertilidad
- •
- Toxicidad embriofetal
- o
- Aconseje a las mujeres en edad fértil sobre el riesgo potencial para el feto y que utilicen un método anticonceptivo eficaz durante el tratamiento con IBRANCE y durante al menos 3 semanas después de la última dosis. Aconseje a las mujeres que informen a su proveedor de atención médica sobre un embarazo conocido o sospechoso [ver Advertencias y precauciones (5.3) y Uso en poblaciones específicas (8.1 y 8.3)].
- o
- Aconseje a los pacientes varones con parejas femeninas en edad fértil que utilicen un método anticonceptivo eficaz durante el tratamiento con IBRANCE y durante al menos 3 meses después de la última dosis [ver Uso en poblaciones específicas (8.3)].
- •
- Lactancia: Aconseje a las mujeres que no deben amamantar durante el tratamiento con IBRANCE y durante 3 semanas después de la última dosis [ver Uso en poblaciones específicas (8.2)].
- •
- Infertilidad: Informe a los varones en edad fértil que IBRANCE puede causar infertilidad y que consideren la preservación de esperma antes de tomar IBRANCE [ver Uso en poblaciones específicas (8.3)].
SECCIÓN NO CLASIFICADA DE SPL
El etiquetado de este producto puede haber sido actualizado. Para obtener información completa de prescripción, visite www.pfizer.com. Para obtener información médica sobre IBRANCE, visite www.pfizermedinfo.com o llame al 1-800-438-1985.
LAB-0723-11.0
PROSPECTO PARA EL PACIENTE
| Esta información para el paciente ha sido aprobada por la Administración de Alimentos y Medicamentos de los EE. UU. Revisado: diciembre de 2024 | ||
|
INFORMACIÓN PARA EL PACIENTE |
||
|
¿Cuál es la información más importante que debo saber sobre IBRANCE? IBRANCE puede causar efectos secundarios graves, incluyendo: Recuentos bajos de glóbulos blancos (neutropenia). Los recuentos bajos de glóbulos blancos son muy comunes al tomar IBRANCE y pueden causar infecciones graves que pueden provocar la muerte. Su proveedor de atención médica debe controlar sus recuentos de glóbulos blancos antes y durante el tratamiento. Si desarrolla recuentos bajos de glóbulos blancos durante el tratamiento con IBRANCE, su proveedor de atención médica puede detener su tratamiento, disminuir su dosis o puede indicarle que espere para comenzar su ciclo de tratamiento. Informe a su proveedor de atención médica de inmediato si tiene signos y síntomas de recuentos bajos de glóbulos blancos o infecciones como fiebre y escalofríos. Problemas pulmonares (neumonitis). IBRANCE puede causar inflamación grave o potencialmente mortal de los pulmones durante el tratamiento que puede provocar la muerte. Informe a su proveedor de atención médica de inmediato si tiene algún síntoma nuevo o que empeora, incluyendo:
Su proveedor de atención médica puede interrumpir o detener completamente el tratamiento con IBRANCE si sus síntomas son graves. Consulte “¿Cuáles son los posibles efectos secundarios de IBRANCE?” para obtener más información sobre los efectos secundarios. |
||
|
¿Qué es IBRANCE? IBRANCE es un medicamento recetado que se usa en adultos para tratar el cáncer de mama positivo para el receptor hormonal (HR) y negativo para el receptor 2 del factor de crecimiento epidérmico humano (HER2) que se ha diseminado a otras partes del cuerpo (metástasis) en combinación con:
No se sabe si IBRANCE es seguro y eficaz en niños. |
||
|
¿Qué debo decirle a mi proveedor de atención médica antes de tomar IBRANCE? Antes de tomar IBRANCE, informe a su proveedor de atención médica sobre todas sus afecciones médicas, incluso si:
Informe a su proveedor de atención médica sobre todos los medicamentos que toma, incluidos los medicamentos recetados y de venta libre, las vitaminas y los suplementos herbales. IBRANCE y otros medicamentos pueden afectarse mutuamente causando efectos secundarios. Conozca los medicamentos que toma. Mantenga una lista de ellos para mostrársela a su proveedor de atención médica o farmacéutico cuando reciba un medicamento nuevo. |
||
|
¿Cómo debo tomar IBRANCE?
|
||
|
¿Cuáles son los posibles efectos secundarios de IBRANCE? IBRANCE puede causar efectos secundarios graves. Consulte “¿Cuál es la información más importante que debo saber sobre IBRANCE?“ Los efectos secundarios más comunes de IBRANCE cuando se usa con letrozol o fulvestrant incluyen:
|
- o
- mareos
- o
- falta de aliento
- o
- debilidad
- o
- sangrado o formación de hematomas con mayor facilidad
- o
- epistaxis
- •
- infecciones (ver “¿Cuál es la información más importante que debo saber sobre IBRANCE?”)
- •
- cansancio
- •
- náuseas
- •
- dolor de boca
- •
- anormalidades en las pruebas de función hepática
- •
- diarrea
- •
- adelgazamiento o pérdida del cabello
- •
- vómitos
- •
- sarpullido
- •
- pérdida de apetito
IBRANCE puede causar problemas de fertilidad en los hombres. Esto puede afectar su capacidad para engendrar un hijo. Hable con su proveedor de atención médica sobre las opciones de planificación familiar antes de comenzar a tomar IBRANCE si esto le preocupa.
Informe a su proveedor de atención médica si tiene algún efecto secundario que le moleste o que no desaparezca.
Estos no son todos los posibles efectos secundarios de IBRANCE.
Llame a su médico para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
¿Cómo debo almacenar IBRANCE?
- •
- Almacene IBRANCE a una temperatura de 20 °C a 25 °C (68 °F a 77 °F).
Mantenga IBRANCE y todos los medicamentos fuera del alcance de los niños.
Información general sobre el uso seguro y eficaz de IBRANCE
A veces, los medicamentos se recetan para fines distintos de los que se indican en un prospecto de información para el paciente. No use IBRANCE para una afección para la que no se lo recetaron. No le dé IBRANCE a otras personas, incluso si tienen los mismos síntomas que usted. Podría causarles daño.
Puede pedirle a su farmacéutico o proveedor de atención médica más información sobre IBRANCE que esté escrita para profesionales de la salud.
¿Cuáles son los ingredientes de IBRANCE?
Principio activo: palbociclib
Ingredientes inactivos: celulosa microcristalina, lactosa monohidrato, glicolato de almidón sódico, dióxido de silicio coloidal, estearato de magnesio y cápsulas de gelatina dura.
Las cubiertas de las cápsulas opacas de color naranja claro, naranja claro/caramelo y caramelo contienen: gelatina, óxido de hierro rojo, óxido de hierro amarillo y dióxido de titanio.
La tinta de impresión contiene: goma laca, dióxido de titanio, hidróxido de amonio, propilenglicol y simeticona.
El etiquetado de este producto puede haberse actualizado. Para obtener la información de prescripción más reciente, visite www.pfizer.com.
LAB-0724-8.0
Para obtener más información, visite www.pfizer.com o llame al 1-800-438-1985.
PRINCIPAL PANEL DE PRESENTACIÓN – Botella de cápsulas de 75 mg
NDC 0069-0187-21
Pfizer
Ibrance®
(palbociclib)
capsules
75 mg
21 Cápsulas
Rx solamente
PRINCIPAL PANEL DE PRESENTACIÓN – Botella de cápsulas de 100 mg
NDC 0069-0188-21
Pfizer
Ibrance®
(palbociclib)
cápsulas
100 mg
21 Cápsulas
Rx only
PANEL PRINCIPAL DE EXHIBICIÓN – Etiqueta del frasco de cápsula de 125 mg
NDC 0069-0189-21
Pfizer
Ibrance®
(palbociclib)
capsules
125 mg
21 Cápsulas
Rx solamente