Fabricante de medicamentos: Torrent Pharmaceuticals Limited (Updated: 2024-10-02)
ASPECTOS DESTACADOS DE LA INFORMACIÓN DE PRESCRIPCIÓN
Cápsulas de APREPITANT, para uso oral
Aprobación inicial en EE. UU.: 2003
INDICACIONES Y USO
Aprepitant es un antagonista del receptor de la sustancia P/neuroquinina 1 (NK1).
Las cápsulas de Aprepitant están indicadas
• en combinación con otros agentes antieméticos, en pacientes de 12 años de edad o mayores para la prevención de:
o náuseas y vómitos agudos y tardíos asociados con cursos iniciales y repetidos de quimioterapia anticancerígena altamente emética (HEC), incluida la cisplatino de dosis alta (1.1)
o náuseas y vómitos asociados con cursos iniciales y repetidos de quimioterapia anticancerígena moderadamente emética (MEC) (1.1)
• para la prevención de náuseas y vómitos posoperatorios (PONV) en adultos (1.2)
Limitaciones de uso: (1.3)
• Aprepitant no se ha estudiado para el tratamiento de náuseas y vómitos establecidos.
• No se recomienda la administración crónica continua de aprepitant.
DOSIFICACIÓN Y ADMINISTRACIÓN
Dosis recomendada para la prevención de náuseas y vómitos inducidos por quimioterapia (CINV) (2.1)
•Cápsulas de Aprepitant en adultos y pacientes pediátricos de 12 años de edad o mayores: es de 125 mg el día 1 y 80 mg los días 2 y 3.
• Administrar aprepitant 1 hora antes de la quimioterapia los días 1, 2 y 3. Si no se administra quimioterapia los días 2 y 3, administrar aprepitant por la mañana.
Consulte la información completa de prescripción para las dosis recomendadas de dexametasona concomitante y antagonista 5-HT3 para HEC y MEC.
Dosis recomendada para PONV (2.2)
• Adultos: 40 mg de cápsulas de Aprepitant dentro de las 3 horas previas a la inducción de la anestesia.
Preparación y administración (2.3)
• Las cápsulas de Aprepitant se pueden administrar con o sin alimentos.
• Tragar las cápsulas de aprepitant enteras.
• Para obtener más detalles sobre la preparación, consulte la información completa de prescripción.
FORMAS Y FUERZAS DE DOSIFICACIÓN
Cápsulas de Aprepitant, USP: 40 mg; 80 mg; 125 mg (3).
CONTRAINDICACIONES
ADVERTENCIAS Y PRECAUCIONES
• Interacciones con CYP3A4: Aprepitant es un sustrato, un inhibidor débil a moderado y un inductor de CYP3A4; Consulte la información completa de prescripción para obtener recomendaciones con respecto a las contraindicaciones, el riesgo de reacciones adversas y los ajustes de dosis de aprepitant y los medicamentos concomitantes. (4, 5.1, 7.1, 7.2)
• Warfarina (un sustrato de CYP2C9): Riesgo de disminución del INR del tiempo de protrombina; controlar el INR en el período de 2 semanas, particularmente de 7 a 10 días, después de iniciar aprepitant. (5.2, 7.1)
• Anticonceptivos hormonales: La eficacia de los anticonceptivos puede reducirse durante la administración y durante los 28 días posteriores a la última dosis de aprepitant. Utilice métodos anticonceptivos alternativos o de respaldo efectivos. (5.3, 7.1, 8.3)
REACCIONES ADVERSAS
Las reacciones adversas más comunes (≥3%) son (6.1):
Prevención de náuseas y vómitos inducidos por quimioterapia (CINV)
• Adultos: fatiga, diarrea, astenia, dispepsia, dolor abdominal, hipo, recuento de glóbulos blancos disminuido, deshidratación y aumento de la alanina aminotransferasa.
• Pediatría: neutropenia, dolor de cabeza, diarrea, disminución del apetito, tos, fatiga, disminución de la hemoglobina, mareos e hipo.
PONV
• Adultos: estreñimiento e hipotensión.
Para informar sobre REACCIONES ADVERSAS SOSPECHOSAS, comuníquese con Torrent Pharma Inc. al 1-800-912-9561 o FDA al 1-800-FDA-1088 o www.fda.gov/medwatch
INTERACCIONES MEDICAMENTOSAS
Consulte 17 para obtener INFORMACIÓN PARA EL PACIENTE y la Guía de medicamentos.
Revisado: 6/2022
Tabla de Contenido
INFORMACIÓN COMPLETA DE PRESCRIPCIÓN: CONTENIDO*
1.1 Prevención de Náuseas y Vómitos Inducidos por Quimioterapia (CINV)
1.2 Prevención de Náuseas y Vómitos Postoperatorios (PONV)
1.3 Limitaciones de Uso
2 DOSIFICACIÓN Y ADMINISTRACIÓN
2.1 Prevención de Náuseas y Vómitos Inducidos por Quimioterapia (CINV)
2.2 Prevención de Náuseas y Vómitos Postoperatorios (PONV)
2.3 Instrucciones de Administración
3 FORMAS Y FUERZAS DE DOSIFICACIÓN
4 CONTRAINDICACIONES
5 ADVERTENCIAS Y PRECAUCIONES
5.1 CYP3A4 Clínicamente Significativo
5.2 Disminución del INR con Warfarina Concomitante
5.3 Riesgo de Reducción de la Eficacia de los Anticonceptivos Hormonales
6 REACCIONES ADVERSAS
6.1 Experiencia en Ensayos Clínicos
6.2 Experiencia Postcomercialización
7 INTERACCIONES MEDICAMENTOSAS
7.1 Efecto de Aprepitant en la Farmacocinética de Otros Medicamentos
7.2 Efecto de Otros Medicamentos en la Farmacocinética de Aprepitant
8 USO EN POBLACIONES ESPECÍFICAS
8.1 EMBARAZO
8.2 Lactancia
8.3 Mujeres y Hombres en Potencial Reproductivo
8.4 Uso Pediátrico
8.5 Uso Geriátrico
8.6 Pacientes con Deterioro Renal
8.7 Pacientes con Deterioro Hepático
10 SOBREDOSIS
11 DESCRIPCIÓN
12 FARMACOLOGÍA CLÍNICA
12.1 MECANISMO DE ACCIÓN
12.2 FARMACODINAMIA
12.3 FARMACOCINÉTICA
13 TOXICOLOGÍA NO CLÍNICA
13.1 Carcinogénesis, Mutagénesis, Deterioro de la Fertilidad
14 ESTUDIOS CLÍNICOS
14.1 Prevención de Náuseas y Vómitos Asociados con HEC en Adultos
14.2 Prevención de Náuseas y Vómitos Asociados con MEC en Adultos
14.3 Prevención de Náuseas y Vómitos Asociados con HEC o MEC en Pacientes Pediátricos
14.4 Prevención de PONV en Adultos
16 CÓMO SE SUMINISTRA/ALMACENAMIENTO Y MANEJO
17 INFORMACIÓN PARA EL PACIENTE
- *
- Las secciones o subsecciones omitidas de la información completa de prescripción no están listadas.
1 INDICACIONES Y USO
1.1 Prevención de las náuseas y los vómitos inducidos por la quimioterapia (NVIQ)
Las cápsulas de Aprepitant, en combinación con otros agentes antieméticos, están indicadas en pacientes de 12 años de edad en adelante para la prevención de:
- náuseas y vómitos agudos y retardados asociados con ciclos iniciales y repetidos de quimioterapia contra el cáncer altamente emetógena (HEC), incluida la cisplatina en dosis altas.
- náuseas y vómitos asociados con ciclos iniciales y repetidos de quimioterapia contra el cáncer moderadamente emetógena (MEC).
1.2 Prevención de Náuseas y Vómitos Postoperatorios (PONV)
Las cápsulas de Aprepitant están indicadas en adultos para la prevención de náuseas y vómitos postoperatorios.
1.3 Limitaciones de uso
- Aprepitant no se ha estudiado para el tratamiento de náuseas y vómitos establecidos.
- No se recomienda la administración continua crónica de Aprepitant porque no se ha estudiado y porque el perfil de interacción medicamentosa puede cambiar durante el uso continuo crónico.
2 DOSIS Y ADMINISTRACIÓN
2.1 Prevención de Náuseas y Vómitos Inducidos por Quimioterapia (NVIC)
Adultos y pacientes pediátricos de 12 años de edad o mayores
La dosis oral recomendada de cápsulas de aprepitant, dexametasona y un antagonista 5-HT3 en adultos y pacientes pediátricos de 12 años de edad o mayores que pueden tragar cápsulas orales, para la prevención de náuseas y vómitos asociados con la administración de HEC o MEC se muestra en la Tabla 1 o la Tabla 2, respectivamente.
|
*Administrar cápsulas de aprepitant 1 hora antes del tratamiento de quimioterapia en los Días 1, 2 y 3. Si no se administra quimioterapia en los Días 2 y 3, administrar cápsulas de aprepitant por la mañana. |
||||||
|
†Administrar dexametasona 30 minutos antes del tratamiento de quimioterapia en el Día 1 y por la mañana en los Días 2 a 4. Se recomienda una reducción del 50% de la dosis de dexametasona para tener en cuenta una interacción medicamentosa con aprepitant [ver Farmacología Clínica (12.3)] . |
||||||
| Población | Día 1 | Día 2 | Día 3 | Día 4 | ||
| Aprepitant cápsulas* |
Adultos y Pacientes Pediátricos de 12 años y mayores |
125 mg por vía oral | 80 mg por vía oral | 80 mg por vía oral | ninguno | |
| Dexametasona | Adultos | 12 mg por vía oral | 8 mg por vía oral | 8 mg por vía oral | 8 mg por vía oral | |
| Pacientes Pediátricos de 12 años y mayores |
Si se coadministra un corticosteroide, como dexametasona, administrar el 50% de la dosis recomendada de corticosteroide en los Días 1 a 4 [ver Estudios Clínicos (14.3)].† | |||||
| Antagonista 5-HT3 | Adultos y Pacientes Pediátricos de 12 años y mayores |
Ver seleccionado antagonista 5-HT3 información de prescripción para la dosis recomendada |
ninguno | ninguno | ninguno | |
|
*Administrar cápsulas de aprepitant 1 hora antes del tratamiento de quimioterapia en los días 1, 2 y 3. Si no se administra quimioterapia en los días 2 y 3, administrar las cápsulas de aprepitant por la mañana. |
|||||
|
†Administrar dexametasona 30 minutos antes del tratamiento de quimioterapia en el día 1. Se recomienda una reducción del 50% de la dosis de dexametasona para tener en cuenta una interacción medicamentosa con aprepitant [ver Farmacología clínica (12.3)]. |
|||||
| Población | Día 1 | Día 2 | Día 3 | ||
| Aprepitant cápsulas* |
Adultos y Pacientes pediátricos de 12 años o más |
125 mg por vía oral | 80 mg por vía oral | 80 mg por vía oral | |
| Dexametasona | Adultos | 12 mg por vía oral | ninguno | ninguno | |
| Pediátrico Pacientes de 12 años o más |
Si se coadministra un corticosteroide, como dexametasona, administrar el 50% de la dosis recomendada de corticosteroide en los días 1 a 4 [ver Estudios clínicos (14.3)].† | ||||
| Antagonista 5-HT3 | Adultos y Pacientes pediátricos de 12 años o más |
Ver seleccionado Antagonista 5-HT3 información de prescripción para la dosis recomendada |
ninguno | ninguno | |
2.2 Prevención de náuseas y vómitos posoperatorios (PONV)
La dosis oral recomendada de cápsulas de aprepitant es de 40 mg dentro de las 30 horas previas a la inducción de la anestesia.
2.3 Instrucciones de administración
Las cápsulas de aprepitant se pueden administrar con o sin alimentos
Cápsulas de aprepitant
- Traga las cápsulas enteras
3 FORMAS DE DOSIFICACIÓN Y CONCENTRACIONES
• 40 mg: cuerpo blanco y tapa amarilla con “40 mg” impreso en tinta negra en el cuerpo.
• 80 mg: cuerpo blanco y tapa blanca con “80 mg” impreso en tinta negra en el cuerpo.
• 125 mg: cuerpo blanco y tapa rosa con “125 mg” impreso en tinta negra en el cuerpo.
4 CONTRAINDICACIONES
Aprepitant está contraindicado en pacientes:
• que son hipersensibles a cualquier componente del producto. Se han notificado reacciones de hipersensibilidad, incluidas reacciones anafilácticas [ver Reacciones adversas (6.2)].
• que toman pimozida. La inhibición de CYP3A4 por aprepitant podría provocar concentraciones plasmáticas elevadas de este fármaco, que es un sustrato de CYP3A4, lo que podría provocar reacciones graves o potencialmente mortales, como la prolongación del QT, una reacción adversa conocida de la pimozida [ver Advertencias y precauciones (5.1)].
5 ADVERTENCIAS Y PRECAUCIONES
5.1 Clinically Significant CYP3A4
Aprepitant es un sustrato, un inhibidor de débil a moderado (dependiente de la dosis) y un inductor de CYP3A4.
- El uso de aprepitant con otros fármacos que son sustratos de CYP3A4 puede aumentar la concentración plasmática del fármaco concomitante.
- El uso de pimozida con aprepitant está contraindicado debido al riesgo de aumento significativo de las concentraciones plasmáticas de pimozida, lo que podría provocar una prolongación del intervalo QT, una reacción adversa conocida de la pimozida [ver Contraindicaciones (4)].
- El uso de aprepitant con inhibidores potentes o moderados de CYP3A4 (p. ej., ketoconazol, diltiazem) puede aumentar las concentraciones plasmáticas de aprepitant y aumentar el riesgo de reacciones adversas relacionadas con aprepitant.
- El uso de aprepitant con inductores potentes de CYP3A4 (p. ej., rifampicina) puede reducir las concentraciones plasmáticas de aprepitant y disminuir su eficacia.
Consulte las tablas 10 y 11 para obtener una lista de interacciones medicamentosas potencialmente significativas [ver Interacciones medicamentosas (7.1, 7.2)].
5.2 Disminución del INR con la administración concomitante de warfarina
La administración concomitante de aprepitant con warfarina, un sustrato de CYP2C9, puede provocar una disminución clínicamente significativa del índice internacional normalizado (INR) del tiempo de protrombina [ver Farmacología clínica (12.3)]. Controle el INR en pacientes en tratamiento crónico con warfarina durante las 2 semanas siguientes al inicio del régimen de 3 días de aprepitant con cada ciclo de quimioterapia, especialmente entre los días 7 y 10, o tras la administración de una dosis única de 40 mg de aprepitant para la prevención de las náuseas y los vómitos posoperatorios [ver Interacciones medicamentosas (7.1)].
5.3 Riesgo de eficacia reducida de los anticonceptivos hormonales
Tras la administración concomitante con aprepitant, la eficacia de los anticonceptivos hormonales puede verse reducida durante la administración y durante los 28 días siguientes a la última dosis de aprepitant [ver Farmacología clínica (12.3)]. Se debe aconsejar a las pacientes que utilicen métodos anticonceptivos alternativos o de barrera eficaces durante el tratamiento con aprepitant y durante 1 mes después de la última dosis de aprepitant [ver Interacciones medicamentosas (7.1), Uso en poblaciones específicas (8.3)].
6 REACCIONES ADVERSAS
6.1 Experiencia en ensayos clínicos
Debido a que los ensayos clínicos se llevan a cabo en condiciones muy variables, las tasas de reacciones adversas observadas en los ensayos clínicos de un fármaco no se pueden comparar directamente con las tasas en los ensayos clínicos de otro fármaco y pueden no reflejar las tasas observadas en la práctica clínica. La seguridad general de aprepitant se evaluó en aproximadamente 6.800 individuos.
Reacciones adversas en adultos en la prevención de náuseas y vómitos asociados con HEC y MEC
En 2 ensayos clínicos controlados con activo, doble ciego en pacientes que recibieron quimioterapia altamente emética (HEC) (Estudios 1 y 2), aprepitant en combinación con ondansetron y dexametasona (régimen de aprepitant) se comparó con ondansetron y dexametasona solos (terapia estándar [ver Estudios clínicos (14.1)].
En 2 ensayos clínicos controlados con activo en pacientes que recibieron quimioterapia moderadamente emética (MEC) (Estudios 3 y 4), aprepitant en combinación con ondansetron y dexametasona (régimen de aprepitant) se comparó con ondansetron y dexametasona solos (terapia estándar) [ver Estudios clínicos (14.2)]. La reacción adversa más común reportada en pacientes que recibieron MEC en los Estudios 3 y 4 agrupados fue dispepsia (6% versus 4%).
En estos 4 estudios, hubo 1.412 pacientes tratados con el régimen de aprepitant durante el Ciclo 1 de quimioterapia y 1.099 de estos pacientes continuaron en la extensión de múltiples ciclos por hasta 6 ciclos de quimioterapia. Las reacciones adversas más comunes reportadas en pacientes que recibieron HEC y MEC en los Estudios 1, 2, 3 y 4 agrupados se enumeran en la Tabla 5.
|
*Reportado en ≥3% de los pacientes tratados con el régimen de Aprepitant y con una incidencia mayor que la terapia estándar. † Régimen de Aprepitant |
||
| Aprepitant, ondansetron y dexametasona† (N=1.412) |
Ondansetron y dexametasona‡ (N=1.396) |
|
| fatiga | 13% | 12% |
| diarrea | 9% | 8% |
| astenia | 7% | 6% |
| dispepsia | 7% | 5% |
| dolor abdominal | 6% | 5% |
| hipo | 5% | 3% |
| recuento de glóbulos blancos disminuido | 4% | 3% |
| deshidratación | 3% | 2% |
| alanina aminotransferasa aumentada | 3% | 2% |
En un análisis agrupado de los estudios HEC y MEC, las reacciones adversas menos comunes reportadas en pacientes con el régimen de aprepitant se enumeran en la Tabla 6.
|
* Reportadas en >0.5% de los pacientes tratados con el régimen de aprepitant, a una incidencia mayor que la terapia estándar y no descritas previamente en la Tabla 5. |
|
| Infecciones e Infestaciones | candidiasis oral, faringitis |
| Trastornos de la sangre y del sistema linfático | anemia, neutropenia febril, neutropenia, trombocitopenia |
| Trastornos del metabolismo y la nutrición | disminución del apetito, hipokalemia |
| Trastornos psiquiátricos | ansiedad |
| Trastornos del sistema nervioso | mareos, disgeusia, neuropatía periférica |
| Trastornos cardíacos | palpitaciones |
| Trastornos vasculares | rubor, sofocos |
| Trastornos respiratorios, torácicos y mediastínicos | tos, disnea, dolor orofaríngeo |
| Trastornos gastrointestinales | boca seca, eructos, flatulencia, gastritis, enfermedad por reflujo gastroesofágico, náuseas, vómitos |
| Trastornos de la piel y del tejido subcutáneo | alopecia, hiperhidrosis, erupción cutánea |
| Trastornos musculoesqueléticos y del tejido conjuntivo | dolor musculoesquelético |
| Trastornos generales y condiciones del sitio de administración |
edema periférico, malestar |
| Investigaciones | aumento de la aminotransferasa aspártica, aumento de la fosfatasa alcalina en sangre, disminución del sodio en sangre, aumento de la urea en sangre, proteinuria, disminución del peso |
En un estudio clínico adicional controlado con activo, 1.169 pacientes que recibieron aprepitant y HEC, las reacciones adversas fueron generalmente similares a las observadas en otros estudios de HEC con aprepitant.
En otro estudio de CINV, se informó síndrome de Stevens-Johnson como una reacción adversa grave en un paciente que recibió el régimen de aprepitant con quimioterapia contra el cáncer.
Las reacciones adversas en las extensiones de múltiples ciclos de los estudios HEC y MEC durante hasta 6 ciclos de quimioterapia fueron generalmente similares a las observadas en el Ciclo 1.
Reacciones adversas en pacientes pediátricos de 6 meses a 17 años de edad en la prevención de náuseas yvómitos asociados con HEC o MEC
En un análisis agrupado de 2 ensayos clínicos controlados con activo en pacientes pediátricos de 6 meses a 17 años que recibieron quimioterapia contra el cáncer altamente o moderadamente emetógena (Estudio 5 y un estudio de seguridad, Estudio 6), aprepitant en combinación con ondansetron con o sin dexametasona (régimen de aprepitant) se comparó con ondansetron con o sin dexametasona (régimen de control).
Hubo 184 pacientes tratados con el régimen de aprepitant durante el Ciclo 1 y 215 pacientes recibieron aprepitant de etiqueta abierta durante hasta 9 ciclos adicionales de quimioterapia.
En el Ciclo 1, las reacciones adversas más comunes informadas en pacientes pediátricos tratados con el régimen de aprepitant en los Estudios 5 y 6 agrupados se enumeran en la Tabla 7.
|
* Informado en ≥3% de los pacientes tratados con el régimen de aprepitant y con una incidencia mayor que el régimen de control. |
||
|
‡ Régimen de control |
||
| Aprepitant y ondansetron (N=184) | Ondansetron (N=168) | |
| neutropenia | 13% | 11% |
| dolor de cabeza | 9% | 5% |
| diarrea | 6% | 5% |
| disminución del apetito | 5% | 4% |
| tos | 5% | 3% |
| fatiga | 5% | 2% |
| hemoglobina disminuida | 5% | 4% |
| mareos | 5% | 1% |
| hipo | 4% | 1% |
Cuarenta y nueve pacientes fueron tratados con quimioterapia con ifosfamida en cada brazo. Dos de los pacientes tratados con ifosfamida en el brazo de aprepitant desarrollaron cambios de comportamiento (agitación = 1; comportamiento anormal = 1), mientras que ningún paciente tratado con ifosfamida en el brazo de control desarrolló cambios de comportamiento. Aprepitant tiene el potencial de aumentar la neurotoxicidad mediada por ifosfamida a través de la inducción de CYP3A4 [ver Interacciones medicamentosas (7.1) y Farmacología clínica (12.3)].
Reacciones adversas en pacientes adultos en la prevención de PONV
En 2 estudios clínicos controlados con activo, doble ciego en pacientes que recibieron anestesia general (Estudios 7 y 8), aprepitant 40 mg por vía oral se comparó con ondansetrón 4 mg intravenoso [ver Estudios clínicos (14.4)].
Hubo 564 pacientes tratados con aprepitant y 538 pacientes tratados con ondansetrón.
Las reacciones adversas más comunes reportadas en pacientes tratados con aprepitant para PONV en los Estudios 7 y 8 combinados se enumeran en la Tabla 8.
|
* Reportado en ≥3% de los pacientes tratados con aprepitant 40 mg y con una incidencia mayor que ondansetrón. |
||
| Aprepitant 40 mg (N = 564) |
Ondansetrón (N = 538) | |
| estreñimiento | 9% | 8% |
| hipotensión | 6% | 5% |
En un análisis combinado de estudios de PONV, las reacciones adversas menos comunes reportadas en pacientes tratados con aprepitant se enumeran en la Tabla 9.
|
*Reportado en >0.5% de los pacientes tratados con aprepitant y con una incidencia mayor que ondansetrón |
|
| Infecciones e Infestaciones | infección postoperatoria |
| Trastornos del metabolismo y la nutrición | hipokalemia, hipovolemia |
| Trastornos del sistema nervioso | mareos, hipoestesia, síncope |
| Trastornos cardíacos | bradicardia |
| Trastornos vasculares | hematoma |
| Trastornos respiratorios, torácicos y mediastínicos | disnea, hipoxia, depresión respiratoria |
| Trastornos gastrointestinales | dolor abdominal, boca seca, dispepsia |
| Trastornos de la piel y del tejido subcutáneo | urticaria |
| Trastornos generales y condiciones del sitio de administración | hipotermia |
| Investigaciones | albúmina sanguínea disminuida, bilirrubina aumentada, glucosa sanguínea aumentada, potasio sanguíneo disminuido |
| Lesiones, envenenamiento y complicaciones de procedimientos | hemorragia operatoria, dehiscencia de la herida |
Además, se notificaron dos reacciones adversas graves en estudios clínicos de PONV en pacientes que tomaron una dosis de aprepitant superior a la recomendada: un caso de estreñimiento y un caso de subíleo.
Otros estudios
Angioedema y urticaria se notificaron como reacciones adversas graves en un paciente que recibió aprepitant en un estudio no CINV/no PONV (aprepitant solo está aprobado en las poblaciones CINV y PONV).
6.2 Experiencia postcomercialización
Las siguientes reacciones adversas se han identificado durante el uso posterior a la aprobación de aprepitant. Debido a que estas reacciones se notifican voluntariamente de una población de tamaño incierto, no siempre es posible estimar de manera confiable su frecuencia o establecer una relación causal con la exposición al fármaco.
Trastornos de la piel y del tejido subcutáneo: prurito, erupción cutánea, urticaria, síndrome de Stevens-Johnson/necrólisis epidérmica tóxica.
Trastornos del sistema inmunitario: reacciones de hipersensibilidad, incluidas reacciones anafilácticas [ver Contraindicaciones (4)].
Trastornos del sistema nervioso: neurotoxicidad inducida por ifosfamida notificada después de la coadministración de aprepitant e ifosfamida.
7 INTERACCIONES MEDICAMENTOSAS
7.1 Efecto de Aprepitant en la Farmacocinética de Otros Medicamentos
Aprepitant es un sustrato, un inhibidor de débil a moderado (dependiente de la dosis) y un inductor de CYP3A4. Aprepitant también es un inductor de CYP2C9 [ver Farmacología Clínica (12.3)].
Aprepitant actúa como un inhibidor moderado de CYP3A4 cuando se administra como un régimen de 3 días (125 mg/80 mg/80 mg) y puede aumentar las concentraciones plasmáticas de los medicamentos concomitantes que son sustratos de CYP3A4. Aprepitant actúa como un inhibidor débil cuando se administra como una dosis única de 40 mg y no se ha demostrado que altere las concentraciones plasmáticas de los medicamentos concomitantes que se metabolizan principalmente a través de CYP3A4. Algunos sustratos de CYP3A4 están contraindicados con aprepitant [ver Contraindicaciones (4)]. Puede ser necesario ajustar la dosis de algunos sustratos de CYP3A4 y CYP2C9, como se muestra en la Tabla 10.
| Sustratos de CYP3A4 | |
| Pimozide | |
| Impacto Clínico | Aumento de la exposición a pimozide |
| Intervención | Aprepitant está contraindicado [ver Contraindicaciones (4)] . |
| Benzodiazepinas | |
| Impacto Clínico | El aumento de la exposición a midazolam u otras benzodiazepinas metabolizadas a través de CYP3A4 (alprazolam, triazolam) puede aumentar el riesgo de reacciones adversas [ver Farmacología Clínica (12.3)]. |
| Intervención | Régimen de aprepitant de 3 días
Dosis única de 40 mg de aprepitant
|
| Dexametasona | |
| Impacto Clínico | Aumento de la exposición a dexametasona [ver Farmacología Clínica (12.3)]. |
| Intervención | Régimen de aprepitant de 3 días
Dosis única de 40 mg de aprepitant
|
| Metilprednisolona | |
| Impacto Clínico | Aumento de la exposición a metilprednisolona [ver Farmacología Clínica (12.3)]. |
| Intervención | Régimen de aprepitant de 3 días
Dosis única de 40 mg de aprepitant
|
| Agentes quimioterapéuticos que se metabolizan por CYP3A4 | |
| Impacto Clínico | El aumento de la exposición al agente quimioterapéutico puede aumentar el riesgo de reacciones adversas [ver Farmacología Clínica (12.3)] . |
| Intervención | Vinblastina, vincristina o ifosfamida u otros agentes quimioterapéuticos
Etopósido, vinorelbina, paclitaxel y docetaxel
|
| Anticonceptivos hormonales | |
| Clinical Impact | Disminución de la exposición hormonal durante la administración y durante los 28 días posteriores a la administración de la última dosis de aprepitant [ver Advertencias y precauciones (5.3), Uso en poblaciones específicas (8.3), Farmacología clínica (12.3)] . |
| Intervention | Deben utilizarse métodos anticonceptivos alternativos o de respaldo efectivos (como condones y espermicidas) durante el tratamiento con aprepitant y durante 1 mes después de la última dosis de aprepitant. |
| Examples | píldoras anticonceptivas, parches cutáneos, implantes y ciertos DIU |
| Sustratos de CYP2C9 | |
| Warfarin | |
| Clinical Impact | Disminución de la exposición a la warfarina y disminución del tiempo de protrombina (INR) [ver Advertencias y precauciones (5.2), Farmacología clínica (12.3)] . |
| Intervention | En pacientes en terapia crónica con warfarina, controlar el tiempo de protrombina (INR) en el período de 2 semanas, particularmente a los 7 a 10 días, después del inicio del régimen de aprepitant de 3 días con cada ciclo de quimioterapia, o después de la administración de una sola dosis de 40 mg de aprepitant. |
| Otros | |
| Antagonistas de 5-HT3 | |
| Clinical Impact | Sin cambios en la exposición al antagonista de 5-HT3 [ver Farmacología clínica (12.3)] . |
| Intervention | No se necesita ajuste de dosis |
| Examples | ondansetrón, granisetrón, dolasetrón |
7.2 Efecto de otros medicamentos en la farmacocinética de aprepitant
Aprepitant es un sustrato de CYP3A4 [ver Farmacología clínica (12.3)]. La coadministración de aprepitant con medicamentos que son inhibidores o inductores de CYP3A4 puede resultar en concentraciones plasmáticas aumentadas o disminuidas de aprepitant, respectivamente, como se muestra en la Tabla 11.
| Inhibidores de CYP3A4 moderados a fuertes | |
| Clinical Impact | La exposición significativamente aumentada de aprepitant puede aumentar el riesgo de reacciones adversas asociadas con aprepitant [ver Reacciones adversas (6.1) y Farmacología clínica (12.3)] . |
| Intervention | Evite el uso concomitante de aprepitant |
| Examples | Inhibidor moderado: diltiazem Inhibidores fuertes: |
| Inductores fuertes de CYP3A4 | |
| Clinical Impact | La exposición sustancialmente disminuida de aprepitant en pacientes que toman crónicamente un inductor fuerte de CYP3A4 puede disminuir la eficacia de aprepitant [ver Farmacología clínica (12.3)] . |
| Intervention | Evite el uso concomitante de aprepitant |
| Examples | rifampicina, carbamazepina, fenitoína |
8 USO EN POBLACIONES ESPECÍFICAS
8.1 EMBARAZO
No hay datos suficientes sobre el uso de aprepitant en mujeres embarazadas para informar un riesgo asociado con el fármaco. En estudios de reproducción en animales, no se observaron efectos adversos en el desarrollo en ratas o conejos expuestos durante el período de organogénesis a niveles sistémicos del fármaco (AUC) aproximadamente 1.5 veces la exposición humana adulta en el régimen de aprepitant de 125 mg/80 mg/80 mg [ver Datos].
El riesgo de fondo estimado de defectos de nacimiento mayores y aborto espontáneo para las poblaciones indicadas es desconocido. En la población general de los EE. UU., el riesgo de fondo estimado de defectos de nacimiento mayores y aborto espontáneo en embarazos clínicamente reconocidos es del 2 al 4% y del 15 al 20%, respectivamente.
Datos
Datos de animales
En estudios de desarrollo embrio-fetal en ratas y conejos, se administró aprepitant durante el período de organogénesis a dosis orales de hasta 1,000 mg/kg dos veces al día en ratas y hasta la dosis máxima tolerada de 25 mg/kg/día en conejos. No se observó letalidad embrio-fetal ni malformaciones a ningún nivel de dosis en ninguna de las especies. Las exposiciones (AUC) en ratas embarazadas a 1,000 mg/kg dos veces al día y en conejos embarazadas a 125 mg/kg/día fueron aproximadamente 1.5 veces la exposición adulta en el régimen de aprepitant de 125 mg/80 mg/80 mg. Aprepitant cruza la placenta en ratas y conejos.
8.2 Lactancia
Resumen de Riesgos
No se han realizado estudios de lactancia para evaluar la presencia de aprepitant en la leche materna, los efectos en el lactante amamantado o los efectos en la producción de leche. Aprepitant está presente en la leche de rata. Los beneficios para el desarrollo y la salud de la lactancia materna deben considerarse junto con la necesidad clínica de la madre de aprepitant y cualquier posible efecto adverso en el lactante amamantado por aprepitant o por la condición materna subyacente.
8.3 Mujeres y Hombres en Edad Reproductiva
Tras la administración de aprepitant, la eficacia de los anticonceptivos hormonales puede reducirse. Se debe aconsejar a las mujeres en edad reproductiva que utilizan anticonceptivos hormonales que utilicen un método alternativo eficaz o un método anticonceptivo no hormonal de respaldo (como condones y espermicidas) durante el tratamiento con aprepitant y durante 1 mes después de la última dosis [ver Interacciones medicamentosas (7.1), Farmacología clínica (12.3)].
8.4 Uso Pediátrico
Prevención de Náuseas y Vómitos Asociados con HEC o MEC
La seguridad y eficacia de las cápsulas de aprepitant en pacientes pediátricos de 12 años de edad o mayores para la prevención de náuseas y vómitos agudos y tardíos asociados con cursos iniciales y repetidos de HEC, incluida la cisplatino de dosis alta, y MEC. El uso de aprepitant en estos grupos de edad está respaldado por evidencia de 302 pacientes pediátricos en un estudio clínico aleatorizado, doble ciego, controlado con comparador activo (n=207 pacientes de 6 meses a menos de 12 años, n=95 pacientes de 12 a 17 años). Aprepitant se estudió en combinación con ondansetrón con o sin dexametasona (a discreción del médico) [ver Estudios clínicos (14.3)]. Las reacciones adversas fueron similares a las reportadas en pacientes adultos [ver Reacciones adversas (6.1)].
La seguridad y eficacia de aprepitant para la prevención de náuseas y vómitos asociados con HEC o MEC no se han establecido en pacientes menores de 6 meses.
Prevención de Náuseas y Vómitos Postoperatorios (PONV)
La seguridad y eficacia de aprepitant no se han establecido para la prevención de náuseas y vómitos postoperatorios en pacientes pediátricos.
Estudio en Animales Jóvenes
Se realizó un estudio en ratas jóvenes para evaluar los efectos de aprepitant sobre el crecimiento y el desarrollo neuroconductual y sexual. Las ratas fueron tratadas con dosis orales de hasta la dosis máxima factible de 1,000 mg/kg dos veces al día (proporcionando exposición en ratas macho menor que la exposición a la dosis humana pediátrica recomendada y exposición en ratas hembra equivalente a la exposición humana pediátrica) desde el período postnatal temprano (Día Postnatal 10) hasta el Día Postnatal 58. Se observaron ligeros cambios en el inicio de la maduración sexual en ratas hembras y machos; sin embargo, no hubo efectos en el apareamiento, la fertilidad, la supervivencia embrio-fetal o la histomorfología de los órganos reproductivos. No hubo efectos en las pruebas neuroconductuales de función sensorial, función motora y aprendizaje y memoria.
8.5 Uso Geriátrico
De los 544 pacientes adultos con cáncer tratados con aprepitant en estudios clínicos de CINV, el 31% tenía 65 años o más, mientras que el 5% tenía 75 años o más. De los 1,120 pacientes adultos con cáncer tratados con aprepitant en estudios clínicos de PONV, el 7% tenía 65 años o más, mientras que el 2% tenía 75 años o más. Otra experiencia clínica reportada con aprepitant no ha identificado diferencias en las respuestas entre pacientes ancianos y más jóvenes. En general, se debe tener precaución al dosificar a pacientes ancianos, ya que tienen una mayor frecuencia de disminución de la función hepática, renal o cardíaca y enfermedades concomitantes u otra terapia farmacológica [ver Farmacología clínica (12.3)].
8.6 Pacientes con Insuficiencia Renal
La farmacocinética de aprepitant en pacientes con insuficiencia renal grave y aquellos con enfermedad renal en etapa terminal (ESRD) que requieren hemodiálisis fue similar a la de sujetos sanos con función renal normal. No es necesario ajustar la dosis para pacientes con cualquier grado de insuficiencia renal o para pacientes con ESRD que se someten a hemodiálisis.
8.7 Pacientes con Insuficiencia Hepática
La farmacocinética de aprepitant en pacientes con insuficiencia hepática leve y moderada fue similar a la de sujetos sanos con función hepática normal. No es necesario ajustar la dosis para pacientes con insuficiencia hepática leve a moderada (puntuación de Child-Pugh de 5 a 9). No hay datos clínicos o farmacocinéticos en pacientes con insuficiencia hepática grave (puntuación de Child-Pugh superior a 9). Por lo tanto, puede ser necesaria una monitorización adicional de las reacciones adversas en estos pacientes cuando se administra aprepitant [ver Farmacología clínica (12.3)].
10 SOBREDOSIS
No hay información específica disponible sobre el tratamiento de la sobredosis.
Se reportaron somnolencia y dolor de cabeza en un paciente que ingirió 1,440 mg de aprepitant (aproximadamente 11 veces la dosis única máxima recomendada).
En caso de sobredosis, se debe suspender el aprepitant y se debe proporcionar tratamiento de apoyo general y monitoreo. Debido a la actividad antiemética del aprepitant, la emesis inducida por fármacos puede no ser efectiva en casos de sobredosis de aprepitant.
Aprepitant no se elimina por hemodiálisis.
11 DESCRIPCIÓN
Las cápsulas de aprepitant, USP contienen el ingrediente activo, aprepitant, USP. Aprepitant, USP es un antagonista del receptor de la sustancia P/neuroquinina 1 (NK 1), un agente antiemético, descrito químicamente como 5 – [[(2 R, 3 S) – 2 – [(1 R) – 1 – [3,5 – bis (trifluorometil) fenil] etoxilo] – 3 – (4 – fluorofenil) – 4 – morfolinil] metilo] – 1,2 – dihidro – 3 H – 1,2,4 – triazol – 3ona.
Su fórmula empírica es C23H21F7N4O3, y su fórmula estructural es:
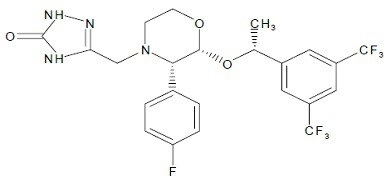
Aprepitant, USP es un polvo blanco a blanquecino, con un peso molecular de 534.43. Es prácticamente insoluble en agua. Aprepitant es poco soluble en alcohol y ligeramente soluble en acetonitrilo.
Cada cápsula de aprepitant para administración oral contiene 40 mg, 80 mg o 125 mg de aprepitant, USP y los siguientes ingredientes inactivos: hipromelosa 2910, poloxámero 407, sacarosa, celulosa microcristalina e tinta de impresión (goma laca, óxido de hierro negro y propilenglicol). Los excipientes de la cápsula son gelatina, dióxido de titanio y sulfato de laurilo de sodio. La cápsula de 40 mg también contiene óxido férrico amarillo, sulfato de laurilo de sodio y dióxido de titanio, la cápsula de 80 mg contiene sulfato de laurilo de sodio y dióxido de titanio y la cápsula de 125 mg contiene óxido férrico rojo, sulfato de laurilo de sodio y dióxido de titanio.
Cumple con la Prueba de Disolución 2 de USP.
12 FARMACOLOGÍA CLÍNICA
12.1 MECANISMO DE ACCIÓN
Aprepitant es un antagonista selectivo de alta afinidad de los receptores humanos de sustancia P/neuroquinina 1 (NK1). Aprepitant tiene poca o ninguna afinidad por los receptores de serotonina (5-HT3), dopamina y corticosteroides, los objetivos de las terapias existentes para las náuseas y los vómitos inducidos por la quimioterapia (CINV) y las náuseas y los vómitos postoperatorios (PONV).
Se ha demostrado en modelos animales que aprepitant inhibe la emesis inducida por agentes quimioterapéuticos citotóxicos, como el cisplatino, a través de acciones centrales. Los estudios de tomografía por emisión de positrones (PET) en animales y humanos con aprepitant han demostrado que cruza la barrera hematoencefálica y ocupa los receptores NK1 del cerebro. Los estudios en animales y humanos muestran que aprepitant aumenta la actividad antiemética del antagonista del receptor 5-HT3 ondansetrón y el corticosteroide dexametasona e inhibe tanto las fases aguda como tardía de la emesis inducida por cisplatino.
12.2 FARMACODINAMIA
En dos estudios de dosis única, múltiples dosis, aleatorizados y controlados con placebo, hombres jóvenes sanos recibieron dosis orales de aprepitant de 10 mg (N=2), 30 mg (N=3), 100 mg (N=3) o 300 mg (N=5) una vez al día (0.08, 0.24, 0.8 y 2.4 veces la dosis única máxima recomendada, respectivamente) durante 14 días con 2 o 3 sujetos en placebo. Se evaluaron tanto la concentración plasmática de aprepitant como la ocupación del receptor NK1 en el cuerpo estriado mediante tomografía por emisión de positrones, antes de la dosis y 24 horas después de la última dosis. A concentraciones plasmáticas de aprepitant de aproximadamente 10 ng/mL y 100 ng/mL, las ocupaciones del receptor NK1 fueron aproximadamente del 50% y el 90%, respectivamente. El régimen de aprepitant oral para CINV produjo concentraciones plasmáticas mínimas medias de aprepitant superiores a 500 ng/mL en adultos, lo que se esperaría que, según la curva ajustada con la ecuación de Hill, resultara en una ocupación del receptor NK1 del cerebro superior al 95%. Sin embargo, no se ha determinado la ocupación del receptor para ningún régimen de dosificación de CINV o PONV. Además, no se ha establecido la relación entre la ocupación del receptor NK1 y la eficacia clínica de aprepitant.
Electrofisiología cardíaca
En un estudio QTc completo, aleatorizado, doble ciego, controlado con positivo, una dosis única de 200 mg de fosaprepitant no tuvo ningún efecto en el intervalo QTc. Las concentraciones máximas de aprepitant después de una dosis única de 200 mg de fosaprepitant fueron 4 y 9 veces más altas que las alcanzadas con aprepitant oral 125 mg y 40 mg, respectivamente. No se espera una prolongación del QT con los regímenes de dosificación de aprepitant oral recomendados para CINV y PONV.
12.3 FARMACOCINÉTICA
Después de la administración oral de una dosis única de 40 mg de aprepitant en ayunas, el área media bajo la curva de concentración plasmática-tiempo (AUC0–∞) fue de 7.8 mcg•hr/mL y la concentración plasmática máxima media (Cmax) fue de 0.7 mcg/mL, ocurriendo aproximadamente a las 3 horas después de la dosis
(Tmax). La biodisponibilidad absoluta a la dosis de 40 mg no se ha determinado.
Después de la administración oral de una dosis única de 125 mg de aprepitant en el Día 1 y 80 mg una vez al día en los Días 2 y 3, el AUC0-24hr fue de aproximadamente 19.6 mcg•hr/mL y 21.2 mcg•hr/mL en el Día 1 y el Día 3, respectivamente. El Cmax de 1.6 mcg/mL y 1.4 mcg/mL se alcanzaron en aproximadamente 4 horas (Tmax) en el Día 1 y el Día 3, respectivamente. En el rango de dosis de 80 a 125 mg, la biodisponibilidad oral absoluta media de aprepitant es de aproximadamente 60 a 65%. La administración oral de la cápsula con un desayuno estándar rico en grasas no tuvo ningún efecto clínicamente significativo en la biodisponibilidad de aprepitant.
La farmacocinética de aprepitant fue no lineal en todo el rango de dosis clínicas. En adultos jóvenes sanos, el aumento en AUC0-∞ fue un 26% mayor que la proporcionalidad a la dosis entre dosis únicas de 80 mg y 125 mg administradas en estado de alimentación.
Distribución
Aprepitant está unido a proteínas plasmáticas en más del 95%. El volumen de distribución aparente medio en estado estacionario (Vd ss) fue de aproximadamente 70 L en humanos.
Aprepitant cruza la barrera hematoencefálica en humanos [ver Farmacología clínica (12.1)].
Eliminación
Metabolismo
Aprepitant se metaboliza ampliamente. Los estudios in vitro utilizando microsomas hepáticos humanos indican que aprepitant se metaboliza principalmente por CYP3A4 con un metabolismo menor por CYP1A2 y CYP2C19. El metabolismo se produce principalmente por oxidación en el anillo de morfolina y sus cadenas laterales. No se detectó metabolismo por CYP2D6, CYP2C9 o CYP2E1. En adultos jóvenes sanos, aprepitant representa aproximadamente el 24% de la radiactividad en plasma durante 72 horas después de una dosis única oral de 300 mg de [14C]-aprepitant (2.4 veces la dosis máxima recomendada de aprepitant), lo que indica una presencia sustancial de metabolitos en el plasma. Se han identificado siete metabolitos de aprepitant, que solo son débilmente activos, en el plasma humano.
Excreción
Después de la administración de una dosis única intravenosa de 100 mg de [14C]-prodroga de aprepitant a sujetos sanos, se recuperó el 57% de la radiactividad en la orina y el 45% en las heces. No se realizó un estudio con la formulación de cápsulas radiactivas. Los resultados después de la administración oral pueden diferir.
Aprepitant se elimina principalmente por metabolismo; aprepitant no se excreta por vía renal. El aclaramiento plasmático aparente de aprepitant osciló entre aproximadamente 62 y 90 mL/min. La semivida terminal aparente osciló entre aproximadamente 9 y 13 horas.
Poblaciones específicas
Pacientes geriátricos
Tras la administración oral de una dosis única de 125 mg de aprepitant el Día 1 y 80 mg una vez al día del Día 2 al Día 5 (2 días adicionales de dosificación en comparación con la duración recomendada), el AUC0-24hr de aprepitant fue un 21 % más alto el Día 1 y un 36 % más alto el Día 5 en adultos mayores (de 65 años o más) en comparación con adultos más jóvenes. El Cmax fue un 10 % más alto el Día 1 y un 24 % más alto el Día 5 en adultos mayores en comparación con adultos más jóvenes. Estas diferencias no se consideran clínicamente significativas [ver Uso en Poblaciones Específicas (8.5)].
Pacientes pediátricos
Como parte de un régimen de 3 días, la dosificación de cápsulas de aprepitant (125 mg/80 mg/80 mg) en 18 pacientes pediátricos (de 12 a 17 años) logró un AUC0-24hr promedio de 17 mcg•hr/mL el Día 1, con una concentración plasmática pico promedio (Cmax) de 1,3 mcg/mL que se produjo aproximadamente a las 4 horas. Las concentraciones promedio al final del Día 2 (N = 8) y del Día 3 (N = 16) fueron ambas de 0,6 mcg/mL
Un análisis farmacocinético poblacional de aprepitant en pacientes pediátricos (de 6 meses a 17 años) sugiere que el sexo y la raza no tienen un efecto clínicamente significativo en la farmacocinética de aprepitant.
Pacientes masculinos y femeninos
Tras la administración oral de una dosis única de aprepitant que osciló entre 40 mg y 375 mg (3 veces la dosis máxima recomendada de aprepitant), el AUC0-24hr y el Cmax son un 9 % y un 17 % más altos en mujeres en comparación con hombres. La vida media de aprepitant es aproximadamente un 25 % más baja en mujeres en comparación con hombres y el Tmax se produce aproximadamente al mismo tiempo. Estas diferencias no se consideran clínicamente significativas.
Grupos raciales o étnicos
Tras la administración oral de una dosis única de aprepitant que osciló entre 40 mg y 375 mg (3 veces la dosis máxima recomendada de aprepitant), el AUC0-24hr y el Cmax son aproximadamente un 27 % y un 19 % más altos en hispanos en comparación con caucásicos. El AUC0-24hr y el Cmax fueron un 74 % y un 47 % más altos en asiáticos en comparación con caucásicos. No hubo diferencia en el AUC0-24hr o el Cmax entre caucásicos y negros. Estas diferencias no se consideran clínicamente significativas.
Pacientes con insuficiencia renal
Se administró una dosis única de 240 mg de aprepitant (aproximadamente 1,9 veces la dosis máxima recomendada de aprepitant) a pacientes con insuficiencia renal grave (depuración de creatinina inferior a 30 mL/min/1,73 m2 medida mediante depuración urinaria de creatinina de 24 horas) y a pacientes con enfermedad renal en etapa terminal (ERSD) que requirieron hemodiálisis.
En pacientes con insuficiencia renal grave, el AUC0-∞ de aprepitant total (libre y unido a proteínas) disminuyó un 21 % y el Cmax disminuyó un 32 %, en comparación con sujetos sanos (depuración de creatinina superior a 80 mL/min estimada por el método de Cockcroft-Gault). En pacientes con ESRD sometidos a hemodiálisis, el AUC0-∞ de aprepitant total disminuyó un 42 % y el Cmax disminuyó un 32 %. Debido a las disminuciones moderadas en la unión de proteínas de aprepitant en pacientes con enfermedad renal, el AUC del fármaco libre farmacológicamente activo no se vio afectado de manera significativa en pacientes con insuficiencia renal en comparación con sujetos sanos. La hemodiálisis realizada 4 u 8 horas después de la dosificación no tuvo un efecto significativo en la farmacocinética de aprepitant; menos del 0,2 % de la dosis se recuperó en el dializado [ver Uso en Poblaciones Específicas (8.6)].
Pacientes con insuficiencia hepática
Tras la administración de una dosis única de 125 mg de aprepitant el Día 1 y 80 mg una vez al día los Días 2 y 3 a pacientes con insuficiencia hepática leve (puntuación Child-Pugh 5 a 6), el AUC0-24hr de aprepitant fue un 11 % más bajo el Día 1 y un 36 % más bajo el Día 3, en comparación con sujetos sanos que recibieron el mismo régimen. En pacientes con insuficiencia hepática moderada (puntuación Child-Pugh 7 a 9), el AUC0-24hr de aprepitant fue un 10 % más alto el Día 1 y un 18 % más alto el Día 3, en comparación con sujetos sanos que recibieron el mismo régimen. Estas diferencias en el AUC0-24hr no se consideran clínicamente significativas. No hay datos clínicos o farmacocinéticos en pacientes con insuficiencia hepática grave (puntuación Child-Pugh mayor que 9) [ver Uso en Poblaciones Específicas (8.7)].
Índice de masa corporal (IMC)
Por cada 5 kg/m2 de aumento en el IMC, el AUC0-24hr y el Cmax de aprepitant disminuyen un 9 % y un 10 %. El IMC de los sujetos en el análisis varió de 18 kg/m2 a 36 kg/m2. Este cambio no se considera clínicamente significativo.
Estudios de interacciones farmacológicas
Aprepitant es un sustrato, un inhibidor débil a moderado (dependiente de la dosis) y un inductor de CYP3A4. Aprepitant también es un inductor de CYP2C9. Aprepitant es poco probable que interactúe con fármacos que son sustratos del transportador P-glicoproteína.
Efectos de aprepitant en la farmacocinética de otros fármacos
Sustratos de CYP3A4 (es decir, midazolam): Las interacciones entre aprepitant y midazolam coadministrado se enumeran en la Tabla 12 (el aumento se indica como “↑”, la disminución como “↓”, sin cambio como “↔”).
| Dosificación de aprepitant | Dosificación de midazolam | Interacciones observadas de fármacos |
| Aprepitant 125 mg en el Día 1 y 80 mg en los Días 2 a 5 | oral 2 mg dosis única en Días 1 y 5 |
AUC de midazolam ↑ 2.3 veces en el Día 1 y ↑ 3.3 veces en el Día 5 [ver Interacciones con medicamentos (7.1)] |
| Aprepitant 125 mg en el Día 1 y 80 mg en los Días 2 y 3 |
intravenoso 2 mg antes del régimen de 3 días de aprepitant y en los Días 4, 8 y 15 |
AUC de midazolam ↑ 25% en el Día 4, AUC ↓ 19% en el Día 8 y AUC ↓ 4% en el Día 15 |
| Aprepitant 125 mg en el Día 1 | intravenoso 2 mg administrado 1 hora después de aprepitant | AUC de midazolam ↑ 1.5 veces |
| Aprepitant 40 mg | oral 2 mg | AUC de midazolam ↑ 1.2 veces en el Día 1 |
Una diferencia de menos de 2 veces el aumento del AUC de midazolam no se considera clínicamente importante.
Corticosteroides:
Dexametasona: Aprepitant, cuando se administra como un régimen de 125 mg en el Día 1 y 80 mg/día en los Días 2 a 5, coadministrado con 20 mg de dexametasona en el Día 1 y 8 mg de dexametasona en los Días 2 a 5, aumentó el AUC de dexametasona en 2,2 veces en los Días 1 y 5
[ver Dosificación y administración (2.1)]. Una dosis única de aprepitant (40 mg) cuando se coadministra con una dosis única de dexametasona 20 mg, aumentó el AUC de dexametasona en 1,45 veces, lo que no se considera clínicamente significativo.
Metilprednisolona: Aprepitant, cuando se administra como un régimen de 125 mg en el Día 1 y 80 mg/día en los Días 2 y 3, coadministrado con 125 mg de metilprednisolona IV en el Día 1 y 40 mg de metilprednisolona por vía oral en los Días 2 y 3, aumentó el AUC de metilprednisolona en 1,34 veces en el Día 1 y en 2,5 veces en el Día 3. Aunque no se ha estudiado la administración concomitante de metilprednisolona con la dosis única de 40 mg de aprepitant, una dosis única de 40 mg de aprepitant produce una inhibición débil de CYP3A4 (basada en el estudio de interacción con midazolam) y no se espera que altere las concentraciones plasmáticas de metilprednisolona en un grado clínicamente significativo.
Agentes quimioterapéuticos:
Docetaxel: En un estudio farmacocinético, aprepitant (régimen de 125 mg/80 mg/80 mg) no influyó en la farmacocinética del docetaxel.
Vinorelbina: En un estudio farmacocinético, aprepitant (régimen de 125 mg/80 mg/80 mg) no influyó en la farmacocinética de la vinorelbina en un grado clínicamente significativo.
Sustratos de CYP2C9 (Warfarina, Tolbutamida): Warfarina: Se administró una dosis única de 125 mg de aprepitant en el Día 1 y 80 mg/día en los Días 2 y 3 a sujetos sanos que estaban estabilizados en terapia crónica con warfarina. Aunque no hubo efecto de aprepitant en el AUC plasmático de R(+) o S(-) warfarina determinado en el Día 3, hubo una disminución del 34% en la concentración mínima de S(-) warfarina acompañada de una disminución del 14% en el tiempo de protrombina (reportado como Razón Normalizada Internacional o INR) 5 días después de completar la dosificación con aprepitant [ver Interacciones medicamentosas (7.1)].
Tolbutamida: Aprepitant, cuando se administra como 125 mg en el Día 1 y 80 mg/día en los Días 2 y 3, disminuyó el AUC de tolbutamida en un 23% en el Día 4, un 28% en el Día 8 y un 15% en el Día 15, cuando se administró una dosis única de tolbutamida 500 mg antes de la administración del régimen de 3 días de aprepitant y en los Días 4, 8 y 15. Este efecto no se consideró clínicamente importante.
Aprepitant, cuando se administra como una dosis única de 40 mg en el Día 1, disminuyó el AUC de tolbutamida en un 8% en el Día 2, un 16% en el Día 4, un 15% en el Día 8 y un 10% en el Día 15, cuando se administró una dosis única de tolbutamida 500 mg antes de la administración de aprepitant 40 mg y en los Días 2, 4, 8 y 15. Este efecto no se consideró significativo.
Otros medicamentos
Anticonceptivos orales: Cuando aprepitant se administró como un régimen de 3 días (125 mg/80 mg/80 mg) con ondansetrón y dexametasona, y se coadministró con un anticonceptivo oral que contenía etinilestradiol y noretindrona, las concentraciones mínimas de etinilestradiol y noretindrona se redujeron hasta en un 64% durante las 3 semanas posteriores al tratamiento.
Cuando se administró una dosis diaria de un anticonceptivo oral que contenía etinilestradiol y norgestimato en los Días 1 a 21, y aprepitant 40 mg se administró en el Día 8, el AUC de etinilestradiol disminuyó en un 4% y en un 29% en el Día 8 y el Día 12, respectivamente, mientras que el AUC de norelgestromina aumentó en un 18% en el Día 8 y disminuyó en un 10% en el Día 12. Además, las concentraciones mínimas de etinilestradiol y norelgestromina en los Días 8 a 21 fueron generalmente más bajas después de la coadministración del anticonceptivo oral con aprepitant 40 mg en el Día 8 en comparación con los niveles mínimos después de la administración del anticonceptivo oral solo [ver Interacciones medicamentosas (7.1)].
Sustratos de la glicoproteína P: Es poco probable que aprepitant interactúe con medicamentos que son sustratos del transportador de glicoproteína P, como lo demuestra la falta de interacción de aprepitant con digoxina en un estudio clínico de interacción medicamentosa.
Antagonistas de 5-HT3 : En estudios clínicos de interacción medicamentosa, aprepitant no tuvo efectos clínicamente importantes en la farmacocinética de ondansetrón, granisetrón o hidrodolasetrón (el metabolito activo de dolasetrón).
Efecto de otros medicamentos en la farmacocinética de aprepitant
Ketoconazol: Cuando se administró una dosis única de 125 mg de aprepitant en el Día 5 de un régimen de 10 días de 400 mg/día de ketoconazol, un inhibidor fuerte de CYP3A4, el AUC de aprepitant aumentó aproximadamente 5 veces y la vida media terminal media de aprepitant aumentó aproximadamente 3 veces [ver Interacciones medicamentosas (7.2)].
Rifampicina: Cuando se administró una dosis única de 375 mg de aprepitant (3 veces la dosis máxima recomendada de aprepitant) en el Día 9 de un régimen de 14 días de 600 mg/día de rifampicina, un inductor fuerte de CYP3A4, el AUC de aprepitant disminuyó aproximadamente 11 veces y la vida media terminal media disminuyó aproximadamente 3 veces [ver Interacciones medicamentosas (7.2)].
Diltiazem: En pacientes con hipertensión leve a moderada, la administración de aprepitant una vez al día, como una formulación en tabletas comparable a 230 mg de la formulación en cápsulas (aproximadamente 1,8 veces la dosis recomendada de aprepitant), con diltiazem 120 mg 3 veces al día durante 5 días, resultó en un aumento de 2 veces del AUC de aprepitant y un aumento simultáneo de 1,7 veces del AUC de diltiazem. Estos efectos farmacocinéticos no dieron lugar a cambios clínicamente significativos en el ECG, la frecuencia cardíaca o la presión arterial más allá de los cambios inducidos por el diltiazem solo [ver Interacciones medicamentosas (7.2)].
Paroxetina: La coadministración de dosis únicas diarias de aprepitant, como una formulación en tabletas comparable a 85 mg o 170 mg de la formulación en cápsulas (aproximadamente 0,7 y 1,4 veces la dosis máxima recomendada de aprepitant), con paroxetina 20 mg una vez al día, resultó en una disminución del AUC en aproximadamente un 25% y Cmax en aproximadamente un 20% tanto de aprepitant como de paroxetina. Este efecto no se consideró clínicamente importante.
13 TOXICOLOGÍA NO CLÍNICA
13.1 Carcinogénesis, Mutagénesis, Deterioro de la Fertilidad
Se realizaron estudios de carcinogenicidad en ratas Sprague-Dawley y en ratones CD-1 durante 2 años. En los estudios de carcinogenicidad en ratas, los animales fueron tratados con dosis orales que oscilaron entre 0,05 y 1.000 mg/kg dos veces al día. La dosis más alta produjo una exposición sistémica a aprepitant (AUC) de 0,7 a 1,6 veces la exposición humana adulta en el régimen de aprepitant de 125 mg/80 mg/80 mg. El tratamiento con aprepitant en dosis de 5 a 1.000 mg/kg dos veces al día provocó un aumento en la incidencia de adenomas y carcinomas de células foliculares tiroideas en ratas macho. En las ratas hembra, produjo adenomas hepatocelulares a 5 a 1.000 mg/kg dos veces al día y carcinomas hepatocelulares y adenomas de células foliculares tiroideas a 125 a 1.000 mg/kg dos veces al día. En los estudios de carcinogenicidad en ratones, los animales fueron tratados con dosis orales que oscilaron entre 2,5 y 2.000 mg/kg/día. La dosis más alta produjo una exposición sistémica de aproximadamente 2,8 a 3,6 veces la exposición humana adulta en el régimen de aprepitant de 125 mg/80 mg/80 mg. El tratamiento con aprepitant produjo fibrosarcomas cutáneos a dosis de 125 y 500 mg/kg/día en ratones macho.
Mutagénesis
Aprepitant no fue genotóxico en la prueba de Ames, la prueba de mutagénesis de células linfoblastoides humanas (TK6), la prueba de rotura de la cadena de ADN de hepatocitos de rata, la prueba de aberración cromosómica de células de ovario de hámster chino (CHO) y la prueba de micronúcleos de ratón.
Deterioro de la Fertilidad
Aprepitant no afectó la fertilidad o el rendimiento reproductivo general de las ratas macho o hembra a dosis de hasta la dosis máxima factible de 1.000 mg/kg dos veces al día (proporcionando una exposición en ratas macho inferior a la exposición en la dosis humana adulta recomendada y una exposición en ratas hembra de aproximadamente 1,6 veces la exposición humana adulta en el régimen de aprepitant de 125 mg/80 mg/80 mg).
14 ESTUDIOS CLÍNICOS
14.1 Prevención de náuseas y vómitos asociados con HEC en adultos
La administración oral de aprepitant en combinación con ondansetrón y dexametasona (régimen de aprepitant) ha demostrado prevenir las náuseas y vómitos agudos y retardados asociados con HEC, incluyendo cisplatino en dosis alta, y las náuseas y vómitos asociados con MEC.
En los Estudios 1 y 2, ambos estudios clínicos multicéntricos, aleatorizados, paralelos, doble ciego y controlados en adultos, el aprepitant en combinación con ondansetrón y dexametasona se comparó con la terapia estándar (ondansetrón y dexametasona sola) en pacientes que recibieron un régimen de quimioterapia que incluía cisplatino mayor de 50 mg/m2(dosis media de cisplatino = 80.2 mg/m2). Ver Tabla 13.
En estos estudios, el 95% de los pacientes del grupo de aprepitant recibió un agente quimioterapéutico concomitante además del cisplatino prescrito en el protocolo. Los agentes quimioterapéuticos más comunes y el número de pacientes expuestos al aprepitant son los siguientes: etopósido (106), fluorouracilo (100), gemcitabina (89), vinorelbina (82), paclitaxel (52), ciclofosfamida (50), doxorubicina (38), docetaxel (11).
De los 550 pacientes que fueron aleatorizados para recibir el régimen de aprepitant, el 42% eran mujeres, el 58% hombres, el 59% blancos, el 3% asiáticos, el 5% negros, el 12% hispanoamericanos y el 21% multirraciales. Los pacientes tratados con aprepitant en estos estudios clínicos variaron de 14 a 84 años de edad, con una edad media de 56 años. Un total de 170 pacientes tenían 65 años o más, y 29 pacientes tenían 75 años o más.
|
*Se utilizaron el placebo de aprepitant y el placebo de dexametasona para mantener el ciego. |
||||
|
†Aprepitant se administró 1 hora antes del tratamiento de quimioterapia en el Día 1 y por la mañana en los Días 2 y 3 |
||||
|
‡Dexametasona se administró 30 minutos antes del tratamiento de quimioterapia en el Día 1 y por la mañana en los Días 2 a 4. La dosis de 12 mg de dexametasona en el Día 1 refleja un ajuste de dosis para tener en cuenta una interacción farmacológica con el régimen de aprepitant [ver Farmacología Clínica (12.3)]. |
||||
|
§Se utilizó ondansetrón 32 mg intravenoso en los ensayos clínicos de aprepitant. Aunque se utilizó esta dosis en los ensayos clínicos, esta ya no es la dosis recomendada actualmente. Consulte la información de prescripción de ondansetrón para la dosis recomendada actual. |
||||
| Día 1 | Día 2 | Día 3 | Día 4 | |
| Régimen de CINV de Aprepitant | ||||
| Aprepitant oral † | 125 mg | 80 mg | 80 mg | ninguno |
| Dexametasona oral ‡ | 12 mg | 8 mg | 8 mg | 8 mg |
| Ondansetrón | Antagonista 5-HT 3 § |
ninguno | ninguno | ninguno |
| Terapia estándar de CINV | ||||
| Dexametasona oral | 20 mg | 8 mg dos veces al día | 8 mg dos veces al día | 8 mg dos veces al día |
| Ondansetrón | Antagonista 5-HT 3§ | ninguno | ninguno | ninguno |
La actividad antiemética de aprepitant fue evaluada durante la fase aguda (0 a 24 horas después del tratamiento con cisplatino), la fase tardía (25 a 120 horas después del tratamiento con cisplatino) y en general (0 a 120 horas después del tratamiento con cisplatino) en el Ciclo 1. La eficacia se basó en la evaluación de los siguientes criterios de valoración en los que los episodios eméticos incluyeron vómitos, arcadas o arcadas secas:
Criterio principal de valoración:
• respuesta completa (definida como ningún episodio emético y ningún uso de terapia de rescate según lo registrado en los diarios de los pacientes)
Otros criterios de valoración preespecificados:
• protección completa (definida como ningún episodio emético, ningún uso de terapia de rescate y una puntuación máxima en la escala analógica visual [VAS] de náuseas inferior a 25 mm en una escala de 0 a 100 mm)
• sin emesis (definida como ningún episodio emético independientemente del uso de terapia de rescate)
• sin náuseas (VAS máxima inferior a 5 mm en una escala de 0 a 100 mm)
• sin náuseas significativas (VAS máxima inferior a 25 mm en una escala de 0 a 100 mm)
En la Tabla 14 se muestra un resumen de los resultados clave del estudio de cada análisis individual. En ambos estudios, una proporción estadísticamente significativa de pacientes que recibieron el régimen de aprepitant en el Ciclo 1 tuvo una respuesta completa en la fase general (criterio principal de valoración), en comparación con los pacientes que recibieron la terapia estándar. También se observó una diferencia estadísticamente significativa en la respuesta completa a favor del régimen de aprepitant cuando se analizaron por separado la fase aguda y la fase tardía.
|
Rango de puntuación de la escala analógica visual (VAS): 0 mm=sin náuseas; 100 mm=náuseas tan intensas como sea posible. |
||||||
|
*N: Número de pacientes (mayores de 18 años) que recibieron cisplatino, fármaco del estudio y tuvieron al menos una evaluación de eficacia posterior al tratamiento. |
||||||
|
†General: 0 a 120 horas después del tratamiento con cisplatino. |
||||||
|
‡Fase aguda: 0 a 24 horas después del tratamiento con cisplatino. |
||||||
|
§Fase tardía: 25 a 120 horas después del tratamiento con cisplatino. |
||||||
|
¶No estadísticamente significativo cuando se ajusta para comparaciones múltiples. |
||||||
|
#No estadísticamente significativo. |
||||||
| Estudio 1 | Estudio 2 | |||||
| CRITERIOS DE VALORACIÓN | Régimen de aprepitant (N=260)* % |
Terapia estándar (N=261)* % |
Valor p | Régimen de aprepitant (N=261)* % |
Terapia estándar (N=263)* % |
Valor p |
| CRITERIO PRINCIPAL DE VALORACIÓN | ||||||
| Respuesta completa | ||||||
| General † | 73 | 52 | <0.001 | 63 | 43 | <0.001 |
| OTROS CRITERIOS DE VALORACIÓN PREESPECIFICADOS | ||||||
| Respuesta completa | ||||||
| Fase aguda ‡ Fase tardía § | 89 75 |
78 56 |
<0.001 <0.001 |
83 68 |
68 47 |
<0.001 <0.001 |
| Protección completa | ||||||
| General Fase aguda Fase tardía |
63 85 66 |
49 75 52 |
0.001 NS¶ <0.001 |
56 80 61 |
41 65 44 |
<0.001 <0.001 <0.001 |
| Sin emesis | ||||||
| General Fase aguda Fase tardía |
78 90 81 |
55 79 59 |
<0.001 0.001 <0.001 |
66 84 72 |
44 69 48 |
<0.001 <0.001 <0.001 |
| Sin náuseas | ||||||
| General Fase tardía |
48 51 |
44 48 |
NS# NS# |
49 53 |
39 40 |
NS¶ NS¶ |
| Sin náuseas significativas | ||||||
| General Fase tardía |
73 75 |
66 69 |
NS# NS# |
71 73 |
64 65 |
NS# NS# |
En ambos estudios, el tiempo estimado hasta la primera aparición de emesis después del inicio del tratamiento con cisplatino fue mayor con el régimen de aprepitant, y la incidencia de la primera aparición de emesis se redujo en el grupo del régimen de aprepitant en comparación con el grupo de terapia estándar, como se muestra en las curvas de Kaplan-Meier de la Figura 1.
Figura 1: Porcentaje de pacientes que reciben HEC que permanecen libres de emesis a lo largo del tiempo: ciclo 1
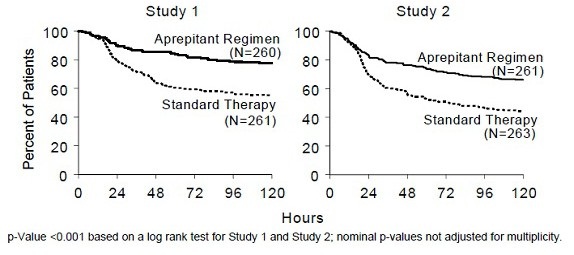
Resultados adicionales informados por los pacientes: El impacto de las náuseas y los vómitos en la vida diaria de los pacientes se evaluó en el ciclo 1 de ambos estudios utilizando el Índice de Vida Funcional-Emesis (FLIE), una medida de resultado validada específica para las náuseas y los vómitos informada por los pacientes. El impacto mínimo o nulo de las náuseas y los vómitos en la vida diaria de los pacientes se define como una puntuación total del FLIE superior a 108. En cada uno de los 2 estudios, una mayor proporción de pacientes que recibieron el régimen de aprepitant notificaron un impacto mínimo o nulo de las náuseas y los vómitos en la vida diaria (Estudio 1: 74 % frente a 64 %; Estudio 2: 75 % frente a 64 %).
Extensión de ciclos múltiples: En los mismos 2 estudios clínicos, los pacientes continuaron en la extensión de ciclos múltiples hasta 5 ciclos adicionales de quimioterapia. La proporción de pacientes sin emesis y sin náuseas significativas por grupo de tratamiento en cada ciclo se muestra en la Figura 2. La eficacia antiemética de los pacientes que recibieron el régimen de aprepitant se mantuvo a lo largo de los ciclos repetidos para aquellos pacientes que continuaron en cada uno de los ciclos múltiples.
Figura 2: Proporción de pacientes que reciben HEC sin emesis y sin náuseas significativas por grupo de tratamiento y ciclo
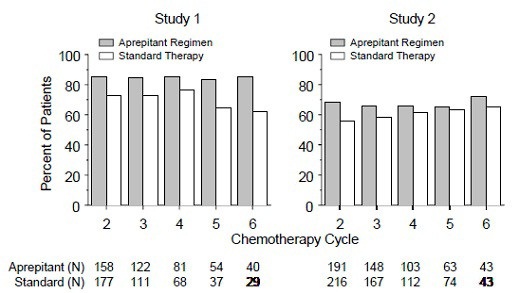
14.2 Prevención de las náuseas y los vómitos asociados a la MEC en adultos
Se estudió Aprepitant en dos estudios aleatorizados, doble ciego y de grupos paralelos (Estudios 3 y 4) en pacientes adultos que recibían MEC.
En el Estudio 3, en pacientes con cáncer de mama, se comparó aprepitant en combinación con ondansetrón y dexametasona con la terapia estándar (ondansetrón y dexametasona) en pacientes que recibían un régimen de MEC que incluía ciclofosfamida de 750 a 1500 mg/m2; o ciclofosfamida de 500 a 1,500 mg/m2 y doxorrubicina (menor o igual a 60 mg/m2) o epirrubicina (menor o igual a 100 mg/m2). Véase la Tabla 15.
En este estudio, las combinaciones más comunes fueron ciclofosfamida + doxorrubicina (61 %); y ciclofosfamida + epirrubicina + fluorouracilo (22 %).
De las 438 pacientes que fueron asignadas aleatoriamente para recibir el régimen de aprepitant, el 99.5 % eran mujeres. De ellas, aproximadamente el 80 % eran blancas, el 8 % negras, el 8 % asiáticas, el 4 % hispanas y menos del 1 % otras. Las pacientes tratadas con aprepitant en este estudio clínico tenían entre 25 y 78 años de edad, con una edad media de 53 años; 70 pacientes tenían 65 años o más, y 12 pacientes tenían más de 74 años.
|
*Se utilizaron placebo de APREPITANT y placebo de dexametasona para mantener el enmascaramiento. |
|||
|
†APREPITANT se administró 1 hora antes del tratamiento de quimioterapia el día 1 y por las mañanas de los días 2 y 3. |
|||
|
‡La dexametasona se administró 30 minutos antes del tratamiento de quimioterapia el día 1. La dosis de 12 mg de dexametasona el día 1 refleja un ajuste de la dosis para tener en cuenta una interacción farmacológica con el régimen de APREPITANT [véase Farmacología clínica (12.3)] . |
|||
|
§La primera dosis de ondansetrón se administró entre 30 y 60 minutos antes del tratamiento de quimioterapia el día 1 y la segunda dosis se administró 8 horas después de la primera dosis de ondansetrón. |
|||
| Día 1 | Día 2 | Día 3 | |
| Régimen de APREPITANT para las náuseas y los vómitos inducidos por la quimioterapia | |||
| APREPITANT oral† | 125 mg | 80 mg | 80 mg |
| Dexametasona oral | 12 mg ‡ | ninguna | ninguna |
| Ondansetrón oral | 8 mg x 2 dosis§ | ninguna | ninguna |
| Terapia estándar para las náuseas y los vómitos inducidos por la quimioterapia | |||
| Dexametasona oral | 20 mg ‡ | none | none |
| Ondansetrón oral | 8 mg x 2 dosis§ | 8 mg dos veces al día | 8 mg dos veces al día |
La actividad antiemética de aprepitant se evaluó con base en los siguientes criterios de valoración en los que los episodios eméticos incluyeron vómitos, arcadas o arcadas secas:
Criterio principal de valoración:
• respuesta completa (definida como ningún episodio emético y ningún uso de terapia de rescate según se registró en los diarios de los pacientes) en la fase general (0 a 120 horas después de la quimioterapia)
Otros criterios de valoración preespecificados:
• sin emesis (definido como ningún episodio emético independientemente del uso de terapia de rescate)
• sin náuseas (VAS máxima inferior a 5 mm en una escala de 0 a 100 mm)
• sin náuseas significativas (VAS máxima inferior a 25 mm en una escala de 0 a 100 mm)
• protección completa (definida como ningún episodio emético, ningún uso de terapia de rescate y una puntuación máxima en la escala analógica visual [VAS] de náuseas inferior a 25 mm en una escala de 0 a 100 mm)
• respuesta completa durante las fases aguda y tardía.
En la Tabla 16, se muestra un resumen de los resultados clave del Estudio 3. En el Estudio 3, una proporción estadísticamente significativa (p=0,015) mayor de pacientes que recibieron el régimen con aprepitant (51 %) en el Ciclo 1 tuvo una respuesta completa (criterio principal de valoración) durante la fase general en comparación con los pacientes que recibieron la terapia estándar (42 %). La diferencia entre los grupos de tratamiento se debió principalmente al “Criterio de valoración sin emesis”, un componente principal de este criterio principal de valoración compuesto. Además, una mayor proporción de pacientes que recibieron el régimen con aprepitant en el Ciclo 1 tuvo una respuesta completa durante las fases aguda (0 a 24 horas) y tardía (25 a 120 horas) en comparación con los pacientes que recibieron la terapia estándar; sin embargo, las diferencias entre los grupos de tratamiento no alcanzaron significación estadística, después de los ajustes de multiplicidad.
|
*N: Número de pacientes incluidos en el análisis primario de respuesta completa. |
|||
|
†General: 0 a 120 horas después del tratamiento de quimioterapia. |
|||
|
‡NS cuando se ajusta para la regla de comparaciones múltiples preespecificada; valor p no ajustado <0,001. |
|||
| CRITERIOS DE VALORACIÓN | Régimen con Aprepitant (N=433)* % |
Terapia estándar (N=424)* % |
Valor p |
| CRITERIO PRINCIPAL DE VALORACIÓN† | |||
| Respuesta completa | 51 | 42 | 0.015 |
| OTROS CRITERIOS DE VALORACIÓN PREESPECIFICADOS† | |||
| Sin emesis | 76 | 59 | NS‡ |
| Sin náuseas | 33 | 33 | NS |
| Sin náuseas significativas | 61 | 56 | NS |
| Sin terapia de rescate | 59 | 56 | NS |
| Protección completa | 43 | 37 | NS |
Resultados adicionales informados por el paciente: En el Estudio 3, en pacientes que recibieron MEC, el impacto de las náuseas y los vómitos en la vida diaria de los pacientes se evaluó en el Ciclo 1 utilizando el FLIE. Una mayor proporción de pacientes que recibieron el régimen de aprepitant reportaron un impacto mínimo o nulo en la vida diaria (64% versus 56%). Esta diferencia entre los grupos de tratamiento se debió principalmente al “Dominio sin vómitos” de este criterio de valoración compuesto.
Extensión de ciclos múltiples: En el Estudio 3, los pacientes que recibieron MEC pudieron continuar en la extensión de ciclos múltiples del estudio hasta por 3 ciclos adicionales de quimioterapia. El efecto antiemético para los pacientes que recibieron el régimen de aprepitant se mantuvo durante todos los ciclos.
En el Estudio 4, se comparó aprepitant en combinación con ondansetrón y dexametasona con una terapia estándar (ondansetrón y dexametasona solos) en pacientes que recibieron un régimen de MEC que incluía cualquier dosis intravenosa de oxaliplatino, carboplatino, epirubicina, idarubicina, ifosfamida, irinotecán, daunorubicina, doxorubicina; ciclofosfamida intravenosa (menos de 1500 mg/m 2); o citarabina intravenosa (más de 1 g/m 2). Ver Tabla 15. Los pacientes que recibieron el régimen de aprepitant estaban recibiendo quimioterapia para una variedad de tipos de tumores, incluyendo 50% con cáncer de mama, 21% con cánceres gastrointestinales incluyendo cáncer colorrectal, 13% con cáncer de pulmón y 6% con cánceres ginecológicos.
De los 430 pacientes que fueron asignados al azar para recibir el régimen de aprepitant, el 76% eran mujeres y el 24% eran hombres. La distribución por raza fue 67% blanca, 6% negra o afroamericana, 11% asiática y 12% multirracial. Clasificados por origen étnico, el 36% eran hispanos y el 64% no hispanos. Los pacientes tratados con aprepitant en este estudio clínico tenían entre 22 y 85 años de edad, con una edad media de 57 años; aproximadamente el 59% de los pacientes tenían 55 años o más y 32 pacientes tenían más de 74 años.
La actividad antiemética de aprepitant se evaluó en base a la ausencia de vómitos (con o sin terapia de rescate) en el período general (0 a 120 horas después de la quimioterapia) y la respuesta completa (definida como ausencia de vómitos y no uso de terapia de rescate) en el período general.
En la Tabla 17 se muestra un resumen de los resultados clave del Estudio 4. En el Estudio 4, una proporción estadísticamente significativamente mayor de pacientes que recibieron el régimen de aprepitant (76%) en el Ciclo 1 no tuvo vómitos durante la fase general en comparación con los pacientes que recibieron la terapia estándar (62%). Además, una mayor proporción de pacientes que recibieron el régimen de aprepitant (69%) en el Ciclo 1 tuvo una respuesta completa en la fase general (0 a 120 horas) en comparación con los pacientes que recibieron la terapia estándar (56%). En la fase aguda (0 a 24 horas después del inicio de la quimioterapia), se observó que una mayor proporción de pacientes que recibieron aprepitant en comparación con los pacientes que recibieron la terapia estándar no tuvieron vómitos (92% y 84%, respectivamente) y una respuesta completa (89% y 80%, respectivamente). En la fase tardía (25 a 120 horas después del inicio de la quimioterapia), se observó que una mayor proporción de pacientes que recibieron aprepitant en comparación con los pacientes que recibieron la terapia estándar no tuvieron vómitos (78% y 67%, respectivamente) y una respuesta completa (71% y 61%, respectivamente).
En un análisis de subgrupos por tipo de tumor, se observó que una proporción numéricamente mayor de pacientes que recibieron aprepitant no tuvieron vómitos y una respuesta completa en comparación con los pacientes que recibieron la terapia estándar. Por sexo, la diferencia en las tasas de respuesta completa entre los grupos de aprepitant y el régimen estándar fue del 14% en mujeres (64,5% y 50,3%, respectivamente) y del 4% en hombres (82,2% y 78,2%, respectivamente) durante la fase general. Se observó una diferencia similar para el sexo en el criterio de valoración de ausencia de vómitos.
|
*N = Número de pacientes que recibieron tratamiento de quimioterapia, fármaco del estudio y tuvieron al menos una evaluación de eficacia posterior al tratamiento. |
|||
| CRITERIOS DE VALORACIÓN | Régimen de aprepitant (N=430)* % |
Terapia estándar (N=418)* % |
Valor p |
| Sin vómitos en general | 76 | 62 | <0.0001 |
| Respuesta completa en general | 69 | 56 | 0.0003 |
14.3 Prevención de náuseas y vómitos asociados con HEC o MEC en pacientes pediátricos
En un estudio clínico aleatorizado, doble ciego, controlado con comparador activo que incluyó a 302 pacientes pediátricos de 6 meses a 17 años que recibieron HEC o MEC, el aprepitant en combinación con ondansetrón se comparó con el ondansetrón solo (régimen de control) para la prevención de CINV (Estudio 5). La dexametasona intravenosa estaba permitida como parte del régimen antiemético en ambos grupos de tratamiento, a discreción del médico. Se requirió una reducción de la dosis de dexametasona en un 50% para los pacientes del grupo de aprepitant, reflejando un ajuste de dosis para tener en cuenta una interacción farmacológica [ver Farmacología Clínica (12.3)]. No se requirió una reducción de la dosis de dexametasona para los pacientes que recibieron el régimen de control.
Los pacientes elegibles tenían una malignidad documentada en el diagnóstico original o en la recaída y estaban programados para recibir quimioterapia emetógena o un régimen de quimioterapia que no se había tolerado previamente debido a los vómitos junto con ondansetrón como parte de su régimen antiemético.
De los 152 pacientes pediátricos aleatorizados para recibir el régimen de aprepitant, el 55% eran varones, el 45% mujeres, el 78% blancos, el 7% asiáticos, el 0% negros, el 24% hispanos y el 13% multirraciales. Las neoplasias primarias más comunes en los sujetos que recibieron el régimen de aprepitant fueron osteosarcoma (11%), sarcoma de Ewing (11%), neuroblastoma (9%) y rabdomiosarcoma (8%). Otros agentes de quimioterapia concomitantes comúnmente administrados y el número de pacientes expuestos al aprepitant fueron: sulfato de vincristina (65), etopósido (59), doxorubicina (48), ifosfamida (45), carboplatino (39) y cisplatino (35).
Los regímenes de tratamiento en el Estudio 5 para pacientes pediátricos se definen en la Tabla 18. De los pacientes pediátricos, el 29% en el régimen de aprepitant y el 28% en el régimen de control utilizaron dexametasona como parte del régimen antiemético en el Ciclo 1.
|
*La dexametasona intravenosa estaba permitida a discreción del médico. Se requirió una reducción de la dosis de dexametasona en un 50% para los pacientes del grupo de aprepitant, reflejando un ajuste de dosis para tener en cuenta una interacción farmacológica [ver Farmacología Clínica (12.3)]. No se requirió una reducción de la dosis de dexametasona para los pacientes en el régimen de control. |
|||
|
†El aprepitant se administró 1 hora antes del tratamiento de quimioterapia en los Días 1, 2 y 3. Si no se dio quimioterapia en los Días 2 y 3, el aprepitant se administró por la mañana. |
|||
|
‡El ondansetrón se administró 30 minutos antes de la quimioterapia en el Día 1 |
|||
|
§Se usó un placebo de aprepitant para mantener el ciego. |
|||
| Día 1 | Día 2 | Día 3 | |
| Régimen de aprepitant para CINV | |||
| Pacientes pediátricos de 6 meses a menos de 12 años de edad† | 3 mg/kg de peso corporal suspensión oral | 2 mg/kg de peso corporal suspensión oral | 2 mg/kg de peso corporal suspensión oral |
| Pacientes pediátricos de 12 a 17 años de edad† | 125 mg cápsula | 80 mg cápsula | 80 mg cápsula |
| Ondansetrón | Según la atención estándar ‡ | ninguno | ninguno |
| Régimen de control para CINV§ | |||
| Ondansetrón | Según la atención estándar ‡ | ninguno | ninguno |
La actividad antiemética de aprepitant se evaluó durante un período de 5 días (120 horas) después del inicio de la quimioterapia el día 1. El criterio principal de valoración en el Estudio 5 fue la respuesta completa en la fase tardía (25 a 120 horas después de la quimioterapia) en el Ciclo 1. Los pacientes tuvieron la oportunidad de recibir aprepitant de etiqueta abierta en ciclos posteriores (Ciclos opcionales del 2 al 6); sin embargo, no se evaluó la eficacia en estos ciclos opcionales. La eficacia general se basó en la evaluación de los siguientes criterios de valoración:
Criterio principal de valoración:
• respuesta completa (sin vómitos, arcadas ni uso de medicación de rescate) en la fase tardía (25 a 120 horas después del inicio de la quimioterapia)
Otros criterios de valoración preespecificados:
• respuesta completa en la fase aguda (0 a 24 horas después del inicio de la quimioterapia)
• respuesta completa en la fase general (hasta 120 horas después del inicio de la quimioterapia)
• ausencia de vómitos (definida como ausencia de emesis, arcadas o arcadas improductivas, independientemente del uso de medicación de rescate) en la fase general
• seguridad y tolerabilidad
En la Tabla 19 se muestra un resumen de los resultados clave del estudio.
|
*Respuesta completa = Sin vómitos ni arcadas y sin uso de medicación de rescate. |
||
|
†p<0.01 cuando se compara con el Régimen de control ‡ p<0.05 cuando se compara con el Régimen de control |
||
|
n/m = Número de pacientes con la respuesta deseada/número de pacientes incluidos en el punto temporal. |
||
|
Fase aguda: 0 a 24 horas después del inicio de la quimioterapia. |
||
|
Fase tardía: 25 a 120 horas después del inicio de la quimioterapia. |
||
|
Fase general: 0 a 120 horas después del inicio de la quimioterapia. |
||
| Régimen de Aprepitant n/m (%) |
Régimen de control n/m (%) | |
| CRITERIO PRINCIPAL DE VALORACIÓN | ||
| Respuesta completa * – Fase tardía | 77/152 (50.7)† | 39/150 (26.0) |
| OTROS CRITERIOS DE VALORACIÓN PREESPECIFICADOS | ||
| Respuesta completa * – Fase aguda | 101/152 (66.4)‡ | 78/150 (52.0) |
| Respuesta completa * – Fase general | 61/152 (40.1)† | 30/150 (20.0) |
14.4 Prevención de náuseas y vómitos postoperatorios en adultos
En dos estudios clínicos multicéntricos, aleatorizados, doble ciego, controlados con comparador activo y en grupos paralelos (Estudios 7 y 8), se comparó el aprepitant con el ondansetrón para la prevención de las náuseas y vómitos postoperatorios en 1.658 pacientes sometidos a cirugía abdominal abierta. Estos dos estudios tenían un diseño similar; sin embargo, diferían en términos de hipótesis del estudio, análisis de eficacia y ubicación geográfica. El Estudio 7 fue un estudio multinacional que incluía a EE. UU., mientras que el Estudio 8 se realizó completamente en EE. UU.
En los dos estudios, los pacientes fueron aleatorizados para recibir 40 mg de aprepitant, 125 mg de aprepitant o 4 mg de ondansetrón en una dosis única. El aprepitant se administró por vía oral con 50 mL de agua de 1 a 3 horas antes de la anestesia. El ondansetrón se administró por vía intravenosa inmediatamente antes de la inducción de la anestesia. Una comparación entre la dosis de 125 mg de aprepitant no demostró ningún beneficio clínico adicional sobre la dosis de 40 mg y no es un régimen de dosificación recomendado [ver Dosificación y Administración (2.2)].
De los 564 pacientes que recibieron 40 mg de aprepitant, el 92% eran mujeres y el 8% eran hombres; de estos, el 58% eran blancos, el 13% hispanoamericanos, el 7% multirraciales, el 14% negros, el 6% asiáticos y el 2% otros. La edad de los pacientes tratados con 40 mg de aprepitant osciló entre 19 y 84 años, con una edad media de 46,1 años. 46 pacientes tenían 65 años o más, y 13 pacientes tenían 75 años o más.
La actividad antiemética del aprepitant se evaluó durante el período de 0 a 48 horas después del final de la cirugía.
Medidas de eficacia en el Estudio 7 incluyeron:
• Sin vómitos (definido como ningún episodio emético independientemente del uso de terapia de rescate) en las 0 a 24 horas después del final de la cirugía (primario)
• Respuesta completa (definida como ningún episodio emético y sin uso de terapia de rescate) en las 0 a 24 horas después del final de la cirugía (primario)
• Sin vómitos (definido como ningún episodio emético independientemente del uso de terapia de rescate) en las 0 a 48 horas después del final de la cirugía (secundario)
• Tiempo hasta el primer uso de la medicación de rescate en las 0 a 24 horas después del final de la cirugía (exploratorio)
• Tiempo hasta el primer vómito en las 0 a 48 horas después del final de la cirugía (exploratorio).
Se aplicó un procedimiento de prueba cerrada para controlar el error de tipo I para los puntos finales primarios.
Los resultados de los puntos finales primarios y secundarios para 40 mg de aprepitant y 4 mg de ondansetrón se describen en la Tabla 20:
|
n/m = Número de respondedores / número de pacientes en el análisis. |
||||
|
∆Diferencia (%): 40 mg de aprepitant menos ondansetrón. |
||||
|
*Ratio de probabilidades estimado de aprepitant frente a ondansetrón. Un valor > 1 favorece al aprepitant sobre el ondansetrón. |
||||
|
‡LB = Límite inferior del intervalo de confianza unilateral del 97.5% para la ratio de probabilidades. |
||||
|
§Basado en la estrategia de multiplicidad de secuencia fija preespecificada, 40 mg de aprepitant no fue superior al ondansetrón. |
||||
| Tratamiento | n/m (%) | Aprepitant vs. Ondansetrón |
||
| ∆ | Ratio de probabilidades * | Análisis | ||
| PUNTOS FINALES PRIMARIOS | ||||
| Sin Vomitar 0 a 24 horas (Superioridad) (sin episodios eméticos) | ||||
| Aprepitant 40 mg | 246/293 (84.0) | 12.6% | 2.1 | P < 0.001† |
| Ondansetrón | 200/280 (71.4) | |||
| Respuesta Completa (No inferioridad: Si LB ‡ > 0.65) (sin vómitos y sin terapia de rescate, 0 a 24 horas) | ||||
| Aprepitant 40 mg | 187/293 (63.8) | 8.8% | 1.4 | LB = 1.02 |
| Ondansetron | 154/280 (55.0) | |||
| Respuesta completa (Superioridad: Si LB >1.0) (sin emesis y sin terapia de rescate, 0 a 24 horas) |
||||
| Aprepitant 40 mg | 187/293 (63.8) | 8.8% | 1.4 | LB=1.02‡ |
| Ondansetron | 154/280 (55.0) | |||
| CRITERIO DE VALORACIÓN SECUNDARIO | ||||
| Sin vómitos 0 a 48 horas (Superioridad) (sin episodios eméticos) | ||||
| Aprepitant 40 mg | 238/292 (81.5) | 15.2% | 2.3 | P<0.001§ |
| Ondansetron | 185/279 (66.3) | |||
En el Estudio 7, el uso de aprepitant no afectó el tiempo hasta el primer uso de medicación de rescate en comparación con ondansetron. Sin embargo, en comparación con el grupo de ondansetron, el uso de aprepitant retrasó el tiempo hasta el primer vómito, como se muestra en la Figura 3.
Figura 3: Porcentaje de pacientes que permanecen libres de emesis durante las 48 horas posteriores al final de la cirugía – Estudio 7
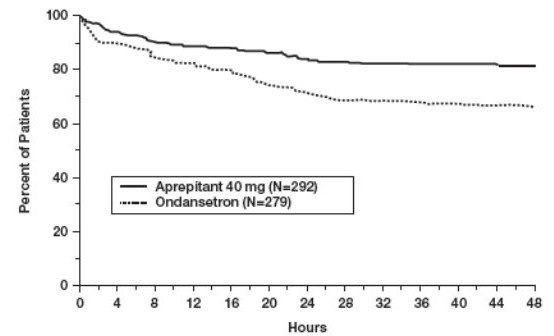
Las medidas de eficacia en el Estudio 8 incluyeron:
• respuesta completa (definida como ningún episodio emético y ningún uso de terapia de rescate) en las 0 a 24 horas posteriores al final de la cirugía (primaria)
• sin emesis (definido como ningún episodio emético independientemente del uso de terapia de rescate) en las 0 a 24 horas posteriores al final de la cirugía (secundaria)
• sin uso de terapia de rescate en las 0 a 24 horas posteriores al final de la cirugía (secundaria)
• sin emesis (definido como ningún episodio emético independientemente del uso de terapia de rescate) en las 0 a 48 horas posteriores al final de la cirugía (secundaria).
El estudio 8 no logró satisfacer su hipótesis principal de que aprepitant es superior a ondansetron en la prevención de PONV según lo medido por la proporción de pacientes con respuesta completa en las 24 horas posteriores al final de la cirugía.
El estudio demostró que 40 mg de aprepitant tuvo un efecto clínicamente significativo con respecto al criterio de valoración secundario “sin vómitos” durante las primeras 24 horas después de la cirugía y se asoció con una mejora del 16% sobre ondansetron para el criterio de valoración sin vómitos.
|
n/m = Número de respondedores/número de pacientes en análisis. |
||||
|
∆ Diferencia (%):Aprepitant 40 mg menos Ondansetron. |
||||
|
*Razón de probabilidad estimada: Aprepitant 40 mg versus Ondansetron. |
||||
|
†No estadísticamente significativo después del ajuste de multiplicidad preespecificado. |
||||
| Tratamiento | n/m (%) | Aprepitant vs. Ondansetron | ||
| ∆ | Razón de probabilidad * | Análisis | ||
| CRITERIO DE VALORACIÓN PRINCIPAL | ||||
| Respuesta completa (sin emesis y sin terapia de rescate, 0 a 24 horas) |
||||
| Aprepitant 40 mg | 111/248 (44.8) | 2.5% | 1.1 | 0.61 |
| Ondansetron | 104/246 (42.3) | |||
| CRITERIOS DE VALORACIÓN SECUNDARIOS | ||||
| Sin vómitos (sin episodios eméticos, 0 a 24 horas) |
||||
| Aprepitant 40 mg | 223/248 (89.9) | 16.3% | 3.2 | <0.001† |
| Ondansetron | 181/246 (73.6) | |||
| Sin uso de medicación de rescate (para emesis o náuseas establecidas, 0 a 24 horas) |
||||
| Aprepitant 40 mg | 112/248 (45.2) | -0.7% | 1.0 | 0.83 |
| Ondansetron | 113/246 (45.9) | |||
| Sin vómitos 0 a 48 horas (superioridad) (sin episodios eméticos, 0 a 48 horas) | ||||
| Aprepitant 40 mg | 209/247 (84.6) | 17.7% | 2.7 | <0.001* |
| Ondansetron | 164/245 (66.9) | |||
16 FORMA DE SUMINISTRO/ALMACENAMIENTO Y MANIPULACIÓN
• Las cápsulas de Aprepitant, USP, 40 mg, son cápsulas de gelatina dura con cuerpo blanco y tapa amarilla con “40 mg” impreso en tinta negra en el cuerpo.
NDC 13668-591-81 Caja de 1 cápsula (que contiene 1 x 1 blíster de dosis única)
NDC 13668-591-82 Caja de 5 cápsulas (que contiene 5 x 1 blíster de dosis única)
• Las cápsulas de Aprepitant, USP, 80 mg, son cápsulas de gelatina dura con cuerpo blanco y tapa blanca con “80 mg” impreso en tinta negra en el cuerpo.
NDC 13668-592-84 Caja de 2 cápsulas (que contiene 2 x 1 blíster de dosis única)
NDC 13668-592-86 Caja de 6 cápsulas (que contiene 3 x 2 blísteres de dosis cada uno)
• Las cápsulas de Aprepitant, USP, 125 mg, son cápsulas de gelatina dura con cuerpo blanco y tapa rosada con “125 mg” impreso en tinta negra en el cuerpo.
NDC 13668-593-86 Caja de 6 cápsulas (que contiene 6 x 1 blíster de dosis única)
• Cápsulas de Aprepitant, USP, Tri-pack-wallet type, paquete de 3 días (125-mg/80-mg/80-mg)
80 mg, son cápsulas de gelatina dura con cuerpo blanco y tapa blanca con “80 mg” impreso en tinta negra en el cuerpo.
125 mg, son cápsulas de gelatina dura con cuerpo blanco y tapa rosada con “125 mg” impreso en tinta negra en el cuerpo.
Blíster de 2 cápsulas de 80 mg y 1 cápsula de 125 mg
NDC 13668-594-87 Caja de 3 cápsulas (blíster tri-pack de paquete de 3 días que contiene una cápsula de 125 mg y dos cápsulas de 80 mg)
Almacenamiento y manipulación
Cápsulas
Almacenar a 20 a 25°C (68 a 77°F) [ver USP Temperatura ambiente controlada].
17 INFORMACIÓN PARA EL PACIENTE
Aconseje al paciente que lea el etiquetado del paciente aprobado por la FDA (Información para el paciente).
Reacciones de hipersensibilidad
Avise a los pacientes que se han notificado reacciones de hipersensibilidad, incluida la anafilaxia, en pacientes que toman aprepitant. Avise a los pacientes que dejen de tomar aprepitant y busquen atención médica inmediata si experimentan signos o síntomas de una reacción de hipersensibilidad, como urticaria, erupción cutánea y picazón, descamación o llagas en la piel, o dificultad para respirar o tragar.
Interacciones medicamentosas
Avise a los pacientes que discutan todos los medicamentos que están tomando, incluidos otros medicamentos recetados, de venta libre o productos herbales [ver Contraindicaciones (4), Advertencias y precauciones (5.1)].
Warfarina: Instruya a los pacientes en terapia crónica con warfarina que sigan las instrucciones de su proveedor de atención médica con respecto a los análisis de sangre para controlar su INR durante el período de 2 semanas, particularmente a los 7 a 10 días, después del inicio del régimen de 3 días de aprepitant con cada ciclo de quimioterapia, o después de la administración de una sola dosis de 40 mg de aprepitant para la prevención de náuseas y vómitos posoperatorios [ver Advertencias y precauciones (5.2)].
Anticonceptivos hormonales: Avise a los pacientes que la administración de aprepitant puede reducir la eficacia de los anticonceptivos hormonales. Instruya a los pacientes a utilizar métodos anticonceptivos alternativos o de respaldo efectivos (como condones y espermicidas) durante el tratamiento con aprepitant y durante 1 mes después de la última dosis de aprepitant [ver Advertencias y precauciones (5.3), Uso en poblaciones específicas (8.3)].

PHARMATHEN INTERNATION S.A., Rodopi 69300, GRECIA (GRC)
Fabricado para:
TORRENT PHARMA INC., Basking Ridge, NJ 07920
Revisado: 06/2022
2823402/3
INFORMACIÓN PARA EL PACIENTE
(a-PRE-pi-tant)
Lea esta Información para el Paciente antes de comenzar a tomar aprepitant y cada vez que reciba una nueva receta. Puede haber nueva información. Esta información no reemplaza hablar con su proveedor de atención médica sobre su condición médica o tratamiento.
¿Qué son las Cápsulas de Aprepitant?
Las cápsulas de aprepitant son un medicamento recetado que se usa:
● Con otros medicamentos que tratan las náuseas y los vómitos en pacientes de 12 años de edad o mayores para prevenir las náuseas y los vómitos causados por ciertos medicamentos contra el cáncer (quimioterapia)
● En adultos para prevenir las náuseas y los vómitos después de la cirugía.
Las cápsulas de aprepitant no se usan para tratar las náuseas y los vómitos que ya tiene.
Las cápsulas de aprepitant no deben usarse continuamente durante un período prolongado (uso crónico)
¿Quién no debe tomar cápsulas de aprepitant?
No tome cápsulas de aprepitant si usted:
● es alérgico a aprepitant o a cualquiera de los ingredientes de las cápsulas de aprepitant. Consulte el final de este folleto para obtener una lista completa de los ingredientes de las cápsulas de aprepitant.
● está tomando pimozide (ORAP®)
¿Qué debo decirle a mi proveedor de atención médica antes de tomar cápsulas de aprepitant?
Antes de tomar cápsulas de aprepitant, informe a su proveedor de atención médica si usted:
● tiene problemas hepáticos
● está embarazada o planea quedar embarazada. No se sabe si las cápsulas de aprepitant pueden dañar a su bebé nonato.
○ Las mujeres que usan medicamentos anticonceptivos que contienen hormonas para prevenir el embarazo (píldoras anticonceptivas, parches para la piel, implantes y ciertos
DIU) también deben usar un método anticonceptivo de respaldo que no contenga hormonas, como condones y espermicidas, durante
el tratamiento con cápsulas de aprepitant y durante 1 mes después de su última dosis de cápsulas de aprepitant.
● está amamantando o planea amamantar. No se sabe si aprepitant pasa a la leche materna. Hable con su proveedor de atención médica sobre la mejor manera de alimentar a su bebé si toma cápsulas de aprepitant.
Informe a su proveedor de atención médica sobre todos los medicamentos que toma, incluidos los medicamentos recetados y de venta libre, las vitaminas y los suplementos herbales.
Las cápsulas de aprepitant pueden afectar la forma en que funcionan otros medicamentos, y otros medicamentos pueden afectar la forma en que funcionan las cápsulas de aprepitant, causando efectos secundarios graves.
Conozca los medicamentos que toma. Mantenga una lista de ellos para mostrársela a su proveedor de atención médica o farmacéutico cuando obtenga un nuevo medicamento.
¿Cómo debo tomar las cápsulas de aprepitant?
● Tome las cápsulas de aprepitant exactamente como se lo recetaron.
● Trague las cápsulas de aprepitant enteras.
● Si está recibiendo quimioterapia, las cápsulas de aprepitant se pueden tomar con o sin alimentos.
● Si toma demasiado aprepitant, llame a su proveedor de atención médica o vaya a la sala de emergencias del hospital más cercano.
● Si está recibiendo quimioterapia contra el cáncer, las cápsulas de aprepitant se toman en 3 dosis durante 3 días, comenzando el día en que recibe la quimioterapia y durante los 2 días siguientes.
● En adultos que están recibiendo quimioterapia, hay 2 formas en que su proveedor de atención médica puede recetarle cápsulas de aprepitant:
Cápsulas de aprepitant por vía oral para las 3 dosis:
○ Debe obtener un paquete que tenga 3 cápsulas de aprepitant.
○ Día 1 (Día de la quimioterapia): Tome una cápsula de 125 mg de aprepitant (blanca y rosada) por vía oral 1 hora antes de comenzar su
tratamiento de quimioterapia.
○ Día 2 y Día 3: Tome una cápsula de 80 mg de aprepitant (blanca) por vía oral 1 hora antes de comenzar su tratamiento de quimioterapia. Si no
se administra tratamiento de quimioterapia en los Días 2 y 3, aprepitant debe tomarse por la mañana.
● En niños de 12 años de edad o mayores que pueden tragar cápsulas por vía oral, aprepitant se prescribe como cápsulas de aprepitant por vía oral para las 3 dosis:
○ Debe obtener un paquete que tenga 3 cápsulas de aprepitant.
○ Día 1 (Día de la quimioterapia): Tome una cápsula de 125 mg de aprepitant (blanca y rosada) por vía oral 1 hora antes de comenzar su
tratamiento de quimioterapia.
○ Día 2 y Día 3: Tome una cápsula de 80 mg de aprepitant (blanca) por vía oral 1 hora antes de comenzar su tratamiento de quimioterapia. Si no
se administra tratamiento de quimioterapia en los Días 2 y 3, aprepitant debe tomarse por la mañana.
● Si usted es un adulto y se va a someter a una cirugía:
○ Su médico le recetará una cápsula de 40 mg de aprepitant antes de la cirugía. Tome una cápsula de aprepitant dentro de las 3 horas previas a la cirugía.
○ Siga las instrucciones de su médico sobre las restricciones para comer y beber antes de la cirugía.
● Si toma el medicamento anticoagulante warfarina sódica (COUMADIN®, JANTOVEN®), su proveedor de atención médica puede hacerle análisis de sangre después de tomar aprepitant para verificar su coagulación sanguínea.
¿Cuáles son los posibles efectos secundarios de las cápsulas de aprepitant?
● En adultos que toman cápsulas de aprepitant, los efectos secundarios más comunes incluyen cansancio, diarrea, debilidad, indigestión, dolor de estómago (abdominal), hipo, disminución del recuento de glóbulos blancos, deshidratación y cambios en las pruebas de función hepática.
● En adultos que toman cápsulas de aprepitant para prevenir las náuseas y los vómitos después de la cirugía, el efecto secundario más común incluye estreñimiento, presión arterial baja (hipotensión).
● En niños de 6 meses a 17 años de edad, los efectos secundarios más comunes incluyen disminución del recuento de glóbulos blancos, dolor de cabeza, diarrea, disminución del apetito, tos, cansancio, disminución del recuento de glóbulos rojos, mareos e hipo.
Informe a su proveedor de atención médica si tiene algún efecto secundario que le moleste o que no desaparezca. Estos no son todos los posibles efectos secundarios de las cápsulas de aprepitant. Para obtener más información, consulte a su proveedor de atención médica o farmacéutico.
Llame a nuestro proveedor de atención médica para obtener asesoramiento médico sobre los efectos secundarios. Puede informar los efectos secundarios a la FDA al 1-800-FDA-1088.
¿Cómo debo almacenar las cápsulas de aprepitant?
● Almacenar a temperatura ambiente, entre 68° y 77°F (20° y 25°C).
Mantenga las cápsulas de aprepitant y todos los medicamentos fuera del alcance de los niños.
Información general sobre el uso seguro y eficaz de las cápsulas de aprepitant
Los medicamentos a veces se recetan para fines distintos a los que se enumeran en el folleto de información para el paciente. No use cápsulas de aprepitant para una afección para la que no se haya recetado. No le dé cápsulas de aprepitant a otras personas, incluso si tienen los mismos síntomas que usted. Puede dañarlos. Puede solicitar a su proveedor de atención médica o farmacéutico información sobre las cápsulas de aprepitant escrita para profesionales de la salud. Para obtener más información sobre aprepitant, llame al 1-800-912-9561.
¿Cuáles son los ingredientes en las cápsulas de aprepitant?
Ingrediente activo: aprepitant
Ingredientes inactivos: hipromelosa 2910, poloxámero 407, sacarosa, celulosa microcristalina. La tinta de impresión: barniz de laca, óxido de hierro negro y propilenglicol. Los excipientes de la cápsula: gelatina, dióxido de titanio y sulfato de laurilo de sodio. La cápsula de 40 mg contiene óxido férrico amarillo, sulfato de laurilo de sodio y dióxido de titanio, la cápsula de 80 mg contiene sulfato de laurilo de sodio y dióxido de titanio, las cápsulas de 125 mg contienen óxido férrico rojo, sulfato de laurilo de sodio y dióxido de titanio.

PHARMATHEN INTERNATION S.A., Rodopi 69300, GRECIA (GRC)
Fabricado para:
TORRENT PHARMA INC. Basking Ridge, NJ 07920
Revisado: 06/2022
ETIQUETA DEL PAQUETE. PANEL DE VISUALIZACIÓN PRINCIPAL
Cartón de Cápsula de Aprepitant, USP 40 mg

Cartón de Cápsula de Aprepitant, USP 80 mg

Cartón de Cápsula de Aprepitant, USP 125 mg
Cartón de Cápsula de Aprepitant, USP (80 mg y 125 mg Kit)